CN101605529B - 稳定制剂及它们的制备和使用方法 - Google Patents
稳定制剂及它们的制备和使用方法 Download PDFInfo
- Publication number
- CN101605529B CN101605529B CN2007800049514A CN200780004951A CN101605529B CN 101605529 B CN101605529 B CN 101605529B CN 2007800049514 A CN2007800049514 A CN 2007800049514A CN 200780004951 A CN200780004951 A CN 200780004951A CN 101605529 B CN101605529 B CN 101605529B
- Authority
- CN
- China
- Prior art keywords
- preparation
- work
- approximately
- liquid preparation
- rapamycin
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/436—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a six-membered ring having oxygen as a ring hetero atom, e.g. rapamycin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4738—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems
- A61K31/4745—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems condensed with ring systems having nitrogen as a ring hetero atom, e.g. phenantrolines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K33/00—Medicinal preparations containing inorganic active ingredients
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/08—Solutions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
- A61P27/06—Antiglaucoma agents or miotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
- A61P27/14—Decongestants or antiallergics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01F—MIXING, e.g. DISSOLVING, EMULSIFYING OR DISPERSING
- B01F33/00—Other mixers; Mixing plants; Combinations of mixers
- B01F33/40—Mixers using gas or liquid agitation, e.g. with air supply tubes
Abstract
本文所述是包含治疗物质的制剂,包括但不限于包含雷帕霉素的制剂、药物制剂、单位剂量形式、药盒、制备制剂的方法和使用制剂的方法。这些制剂和方法具有提高的稳定性。
Description
技术领域
本文所述是包含治疗物质的制剂及它们的制备和使用方法。本文所述是雷帕霉素制剂及它们的制备和使用方法。
相关申请的交叉引用
本申请涉及并要求2006年2月9日提交的题目为“稳定制剂及它们的制备和使用方法”的美国临时专利申请序列号60/772,018的优先权,将其全部内容引入文中作为参考,用于所有目的。
背景技术
许多包含治疗物质的制剂对一种或多种因素或条件是敏感的,这些因素或条件致使它们在一段时间后例如贮存一段时间时后不稳定。一种这样的因素或条件是对制剂周围空间(例如包含制剂的容器的死腔或顶空)中空气的一种或多种有关成分(element)(包括但并不限于氧气)的敏感性。另一种这样的因素或条件是在制剂中存在气体或溶解的气体(包括但并不限于氧气)或者制剂的一种或多种有关成分暴露于光线、污染物质或有机体例如细菌下。另一种这样的条件或因素是顶空体积与填充体积的比例。另一种这样的条件或因素是相对于制剂中一种或多种成分的量的特定分子的量,包括但不限于制剂的活性物质。
以前使制剂稳定的方法包括添加一种或多种抗氧化剂例如BHT(丁基化羟基甲苯)或抗坏血酸棕榈酸酯。抗坏血酸棕榈酸酯通常用于口服或局部药物,不用于注射剂。药物赋形剂手册2003(Handbook of PharmaceuticalExcipients 2003),美国药学会(American Pharmaceutical Association),华盛顿,DC,USA和药物出版社(Pharmaceutical Press),伦敦,UK。在药物赋形剂手册(2003)中,BHT被建议以约0.0009%至约0.002%的水平用于静脉注射。当给药于眼组织时,认为这些用于稳定的抗氧化剂在某些水平上是有毒的。优选不需要另外的制剂有关成分(包括但不限于防腐剂)来维持它们的稳定性的稳定制剂。
需要有如下制剂,包括药物制剂,当其被贮存一段时间时,其保留含有治疗物质的制剂中存在的一种或多种治疗物质或其它有关成分的稳定性。需要有包含对暴露于空气的一种或多种有关成分下敏感的治疗物质的稳定制剂。需要有雷帕霉素的稳定制剂。
发明内容
本文所述是包含治疗物质的稳定制剂(包括包含雷帕霉素的稳定制剂)、药物制剂、单位剂量形式、药盒(kit)、制备稳定制剂的方法、和使用稳定制剂的方法。稳定制剂包括但不限于溶液剂、混悬剂、自乳化制剂、和原位胶化制剂。
本文所述是包含治疗物质(包括但不限于雷帕霉素)的液体制剂,其包含比没有用氮气鼓泡通入(sparging)情况下制备的制剂的氮气水平高至少约50%的溶解的氮气水平。
本文所述是包含治疗物质(包括但不限于抑免蛋白结合化合物或雷帕霉素)的液体制剂,其包含在溶解的气体中不大于20%、不大于19%、不大于17.5%或不大于16.5%的氧气水平。
本文所述是包含治疗物质(包括但不限于抑免蛋白结合化合物或雷帕霉素)的液体制剂,其包含在溶解气体中大于80%、大于85%、大于90%或大于95%的氮气水平。
本文所述是包含含有抑免蛋白结合化合物的液体制剂的密封容器,其中液体制剂与顶空气体接触,该顶空气体含有不多于20%的氧气、不多于15%的氧气、不多于10%的氧气或不多于5%的氧气。
本文所述是包含含有抑免蛋白结合化合物的液体制剂的密封容器,其中液体制剂与顶空气体接触,该顶空气体含有大于80%的氮气、大于85%的氮气、大于90%的氮气或大于95%的氮气。
本文所述是包含雷帕霉素的眼科可接受的液体制剂,其中在-20℃、5℃或25℃的一个或多个温度下贮存一周后,制剂强度至少是70%;在-20℃、5℃或25℃的一个或多个温度下贮存两周后,制剂强度至少是80%;在-20℃、5℃或25℃的一个或多个温度下贮存一个月后,制剂强度至少是90%;在-20℃、5℃或25℃的一个或多个温度下贮存两个月后,制剂强度至少是90%;在-20℃或5℃的一个或多个温度下贮存八个月后,制剂强度至少是90%。
本文所述是包含治疗物质的液体制剂,该治疗物质对空气中的一种或多种成分敏感,其中,在25℃经过至少两个月制剂强度至少是70%,在25℃经过至少两个月制剂强度至少是80%,在25℃经过至少两个月制剂强度至少是90%,在25℃经过至少两个月制剂强度至少是95%;并且,其中,该制剂不包含对眼睛的一种或多种组织有毒的防腐剂。本文所述是包含治疗物质的液体制剂,该治疗物质对空气中的一种或多种成分敏感,其中,在5℃经过至少八个月制剂强度至少是70%,在5℃经过至少八个月制剂强度至少是80%,在5℃经过至少八个月制剂强度至少是90%,并且,其中该制剂不包含对眼睛的一种或多种组织有毒的防腐剂。
本文所述是包含治疗物质(包括但不限于雷帕霉素)的液体制剂,该制剂包含对空气中的一种或多种成分敏感的治疗物质,其中经包装后制剂在25℃和60%相对湿度下稳定至少约3个月,并且,其中该制剂不包含对眼睛的一种或多种组织有毒的抗氧化剂。在一些变通方案中,经包装后,制剂在5℃稳定至少约12个月。在一些变通方案中,经包装后,制剂在-20℃稳定至少约12个月。
在一些变通方案中,在25℃和60%相对湿度下经过至少1周、2周、1个月和2个月,制剂强度至少是60%。在一些变通方案中,在25℃和60%相对湿度下经过至少1周、2周、1个月、2个月、3个月、4个月、8个月、10个月、12个月、14个月、16个月、18个月、20个月、22个月或24个月,制剂强度至少是80%。在一些变通方案中,在25℃和60%相对湿度下经过至少1周、2周、1个月、2个月、3个月、4个月、8个月、10个月、12个月、14个月、16个月、18个月、20个月、22个月或24个月,制剂强度至少是90%。
在一些变通方案中,在5℃经过至少1周、2周、1个月、2个月、3个月、4个月、8个月、10个月、12个月、14个月、16个月、18个月、20个月、22个月或24个月,制剂强度至少是60%。在一些变通方案中,在5℃经过至少1周、2周、1个月、2个月、4个月、8个月、10个月、12个月、14个月、16个月、18个月、20个月或24个月,制剂强度至少是80%。在一些变通方案中,在5℃经过至少1周、2周、1个月、2个月、4个月、8个月、10个月、12个月、14个月、16个月、18个月、20个月、22个月或24个月,制剂强度至少是90%。
在一些变通方案中,在-20℃经过至少1周、2周、1个月、2个月、4个月、8个月、10个月、12个月、14个月、16个月、18个月、20个月、或24个月,制剂强度至少是60%。在一些变通方案中,在-20℃经过至少1周、2周、1个月、2个月、4个月、8个月、10个月、12个月、14个月、16个月、18个月、20个月、22个月或24个月,制剂强度至少是80%;在一些变通方案中,在-20℃经过至少1周、2周、1个月、2个月、4个月、8个月、10个月、12个月、14个月、16个月、18个月、20个月、22个月或24个月,制剂强度至少是90%。
在一些变通方案中,液体制剂是稳定的药物制剂。在一些变通方案中液体制剂是无菌的。
在一些变通方案中,本文所述的液体制剂通过以下方法制备,所述方法包括下述中的一种或多种:超声、蒸发、用惰性气体鼓泡、加热、离心或用惰性气体将液体制剂中的一种或多种组分覆盖。
在一些变通方案中,当眼内或眼周给药时,稳定的制剂或药物制剂递送对治疗、预防眼睛疾病或病症或者延迟其发作有效的一定量的治疗物质。
在一些变通方案中,当眼内或眼周给药时,液体制剂递送对治疗、预防眼睛疾病或病症或者延迟其发作有效的一定量的治疗物质,递送在给药液体制剂后持续至少30天的时间。
在一些变通方案中,液体制剂是在液体介质中的溶液剂、混悬剂、乳液、自乳化制剂、凝胶剂或原位胶化制剂。
在一些变通方案中,对于填充体积少于约50μl而言,对容器进行设计以使表面积和体积的比率降到最低。
在一些变通方案中,本文所述的液体制剂具有的顶空体积与液体制剂体积的比率不大于1.5。在一些变通方案中,顶空体积与液体制剂体积的比率不大于0.5。
在一些变通方案中,对于液体制剂中的每毫克活性物质来讲,本文所述的液体制剂在顶空中含有不多于1μl的氧气。在一些变通方案中,对于液体制剂中的每毫克活性物质来讲,本文所述液体制剂在顶空中含有不多于0.5μl的氧气。在一些变通方案中,对于液体制剂中的每毫克活性物质来讲,本文所述液体制剂在顶空中含有不多于0.25μl的氧气;在一些变通方案中,对于液体制剂中的每毫克活性物质来讲,本文所述液体制剂在顶空中含有不多于0.09μl的氧气。
在一些变通方案中,包含液体制剂的容器被次级包装包围,该次级包装减少液体制剂暴露于其下的光照的量。
本文提供的是包含如文中所述的液体制剂的单位剂量形式。在一些变通方案中,单位剂量形式在预装注射器中。
在一些变通方案中,治疗物质是抑免蛋白结合化合物,包括但不限于雷帕霉素、SDZ-RAD、他克莫司、依维莫司、吡美莫司、CCI-779、AP23841、ABT-578和它们的前药、类似物、衍生物、盐和酯。在一些变通方案中,治疗物质是雷帕霉素。
在一些变通方案中,本文所述的稳定的制剂或药物制剂包括表2所述的任何液体制剂。
在一些变通方案中,被治疗、预防或延迟发作的眼睛疾病或病症是血管发生。在一些变通方案中,血管发生是脉络膜新生血管形成。
本文提供的是制备包含对一种或多种空气成分敏感的一种或多种制剂成分的稳定制剂的方法,其中该方法包括减少一种或多种制剂成分在一种或多种空气成分下的暴露,其中该方法不包括添加对眼睛有的抗氧化剂或防腐剂。
在一些变通方案中,所述方法包括超声、用惰性气体鼓泡、加热、离心或用惰性气体将液体制剂中的一种或多种成分覆盖中的任何一种或多种。在一些变通方案中,稳定制剂中的一种或多种成分对空气中的一种或多种成分是敏感的,所述空气的一种或多种成分是氧气。在一些变通方案中,惰性气体是稀有气体。在一些变通方案中,稀有气体是氮气。在一些变通方案中,所述方法包括下述处理中的任何两种或多种:超声液体制剂中的一种或多种成分、向液体制剂中的一种或多种成分中鼓泡通入惰性气体或用惰性气体覆盖液体制剂中的一种或多种成分。在一些变通方案中,所述方法包括:超声液体制剂中的一种或多种成分、向液体制剂中的一种或多种成分中鼓泡通入惰性气体和用惰性气体覆盖液体制剂中的一种或多种成分。
在一些变通方案中,稳定制剂是稳定的药物制剂。
本文提供的是在个体(包括但不限于人类个体)中治疗、预防眼睛疾病或病症或者延迟其发作的方法,该方法包括将本文所述的稳定的制剂或药物制剂给药至个体的眼睛。在一些变通方案中,眼睛的疾病或病症是脉络膜新生血管形成、AMD、葡萄膜炎、变应性结膜炎、干眼、青光眼、色素性视网膜炎、视网膜中央静脉阻塞疾病、视网膜血管疾病、黄斑水肿、虹膜新生血管形成、糖尿病性视网膜病变、角膜新生血管生成或角膜移植排斥。在一些变通方案中,眼睛的疾病或病症是人类个体中的年龄相关性黄斑变性,且治疗物质包括雷帕霉素,其中将液体制剂给药至个体眼睛的位置或接近于个体眼睛的位置。在一些变通方案中,液体制剂将治疗有效量的雷帕霉素递送至人类个体,在给药后递送持续很长的一段时间。在一些变通方案中,液体制剂将治疗有效量的雷帕霉素递送到人类个体,给药后递送持续至少30天。在一些变通方案中,液体制剂是雷帕霉素在液体介质中的溶液剂、混悬剂或乳剂。在一些变通方案中,将稳定药物制剂给药至选自玻璃体、结膜、巩膜和结膜之间、巩膜中或接近于巩膜处、眼睛筋膜囊下(subtenon)、眼球后和后部巩膜旁(posterior juxtascleral)的部位。在一些变通方案中,将液体制剂给药至人类个体的眼睛的玻璃体。在一些变通方案中,将液体制剂给药至人类个体眼睛的巩膜和结膜之间。在一些变通方案中,将液体制剂给药至具有至少约20/40的视力的眼睛。在一些变通方案中,年龄相关性黄斑变性是湿性年龄相关性黄斑变性。在一些变通方案中,年龄相关性黄斑变性是干性年龄相关性黄斑变性。在一些变通方案中,个体是人类个体。
附图说明
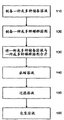
图1A-1F描述了制备本文所述制剂的方法的变通方案。
图2描述了制备本文所述制剂的一种变通方案。
图3显示在1周(1W)、2周(2W)、1个月(1M)和两个月(2M)时,顶空中的氧气百分数对制剂强度百分数;将处理组在顶空处理内进行平均(例如,将来自处理组1-7的所有样品进行平均,将来自处理组8-12的所有样品进行平均和将来自处理组13的所有样品进行平均)。
图4显示在1周(1W)、2周(2W)、1个月(1M)和两个月(2M)时,溶解的气体中的氧气百分数对制剂强度百分数;将处理组在顶空处理范围内进行平均(例如,将来自处理组1-7的所有样品进行平均,将来自处理组8-12的所有样品进行平均,以及将来自处理组13的所有样品进行平均)。
图5显示对于处理组1、8和13(没有用氧气鼓泡的处理组)而言,在1周(1W)、2周(2W)、1个月(1M)和两个月(2M)时,制剂强度百分数相对于顶空中的氧气百分数。
图6A显示在25℃,顶空中氧气的量对2%雷帕霉素溶液的制剂强度的影响。图6B显示在25℃,顶空与填充体积的比率(HS/FV)对2%雷帕霉素溶液的制剂强度的影响。图6C显示在25℃,顶空中氧气的量对2%雷帕霉素溶液的制剂强度的影响。
图7A显示在5℃,顶空中氧气的量对2%雷帕霉素溶液的制剂强度的影响。图7B显示在5℃,顶空与填充体积的比率(HS/FV)对2%雷帕霉素溶液的制剂强度的影响。
图8A显示在-20℃,顶空中氧气的量对2%雷帕霉素溶液的制剂强度的影响。图8B显示在-20℃,顶空与填充体积的比率(HS/FV)对2%雷帕霉素溶液的制剂强度的影响。
表1描述了各种方法因素导致的雷帕霉素稳定性的随时间的变化。
表2描述了可以根据本文所述方法制备的制剂的非限制性示例。
表3概述了处理组、它们在顶空和溶解的气体中的氧气平均百分数和在1周、2周、1个月和两个月时制剂强度百分数。
表4显示了制剂强度、顶空与填充体积的比率和每一定量的雷帕霉素(西罗莫司)的氧气量的随时间推移的数据,图6A、6B、7A、7B、8A和8B基于此数据绘制。
表5显示了制剂强度、顶空中的氧气百分数和每一定量的雷帕霉素(西罗莫司)的氧气量的随时间推移的数据,图6C基于此数据绘制。
发明详述
本文所述的是制剂、药物制剂、单位剂量形式、药盒以及制备和使用本文所述稳定制剂的方法。这些稳定的制剂或药物制剂可以用本文所述的一种或多种方法制备。在一些变通方案中,稳定制剂包含一种或多种对空气中的一种或多种成分敏感的成分。在一些变通方案中,治疗物质对空气中的一种或多种成分(包括但不限于氧气)敏感。在一些变通方案中,治疗物质是雷帕霉素。
在一些变通方案中,将本文所述的稳定的制剂和药物制剂用于治疗、预防、抑制本文中所述的一种或多种疾病和病症(包括但不限于眼睛疾病或病症,包括但不限于后段(posterior segment)的疾病或病症)、延迟其发作或致使其消退。在一些变通方案中,疾病或病症包括脉络膜新生血管形成、黄斑变性、年龄相关性黄斑变性包括湿性年龄相关性黄斑变性(“AMD”)和干性AMD、视网膜新生血管形成、慢性葡萄膜炎和其它的视网膜增生病症中的一种或多种。
本文描述了(1)稳定制剂,(2)用于稳定制剂的治疗物质的非限制性示例,(3)稳定制剂的成分,(4)药物制剂,(5)制备和包装治疗物质的液体制剂的方法,(6)可以通过递送治疗物质来治疗、预防、抑制、延迟其发作或致使其消退的疾病或病症的非限制性示例,(7)用于递送液体制剂的给药途径,和(8)采用本文所述的稳定的制剂和药物制剂通过递送雷帕霉素至个体(包括但不限于人类个体)或个体的眼睛来治疗CNV和湿性AMD。
如本文所用,术语“约”指当本文所述的方法例如实施例中的方法被使用时所得到的精确程度。
稳定的制剂和药物制剂
除非上下文中另外清楚地说明,本文所述的任何制剂或药物制剂能够通过本文所述的方法制备。除非上下文另外清楚地说明,如本文所述制备的任何制剂或药物制剂是如本文所述那样稳定的。本文所述的稳定的制剂和药物制剂的非限制性示例是稳定的溶液剂、乳剂、自乳化制剂、凝胶制剂、原位胶化制剂、混悬剂或纳米混悬剂。稳定的非液体制剂的非限制性示例包括非液体或固体制剂,包括但不限于多聚体植入物或片剂。除非上下文中另外清楚地说明,通过改变溶解的氮气或氧气水平中的任何一个或多个水平到本文所述的水平,可以使任何液体制剂稳定。除非上下文中另外清楚地说明,通过改变顶空气体中的氮气或氧气水平中的任何一个或多个水平到本文所述的水平,可以使任何液体制剂稳定。除非上下文中另外清楚地说明,通过如本文所述改变顶空和填充体积的比例,可以使任何液体制剂稳定。除非上下文中另外清楚地说明,通过改变在本文所述的液体制剂中的有关成分的微升数,包括但不限于相对于每毫克制剂成分的顶空中氧气的量,包括但不限于活性成分例如雷帕霉素的毫克数,可以使任何液体制剂稳定。除非上下文中另外清楚地说明,如果通过本文所述的方法中的一个或多个步骤制备,可以将表2所示的任何液体制剂制备成本文所述的稳定制剂,且本文所述的任何一种稳定制剂可以用于本文所述的方法。表2列出的制剂是指一种或多种溶液剂(″S″)、混悬剂(″SP″)、原位胶化制剂(″ISG″)或自乳化制剂(SEF)。这些制剂的详细说明可见例如2006年2月9日提交的待审的11/351,761,代理人案卷号57796-20004.00,题目为“用于治疗疾病或病症的液体制剂(LIQUID FORMULATIONS FORTREATMENT OF DISEASES OR CONDITIONS)”,和2005年2月9日提交的US 60/664,040,代理人案卷号57796-30004.00,题目为“用于治疗疾病或病症的液体制剂”,将其各自以全部内容引入文中作为参考。
本文所述的“稳定制剂”是包含治疗物质的制剂,其中相对于制剂刚刚制备时,贮存一段时间后它保留至少约60%制剂强度的物质;换言之,稳定制剂是包含治疗物质的制剂,其中相对于制剂刚被制备时的治疗物质的起始水平,至少约60%的制剂强度得以保留。在一些变通方案中,本文所述的稳定制剂贮存一段时间后,相对于制剂中治疗物质的起始水平保留至少约60%、至少约65%、至少约70%、至少约75%、至少约80%、至少约85%、至少约90%、至少约92%、至少约94%、至少约95%、至少约96%、至少约98%或至少约99%的治疗物质水平。在一些变通方案中,制剂贮存一段时间是稳定的,所述一段时间是至少约1个月、至少约2个月、至少约3个月、至少约4个月、至少约5个月、至少约6个月、至少约7个月、至少约8个月、至少约9个月、至少约12个月、至少约18个月或至少约24个月。在一些变通方案中,制剂包含雷帕霉素或其前药、类似物、衍生物、盐或酯。在一些变通方案中,稳定制剂包含雷帕霉素。
本文所述的“稳定的药物制剂”是包含治疗物质的制剂,贮存一段时间后相对于药物制剂中的治疗物质的起始水平,该制剂保留至少约90%的治疗物质的水平。在一些变通方案中,药物制剂贮存一段时间是稳定的,所述一段时间是至少约1个月、至少约2个月、至少约3个月、至少约4个月、至少约5个月、至少约6个月、至少约7个月、至少约8个月、至少约9个月、至少约12个月、至少约18个月或至少约24个月。在一些变通方案中,稳定的药物制剂包含雷帕霉素或其前药、类似物、衍生物、盐或酯。在一些变通方案中,稳定的药物制剂包含雷帕霉素。
在一些变通方案中,本文所述的稳定制剂和稳定的药物制剂在5℃、25℃或-20℃的任何一个或多个温度下贮存一段时间后是稳定的。
本文所述的稳定制剂和稳定的药物制剂通常可以通过能够生产本文所述的制剂和药物制剂的任何方法进行制备,包括不限于一种或多种本文所述方法。在一些变通方案中,仅通过用于制备和贮存它们的方法而使本文所述的稳定制剂和稳定的药物制剂稳定。
正如本文所用,“眼科可接受的”制剂是不含能引起临床不可接受程度的对眼睛的刺激的水平的一种或多种成分的制剂。这些刺激的非限制性示例包括灼烧、刺激、搔痒、发红、肿胀和放电(discharge)。本领域技术人员能够确定制剂是否引起不可接受的对眼睛的刺激水平。在一些变通方案中,本文所述的眼科可接受的制剂引起不能察觉的对眼睛的刺激。
在一些变通方案中,本文所述的稳定制剂和稳定的药物制剂不包含对眼睛有毒的一种或多种在前面所述的稳定制剂和稳定的药物制剂中使用的抗氧化剂、防腐剂或化学稳定剂。在一些变通方案中,本文所述的稳定制剂和稳定的药物制剂不包含任何对眼睛有毒的在前面所述的稳定制剂和稳定的药物制剂中使用的防腐剂、抗氧化剂或化学稳定剂。所述抗氧化剂包括但不限于抗坏血酸、柠檬酸、亚硫酸钠、EDTA二钠、二硫苏糖醇(DTT)、延胡索酸、β-羟基苯甲醚(BHA)、没食子酸丙酯、α和β-生育酚、甲苯磺酸、酒石酸、硫代甘油、硫脲、甲醛合次硫酸氢钠、硫代硫酸钠、谷氨酸、丁基化羟基甲苯(BHT)、抗坏血酸棕榈酸酯、苄醇、苯扎氯铵和马来酸。在一些变通方案中,本文所述的稳定制剂和稳定的药物制剂不包含对眼睛有毒的BHT或抗坏血酸棕榈酸酯或其两者。在一些变通方案中,本文所述的稳定制剂和稳定的药物制剂不包含任何防腐剂、抗氧化剂或化学稳定剂。在一些变通方案中,本文所述的稳定制剂和稳定的药物制剂不包含任何BHT或抗坏血酸棕榈酸酯。本文所述的是无防腐剂、稳定的眼科制剂。本文所述的是无防腐剂、稳定的眼科药物制剂。
在一些变通方案中,本文所述的稳定制剂和药物制剂具有一定水平的氮气或其它惰性或稀有气体,所述水平在通过本文所述的一种或多种方法制备制剂时得到或可得到。
在一些变通方案中,本文所述的稳定制剂和药物制剂具有一定水平的空气中的氧气或其它有关成分,所述水平在通过本文所述的一种或多种方法制备制剂时得到或可得到。在一些变通方案中,本文所述的稳定制剂和药物制剂含有一定水平的溶解的氧气,所述水平相对于没有用氮气鼓泡或用氮气覆盖的制剂中所发现的氧气水平是降低的。在一些变通方案中,稳定制剂和药物制剂具有一定水平的溶解的氧气,所述水平在采用本文所述的一种或多种方法制备制剂时得到或可得到。
在一些变通方案中,在没有用氮气或其它稀有气体鼓泡的制剂中溶解的氧气的水平是约5至约9ppm。
在一些变通方案中,用氮气或其它稀有气体鼓泡的制剂中溶解的氧气水平是没有用氮气或其它稀有气体鼓泡的制剂中溶解的氧气水平的小于约95%、约90%、约80%、约70%、约60%、约50%、约40%、约30%、约20%或约10%。
本文所述的是液体制剂。在一些变通方案中,本文所述的液体制剂具有的顶空体积与液体制剂体积的比率不大于4.0、不大于3.5、不大于3.0、不大于2.5、不大于2.0、不大于1.5、不大于1.0、不大于0.5、不大于0.25、不大于0.2、不大于0.1。在一些变通方案中,顶空体积与液体制剂体积的比率不大于1.5。在一些变通方案中,顶空体积与液体制剂体积的比率不大于1.0。在一些变通方案中,顶空体积与液体制剂体积的比率不大于0.5。在一些变通方案中,顶空体积与液体制剂体积的比率不大于0.25。
本文所述的是液体制剂,其中随时间推移降低制剂强度的有关成分的量保持低于特定的水平,以在较长时间段中维持制剂强度。在一些变通方案中,使有关成分相对于每毫克制剂成分而言保持低于某种量。在一些变通方案中,制剂成分是活性物质。在一些变通方案中,随时间推移降低制剂强度的有关成分是氧气。
本文所述的是液体制剂,对于液体制剂中的每毫克活性物质而言,该液体制剂在顶空中含有不大于13μl、不大于12μl、不大于11μl、不大于10μl、不大于9μl、不大于8μl、不大于7μl、不大于6μl、不大于5μl、不大于4μl、不大于3μl、不大于2μl、不大于1.45μl、不大于1μl、不大于0.75μl、不大于0.55μl、不大于0.5μl、不大于0.25μl、不大于0.2μl、不大于0.1μl、不大于0.09μl、不大于0.05μl、不大于0.03μl、不大于0.01μl或不大于0.001μl的氧气。在一些变通方案中,对于液体制剂中的每毫克活性物质而言,本文所述的液体制剂在顶空中含有不大于1.45μl的氧气。在一些变通方案中,对于液体制剂中的每毫克活性物质而言,本文所述的液体制剂在顶空中含有不大于1μl的氧气。在一些变通方案中,对于液体制剂中的每毫克活性物质而言,液体制剂在顶空中含有不大于0.55μl的氧气。在一些变通方案中,对于液体制剂中的每毫克活性物质而言,液体制剂在顶空中含有不大于0.5μl的氧气。在一些变通方案中,对于液体制剂中的每毫克活性物质而言,液体制剂在顶空中含有不大于0.25μl的氧气。在一些变通方案中,对于液体制剂中的每毫克活性物质而言,液体制剂在顶空中含有不大于0.09μl的氧气。
本文所述是包含治疗物质(包括但不限于抑免蛋白结合化合物或雷帕霉素)的液体制剂,其包含在溶解的气体中大于80%、大于85%、大于90%或大于95%水平的氮气。
本文所述是包含含有抑免蛋白结合化合物的液体制剂的密封容器,其中液体制剂与顶空气体接触,顶空气体含有不大于20%的氧气、不大于15%的氧气、不大于10%的氧气或不大于5%的氧气。
本文所述是包含含有抑免蛋白结合化合物液体制剂的密封容器,其中液体制剂与顶空气体接触,顶空气体含有大于80%的氮气、大于85%的氮气、大于90%的氮气或大于95%的氮气。
在一些变通方案中,本文所述的稳定制剂和药物制剂包含雷帕霉素,且含有一定水平的氧气或空气中的其它有关成分,所述水平在通过本文所述的一种或多种方法制备制剂时得到或可得到。在一些变通方案中,本文所述的稳定制剂和药物制剂包含雷帕霉素,且含有一定水平的溶解的氧气,所述水平低于在没有用氮气鼓泡或用氮气覆盖的制剂中发现的溶解的氧气的水平。在一些变通方案中,稳定制剂和药物制剂包含雷帕霉素,且含有一定水平的溶解的氧气,所述水平在用本文所述的一种或多种方法制备制剂时得到或可得到。在一些变通方案中,在没有用氮气或其它稀有气体鼓泡的包含雷帕霉素的制剂中溶解的氧气水平是约5至约9ppm。在一些变通方案中,在用氮气或其它稀有气体鼓泡的包含雷帕霉素的制剂中溶解的氧气水平是在没有用氮气或其它稀有气体鼓泡的包含雷帕霉素的制剂中溶解的氧气水平的少于约95%、约90%、约80%、约70%、约60%、约50%、约40%、约30%、约20%或约10%。
在一些变通方案中,本文所述的稳定制剂和药物制剂含有一定水平的溶解的氮气,所述水平大于在没有用氮气鼓泡或用氮气覆盖的制剂中发现的溶解的氮气水平。在一些变通方案中,稳定制剂和药物制剂含有一定水平的溶解的氮气,所述水平在用本文所述的一种或多种方法制备制剂时得到或可得到。
本文所述是包含治疗物质(包括但不限于抑免蛋白结合化合物例如雷帕霉素)的液体制剂,该液体制剂具有不大于20%的在溶解的气体中的氧气百分比。在一些变通方案中,本文所述的液体制剂具有不大于19.5%、不大于19%、不大于18.5%、不大于18%、不大于17.5%、不大于17%、不大于16.5%、不大于16%、不大于15%、不大于13%、不大于11%、不大于9%、不大于7%、不大于5%、不大于3%或不大于1%的在溶解的气体中的氧气百分比。
在一些变通方案中,本文所述的液体制剂包含抑免蛋白结合化合物,且具有不大于18%的在溶解的气体中的氧气百分比。在一些变通方案中,本文所述的液体制剂包含雷帕霉素,且具有不大于18%的在溶解的气体中的氧气百分比。
在一些变通方案中,本文所述的液体制剂包含抑免蛋白结合化合物,且具有不大于16.5%的在溶解的气体中的氧气百分比。在一些变通方案中,本文所述的液体制剂包含雷帕霉素,且具有不大于16.5%的在溶解的气体中的氧气百分比。
在一些变通方案中,本文所述的液体制剂包含抑免蛋白结合化合物,且具有不大于15%的在溶解的气体中的氧气百分比。在一些变通方案中,本文所述的液体制剂包含雷帕霉素,且具有不大于15%的在溶解的气体中的氧气百分比。
在一些变通方案中,本文所述的液体制剂包含抑免蛋白结合化合物,且具有不大于10%的在溶解的气体中的氧气百分比。在一些变通方案中,本文所述的液体制剂包含雷帕霉素,且具有不大于10%的在溶解的气体中的氧气百分比。
本文所述是包含含有治疗物质(包括但不限于抑免蛋白结合化合物或雷帕霉素)的液体制剂的密封容器,其中液体制剂与顶空气体接触,所述顶空气体含有不大于20%的氧气。在一些变通方案中,液体制剂与含有不大于15%氧气的顶空气体接触。在一些变通方案中,液体制剂与含有不大于10%氧气的顶空气体接触。在一些变通方案中,液体制剂与含有不大于5%氧气的顶空气体接触。在一些变通方案中,治疗物质是抑免蛋白结合化合物。在一些变通方案中,治疗物质是雷帕霉素。
正如本文所用,“制剂强度”指相对于制剂刚刚被制备时在制剂中存在的治疗物质的重量而言,在特定时间时制剂中存在的治疗物质的重量百分数。
本文所述是包含治疗物质的眼科可接受的液体制剂,其中在-20℃、5℃或25℃中的一个或多个温度下贮存一周后,制剂强度是至少60%。在一些变通方案中,制剂强度是至少65%、至少70%、至少75%、至少80%、至少85%、至少95%、至少96%、至少97%、至少98%或至少99%。在一些变通方案中,治疗物质是抑免蛋白结合化合物或其前药、类似物、衍生物、盐或酯。在一些变通方案中,治疗物质是雷帕霉素。本文所述是包含雷帕霉素的眼科可接受的液体制剂,其中在-20℃、5℃或25℃中的一个或多个温度下贮存一周后,制剂强度是至少70%。本文所述是包含雷帕霉素的眼科可接受的液体制剂,其中在-20℃、5℃或25℃中的一个或多个温度下贮存一周后,制剂强度是至少80%。本文所述是包含雷帕霉素的眼科可接受的液体制剂,其中在-20℃、5℃或25℃中的一个或多个温度下贮存一周后,制剂强度是至少90%。本文所述是包含雷帕霉素的眼科可接受的液体制剂,其中在-20℃、5℃或25℃中的一个或多个温度下贮存一周后,制剂强度是至少95%。
本文所述是眼科可接受的液体制剂,其中在-20℃、5℃或25℃中的一个或多个温度下贮存两周后,制剂强度是至少65%、至少70%、至少75%、至少80%、至少85%、至少95%、至少96%、至少97%、至少98%或至少99%。在一些变通方案中,治疗物质是抑免蛋白结合化合物或其前药、类似物、衍生物、盐或酯。在一些变通方案中,治疗物质是雷帕霉素。
本文所述是眼科可接受的液体制剂,其中在-20℃、5℃或25℃中的一个或多个温度下贮存一个月后,制剂强度是至少65%、至少70%、至少75%、至少80%、至少85%、至少95%、至少96%、至少97%、至少98%或至少99%。在一些变通方案中,治疗物质是抑免蛋白结合化合物或其前药、类似物、衍生物、盐或酯。在一些变通方案中,治疗物质是雷帕霉素。
本文所述是包含治疗物质的眼科可接受的液体制剂,其中在-20℃、5℃或25℃中的一个或多个温度下贮存两个月后,制剂强度是至少80%。本文所述是包含抑免蛋白结合化合物或其前药、类似物、衍生物、盐或酯的眼科可接受的液体制剂,其中在-20℃、5℃或25℃中的一个或多个温度下贮存两个月后,制剂强度是至少80%。本文所述是包含雷帕霉素的眼科可接受的液体制剂,其中在-20℃、5℃或25℃中的一个或多个温度下贮存两个月后,制剂强度是至少80%。
本文所述是包含治疗物质的眼科可接受的液体制剂,其中在-20℃、5℃或25℃中的一个或多个温度下贮存两个月后,制剂强度是至少90%。本文所述是包含抑免蛋白结合化合物或其前药、类似物、衍生物、盐或酯的眼科可接受的液体制剂,其中在-20℃、5℃或25℃中的一个或多个温度下贮存两个月后,制剂强度是至少90%。本文所述是包含雷帕霉素的眼科可接受的液体制剂,其中在-20℃、5℃或25℃中的一个或多个温度下贮存两个月后,制剂强度是至少90%。
本文所述是包含治疗物质的眼科可接受的液体制剂,其中在-20℃或5℃的一个或多个温度下贮存八个月后,制剂强度是至少80%。本文所述是包含抑免蛋白结合化合物或其前药、类似物、衍生物、盐或酯的眼科可接受的液体制剂,其中在-20℃或5℃的一个或多个温度下贮存八个月后,制剂强度是至少80%。本文所述是包含雷帕霉素的眼科可接受的液体制剂,其中在-20℃或5℃或25℃中的一个或多个温度下贮存八个月后,制剂强度是至少80%。
本文所述是包含治疗物质的眼科可接受的液体制剂,其中在-20℃或5℃的一个或多个温度下贮存八个月后,制剂强度是至少90%。本文所述是包含抑免蛋白结合化合物或其前药、类似物、衍生物、盐或酯的眼科可接受的液体制剂,其中在-20℃或5℃的一个或多个温度下贮存八个月后,制剂强度是至少90%。本文所述是包含雷帕霉素的眼科可接受的液体制剂,其中在-20℃或5℃或25℃中的一个或多个温度下贮存八个月后,制剂强度是至少90%。
本文所述是包含治疗物质的液体制剂,该治疗物质对空气中的一种或多种成分敏感,其中在25℃和60%相对湿度下经过至少约一周、两周、一个月或两个月的时间后,制剂强度是至少70%,且其中制剂不包含对眼睛的一种或多种组织有毒的防腐剂。在一些变通方案中,在25℃和60%相对湿度下经过至少两周,制剂强度是至少75%、至少80%、至少85%、至少90%或至少95%。本文所述是包含治疗物质的液体制剂,该治疗物质对空气中的一种或多种成分敏感,其中经过至少一个月,治疗物质的制剂强度是至少70%、至少75%、至少80%、至少85%、至少90%或至少95%。本文所述是包含治疗物质的液体制剂,该治疗物质对空气中的一种或多种成分敏感,其中在25℃和60%相对湿度下经过至少两个月,治疗物质的制剂强度是至少70%、至少75%、至少80%、至少85%、至少90%或至少95%。
在一些变通方案中,本文所述的液体制剂在5℃经过至少约2个月、3个月、4个月、5个月、6个月、7个月、8个月、9个月、10个月、11个月、12个月、14个月、16个月、18个月、20个月、22个月或24个月的一段时间后具有至少80%的制剂强度。在一些变通方案中,本文所述的液体制剂在5℃经过至少约2个月、3个月、4个月、5个月、6个月、7个月、8个月、9个月、10个月、11个月、12个月、14个月、16个月、18个月、20个月、22个月或24个月的一段时间后具有至少90%的制剂强度。在一些变通方案中,本文所述的液体制剂在5℃经过至少约2个月、3个月、4个月、5个月、6个月、7个月、8个月、9个月、10个月、11个月、12个月、14个月、16个月、18个月、20个月、22个月或24个月的一段时间后具有至少95%的制剂强度。
在一些变通方案中,本文所述的液体制剂在-20℃经过至少约2个月、3个月、4个月、5个月、6个月、7个月、8个月、9个月、10个月、11个月、12个月、14个月、16个月、18个月、20个月、22个月或24个月的一段时间后具有至少80%的制剂强度。在一些变通方案中,本文所述的液体制剂在-20℃经过至少约2个月、3个月、4个月、5个月、6个月、7个月、8个月、9个月、10个月、11个月、12个月、14个月、16个月、18个月、20个月、22个月或24个月的一段时间后具有至少90%的制剂强度。在一些变通方案中,本文所述的液体制剂在-20℃经过至少约2个月、3个月、4个月、5个月、6个月、7个月、8个月、9个月、10个月、11个月、12个月、14个月、16个月、18个月、20个月、22个月或24个月的一段时间后具有至少95%的制剂强度。
治疗物质
通常来讲,对空气中的一种或多种成分、热或光敏感的任何化合物可以用于本文所述的稳定制剂。除非上下文中另外说明,否则任何治疗物质可以用于本文所述任何一种或多种制剂、药物制剂、单位剂量形式、药盒、制备方法和使用方法。在一些变通方案中,治疗物质对氧气、热或光中的一种或多种是敏感的。
在一些变通方案中,本文所述的稳定制剂包含治疗物质,该治疗物质用于治疗、预防、抑制本文所述疾病和病症、延迟其发作或致使其消退。下面参考文献,将其各自以全部内容引入文中作为参考,显示了一种或多种制剂,包括但不限于雷帕霉素制剂,可以通过本文所述的方法使所述制剂稳定,且所述文献描述了各种剂量的雷帕霉素和其它治疗物质用于治疗各种疾病或病症的用途:2005年2月9日提交的US 60/651,790,题目为“用于眼睛治疗的制剂(FORMULATIONS FOR OCULAR TREATMENT)”;2005年2月9日提交的US 60/664,040,题目为“用于疾病或病症治疗的液体制剂(LIQUID FORMULATIONS FOR TREATMENT OF DISEASESOR CONDITIONS)”;2005年3月21日提交的US 60/664,119,题目为“用于治疗疾病或病症的药物递送系统(DRUG DELIVERY SYSTEMS FORTREATMENT OF DISEASES OR CONDITIONS)”;2005年3月21日提交的US 60/664,306,题目为“用于治疗疾病或病症的原位胶化制剂和液体制剂(IN SITU GELLING FORMULATIONS AND LIQUIDFORMULATIONS FOR TREATMENT OF DISEASES ORCONDITIONS)”;2006年2月9日提交的US 11/351,844,题目为“用于眼睛治疗的制剂”;2006年2月9日提交的US 11/351,761,题目为“用于疾病或病症治疗的液体制剂”;2006年3月21日提交的US 11/386,290,题目为“用于治疗疾病或病症的药物递送系统”;2006年2月9日提交的US 11/352,092,题目为“雷帕霉素制剂和它们的使用方法(RAPAMYCINFORMULATIONS AND METHODS OF THEIR USE)”;2006年2月9日提交的US 60/772,018,题目为“稳定制剂以及它们的制备和使用方法(STABLE FORMULATIONS,AND METHODS OF THEIRPREPARATION AND USE)”;US 2005/0187241和US 2005/0064010。
可以使用的治疗物质包括通过结合细胞蛋白质的抑免蛋白家族的成员而起作用的化合物。这些化合物称作“抑免蛋白结合化合物”。抑免蛋白结合化合物包括但不限于“莫司(limus)”类化合物。可以使用的莫司类化合物的示例包括但不限于亲环蛋白和FK506-结合蛋白(FKBPs),包括西罗莫司(雷帕霉素)和它的水溶性类似物SDZ-RAD(诺华(Novartis))、TAFA-93(埃索泰尼卡(Isotechnika))、他克莫司、依维莫司、RAD-001(诺华)、吡美莫司、坦罗莫司(temsirolimus)、CCI-779(惠氏(Wyeth))、AP23841(爱瑞德(Ariad))、AP23573(爱瑞德)和ABT-578(雅培(Abbott Laboratories))。可以被使用的莫司化合物类似物和衍生物包括但不限于描述在美国专利5,527,907、6,376,517和6,329,386以及美国专利申请号09/950,307中的化合物,将其各自以全部内容引入文中作为参考。治疗物质还包括莫司化合物的类似物、前药、衍生物、盐或酯。
术语雷帕霉素和西罗莫司在本文中可以互换使用。
其它可以使用的雷帕霉素衍生物包括但不限于7-表-雷帕霉素、7-甲硫基-雷帕霉素、7-表-三甲氧基苯基-雷帕霉素、7-表-甲硫基-雷帕霉素、7-脱甲氧基-雷帕霉素、32-脱甲氧基-雷帕霉素、2-脱甲基-雷帕霉素、雷帕霉素的单-和双-酯衍生物、雷帕霉素的27-肟类、雷帕霉素的42-氧代类似物、二环雷帕霉素类、雷帕霉素二聚体类、雷帕霉素的甲硅烷基醚类、雷帕霉素的芳基磺酸酯类和氨基磺酸酯类、在31和42位的单酯和双酯、和30-脱甲氧基雷帕霉素以及其它描述在下列文献中的衍生物:Vezina等人“雷帕霉素(AY-22,989),新的抗真菌抗生素I.生产链霉素的分类学和活性成分的分离(Rapamycin(AY-22,989),A New Antifungal Antibiotic.I.Taxonomy Of The Producing Streptomycete And Isolation Of The ActivePrinciple)”,抗生素杂志(J.Antibiot.)(东京),28:721-726(1975);Sehgal等人,“雷帕霉素(AY-22,989),新的抗真菌抗生素II.发酵、分离和鉴定(Rapamycin(AY-22,989),A New Antifungal Antibiotic.II.Fermentation,Isolation And Characterization)”,抗生素杂志(东京),28:727-732(1975);Sehgal等人,“脱甲氧基雷帕霉素(AY-24,668),新的抗真菌抗生素(Demethoxyrapamycin(AY-24,668),A New Antifungal Antibiotic)”,抗生素杂志(东京),36,351-354(1983);和Paiva等人,“通过吸水链霉菌将乙酸酯、丙酸酯和甲硫胺酸引入到雷帕霉素中(Incorporation Of Acetate,Propionate,And Methionine Into Rapamycin By Streptomyceteshygroscopicus)”,天然产物杂志(J Nat Prod),54:167-177(1991)、WO92/05179、EP 467606、Caufield等人,“氢化的雷帕霉素衍生物(Hydrogenated Rapamycin Derivatives)”美国专利号5,023,262;Kao等人,“二环雷帕霉素(Bicyclic Rapamycins)”,美国专利号5,120,725;Kao等人,“雷帕霉素二聚体(Rapamycin Dimers)”,美国专利号5,120,727;Failli等人,“雷帕霉素的硅醚(Silyl Ethers Of Rapamycin)”,美国专利号5,120,842;Failli等人,“雷帕霉素42-磺酸酯和42-(N-烷氧羰基)氨基磺酸酯用作免疫抑制剂(Rapamycin 42-Sulfonates And42-(N-carboalkoxy)Sulfamates Useful As Immunosuppressive Agents)”,美国专利号5,177,203;Nicolaou等人,“雷帕霉素的全合成(Total SynthesisOf Rapamycin)”,美国化学会杂志(J.Am.Chem.Soc.),115:4419-4420(1993);Romo等人,“采用Evans-Tishchenko片断耦联的雷帕霉素的全合成(Total Synthesis Of(-)Rapamycin Using An Evans-TishchenkoFragment Coupling)”,美国化学会杂志,115:7906-7907(1993);和Hayward等人,“经新颖的钛-介导的醛醇大环形成反应全合成雷帕霉素(Total Synthesis Of Rapamycin Via A Novel Titanium-Mediated AldolMacrocyclization Reaction)”,美国化学会杂志,115:9345-9346(1993);将其各自以全部内容引入文中作为参考。
莫司类化合物可以在如下制剂、液体制剂和方法中应用,所述制剂、液体制剂和方法用于治疗、预防、抑制血管生成介导的眼睛疾病和病症(包含脉络膜新生血管形成)、延迟其发作或致使其消退。莫司类化合物可以用于预防、治疗、抑制AMD、延迟其发作或致使其消退,所述AMD包括湿性AMD。雷帕霉素可以用于治疗、预防、抑制血管生成介导的眼睛疾病和病症(包含脉络膜新生血管形成),延迟其发作或致使其消退。雷帕霉素和它的衍生物和类似物可以用于预防、治疗、抑制AMD、延迟其发作或致使其消退,所述AMD包括湿性AMD。在一些变通方案中,莫司类化合物的成员或雷帕霉素可以用于治疗湿性AMD或血管生成介导的眼睛疾病和病症,包括脉络膜新生血管形成。
其它可以被使用的治疗物质包括公开在以下专利和出版物中的那些,将其各自以全部内容引入文中作为参考:2004年4月1日公开的PCT公开文本WO 2004/027027,题目为“抑制脉络膜新生血管形成的方法(Methodof inhibiting choroidal neovascularization)”,转让给宾西法尼亚大学的托管人;1995年2月7日授权的US专利号5,387,589,题目为“治疗眼睛炎症的方法(Method of Treating Ocular Inflammation)”,发明人为PrassadKulkarni,转让给路易斯维尔大学研究基金会(University of LouisvilleResearch Foundation);2003年4月23日授权的US专利号6,376,517,题目为“用于视觉和记忆障碍的2-哌啶酸衍生物(Pipecolic acid derivativesfor vision and memory disorders)”,转让给GPI NIL控股有限公司(GPINIL Holdings,Inc);2004年4月8日公开的PCT公开文本WO2004/028477,题目为“:包含甾体类的治疗物质的视网膜下给药方法:使药效学作用定位于脉络膜和视网膜的方法;以及治疗和/或预防视网膜疾病的相关方法(Method subretinal administration of therapeutics includingsteroids:method for localizing pharmadynamic action at the choroid andretina;and related methods for treatment and or prevention of retinaldiseases)”,转让给伊诺克斯公司(Innorx,Inc);2002年7月9日授权的美国专利号6,416,777,题目为“眼科药物递送装置(Ophthalmic drug deliverydevice)”,转让给爱尔康全球有限公司(Alcon Universal Ltd);2004年3月30日授权的美国专利号6,713,081,题目为“眼科治疗物质递送装置及制造和使用这些装置的方法(Ocular therapeutic agent delivery device andmethods for making and using such devices)”,转让给卫生和健康服务部(Department of Health and Human Services);1992年3月31日授权的美国专利号5,100,899,题目为“使用雷帕霉素及它的衍生物和前药抑制哺乳动物移植排斥的方法(Methods of inhibiting transplant rejection inmammals using rapamycin and derivatives and prodrugs thereof)”。
可以使用的其它治疗物质包括吡咯烷二硫代氨基甲酸酯(NFκB抑制剂);角鲨胺;TPN 470类似物和夫马洁林;PKC(蛋白激酶C)抑制剂;Tie-1和Tie-2激酶抑制剂;VEGF受体激酶抑制剂;蛋白体抑制剂例如VelcadeTM(硼替佐米,注射用);雷珠单抗(ranibuzurnab,LucentisTM)和指向同样靶点的其它抗体;培加他尼(pegaptanib、MacugenTM);玻连蛋白受体拮抗剂,例如玻连蛋白受体型整联蛋白的环肽拮抗剂;α-v/β-3整联蛋白拮抗剂;α-v/β-1整联蛋白拮抗剂;噻唑烷二酮类例如罗格列酮或曲格列酮;干扰素,包括γ-干扰素或通过利用右旋糖苷和金属配位作用而靶向CNV的干扰素;色素上皮源性因子(PEDF);内皮抑制素;血管抑素;肿瘤抑素(tumistatin);人血管能抑素(canstatin);乙酸阿奈可他;丙酮化合物(acetonide);曲安西龙;四硫钼酸盐;血管生成因子的RNA沉默或RNA干扰(RNAi),包括靶向VEGF表达的核酶;AccutaneTM(13-顺维生素A酸);ACE抑制剂,包括但不限于喹那普利(quinopril)、卡托普利和培哚普利(perindozril);mTOR(雷帕霉素的哺乳动物靶点)抑制剂;3-氨基沙利度胺;己酮可可碱;2-甲氧基雌二醇;秋水仙碱;AMG-1470;环氧合酶抑制剂,例如奈帕芬胺、罗非昔布、双氯芬酸、罗非昔布、NS398、塞来昔布、万络和(E)-2-烷基-2-(4-甲磺酰苯基)-1-苯乙烯;t-RNA合成酶调节剂;金属蛋白酶13抑制剂;乙酰胆碱酯酶抑制剂;钾通道阻滞剂;endorepellin;6-硫鸟嘌呤的嘌呤类似物;环状过氧化物ANO-2;(重组)精氨酸脱亚氨基酶;表没食子儿茶素-3-没食子酸酯;西立伐他汀;舒拉明类似物;VEGF捕获(trap)分子;凋亡抑制剂;维速达尔(VisudyneTM)、snET2和用于光动力学疗法(PDT)的其它光敏剂;肝细胞生长因子抑制剂(生长因子或其受体的抗体、c-met酪氨酸激酶的小分子抑制剂、HGF的截断片段(truncated versions),例如NK4)。
其它可以使用的治疗物质包括抗炎剂,包括但不限于非甾体抗炎剂和甾体抗炎剂。在一些变通方案中,可以在液体制剂中使用的活性物质是ACE-抑制剂、内源性细胞因子、影响基底膜的物质、影响内皮细胞生长的物质、肾上腺素能激动剂或阻断剂、胆碱能激动剂或阻断剂、醛糖还原酶抑制剂、镇痛剂、麻醉剂、抗过敏剂、抗菌剂、抗高血压药物、升压剂、抗原虫剂、抗病毒剂、抗真菌剂、抗感染剂、抗癌剂、抗代谢药和抗血管生成剂。
可以使用的甾体治疗物质包括但不限于21-乙酰氧基孕烯醇酮、阿氯米松、阿尔孕酮、安西奈德、倍氯米松、倍他米松、布地奈德、氯泼尼松、氯倍他索、氯倍他松、氯可托龙、氯泼尼醇、皮质酮、可的松、可的伐唑、地夫可特、地奈德、去羟米松、地塞米松、二氟拉松、二氟可龙、二氟泼尼酯、甘草次酸、氟扎可特、氟氯奈德、氟米松、氟尼缩松、氟轻松、醋酸氟轻松、氟可丁酯、氟可龙、氟米龙、醋酸氟培龙、醋酸氟泼尼定、氟泼尼龙、氟氢缩松、丙酸氟替卡松、福莫可他、氯氟舒松、丙酸卤倍他索、卤米松、醋酸卤泼尼松、氢可他酯、氢化可的松、氯替泼诺依碳酸酯、马泼尼酮、甲羟松、甲泼尼松、甲泼尼龙、康酸莫米松、帕拉米松、泼尼卡酯、泼尼松龙、泼尼松龙25-二乙氨基-乙酸酯、泼尼松龙磷酸钠、泼尼松、强的松龙戊酸酯(prednival)、泼尼立定、利美索龙、替可的松、曲安西龙、曲安奈德、苯曲安奈德、己曲安奈德和任何它们的衍生物。
在一些变通方案中,可以使用可的松、地塞米松、氟轻松、氢化可的松、甲泼尼龙、泼尼松龙、泼尼松和曲安西龙或他们的衍生物。液体制剂可以包含两种或多种甾体治疗物质的组合。
在非限制性示例中,甾体治疗物质可以占液体制剂重量的约0.05%至约50%。在另一个非限制性示例中,甾体占液体制剂重量的约0.05%至约10%、约10%至约20%、约30%至约40%或约40%至约50%。
可以使用的治疗物质的其它非限制性示例包括但不限于麻醉剂、镇痛剂、细胞运输/流动性阻抑剂(impending agents)例如秋水仙碱、长春新碱、细胞松弛素B和相关化合物;碳酸酐酶抑制剂例如乙酰唑胺、醋甲唑胺、双氯非那胺、丹木斯和神经保护剂例如尼莫地平及相关化合物;抗生素例如四环素、金霉素、杆菌肽、新霉素、多粘菌素、短杆菌肽、头孢氨苄、土霉素、氯霉素、利福平、环丙沙星、氨基糖苷类(aminosides)、庆大霉素、红霉素和青霉素、喹诺酮、头孢他啶、万古霉素、亚胺培南(imipeneme);抗真菌剂例如两性霉素B、氟康唑、酮康唑和咪康唑;抗菌剂例如磺胺类、磺胺嘧啶、磺胺醋酰、磺胺甲二唑和磺胺异噁唑、呋喃西林和丙酸钠;抗病毒剂如碘苷、三氟胸苷、三氟尿苷(trifluorouridine)、阿昔洛韦、更昔洛韦、西多福韦、干扰素、DDI、AZT、膦甲酸、阿糖腺苷、利巴韦林(irbavirin);蛋白酶抑制剂和抗巨细胞病毒剂;抗过敏剂如色甘酸钠、安他唑啉、美沙吡林(methapyriline)、氯苯那敏、西替利嗪、美吡拉敏和非尼拉敏;合成糖皮质激素和盐皮质激素和更多的衍生自胆固醇新陈代谢的普通激素形式(DHEA、孕酮、雌激素);非甾体类抗炎剂例如水杨酸酯、吲哚美辛、布洛芬、双氯芬酸、氟比洛芬、吡罗昔康和COX2抑制剂;抗肿瘤药例如卡莫司汀、顺铂、氟尿嘧啶、多柔比星、门冬酰胺酶、阿扎胞苷、硫唑嘌呤、博来霉素、白消安、卡铂、卡莫司汀、苯丁酸氮芥、环磷酰胺、环孢霉素、阿糖胞苷、达卡巴嗪、放线菌素D、柔红霉素、多柔比星、雌莫司汀、依托泊苷、阿维A酯、非格司亭(filgrastin)、氟尿苷、氟达拉滨、氟尿嘧啶、氟甲睾酮、氟他胺、戈舍瑞林、羟基脲、异环磷酰胺、亮丙瑞林、左旋咪唑、limustine、氮芥、美法仑、巯嘌呤、甲氨蝶呤、丝裂霉素、米托坦、喷司他丁、哌泊溴烷、普卡霉素、丙卡巴肼、沙格莫丁(sargramostin)、链佐星、他莫昔芬、紫杉醇、替尼泊苷、硫鸟嘌呤、尿嘧啶氮芥、长春碱、长春新碱和长春地辛;免疫学药物例如疫苗和免疫刺激物;胰岛素、降钙素、甲状旁腺素和肽、及下丘脑加压素释放因子;β-肾上腺素能阻断剂例如噻吗洛尔、左布诺洛尔和倍他洛尔;细胞因子、白介素和生长因子表皮生长因子、纤维母细胞生长因子、血小板衍生生长因子、转化生长因子β、睫状神经营养生长因子、胶质细胞衍生的神经营养因子、NGF、EPO、PLGF、脑神经生长因子(BNGF)、血管内皮生长因子(VEGF)和抗所述生长因子的单克隆抗体或其片段;抗炎剂,例如氢化可的松、地塞米松、氟轻松、泼尼松、泼尼松龙、甲泼尼龙、氟米龙、倍他米松和曲安西龙;解充血剂例如去氧肾上腺素、萘甲唑林和四氢唑啉(tetrahydrazoline);缩瞳剂和抗胆碱酯酶剂,例如毛果芸香碱、卡巴胆碱、氟磷酸二异丙酯、碘依可酯和地美溴铵;散瞳剂例如硫酸阿托品、环喷托酯、后马托品、东莨菪碱、托吡卡胺、尤卡托品;拟交感神经药物例如肾上腺素、血管收缩剂和血管舒张剂;抗凝剂例如肝素、抗纤维蛋白原、纤溶酶、抗凝激活酶;抗糖尿病剂,包括醋酸己脲、氯磺丙脲、格列吡嗪、格列本脲、妥拉磺脲、甲苯磺丁脲、胰岛素和醛糖还原酶抑制剂、激素类、肽类、核酸类、糖类、脂质类、糖脂类、糖蛋白类和其它大分子类,包括内分泌激素例如垂体、胰岛素、胰岛素相关的生长因子、甲状腺、生长激素类、热休克蛋白;免疫应答调节剂,例如胞壁酰二肽、环孢菌素、干扰素(包括α-、β-和γ-干扰素)、白介素-2、细胞因子、FK506(环氧-吡啶并-氧杂氮杂环二十三碳烯-四酮,也称为他克莫司)、肿瘤坏死因子、喷司他丁、胸腺喷丁、转化因子β-2、促血红细胞生长素、抗新生(antineogenesis)蛋白(例如抗VEGF、干扰素)、抗体(单克隆的、多克隆的、人化的等)或抗体片段、寡适配体、适配体(aptamer)和基因片段(寡核苷酸、质粒、核酶、小干扰RNA(SiRNA)、核酸片断、肽类);免疫调节剂例如安道生、沙利度胺、他莫昔芬;抗血栓药和血管舒张药例如rtPA、尿激酶、纤维蛋白溶酶、一氧化氮供体、核酸、地塞米松、环孢菌素A、硫唑嘌呤、布喹那、胍立莫司、6-巯基嘌呤、咪唑立宾、雷帕霉素、他克莫司(FK-506)、叶酸类似物(例如氨基二甲叶酸、依达曲沙、甲氨蝶呤、吡曲克辛、蝶罗呤、拓忧得三甲曲沙)、嘌呤类似物(例如克拉屈滨、氟达拉滨、6-巯基嘌呤、硫咪嘌呤(thiamiprine)、硫鸟嘌呤(thiaguanine)、嘧啶类似物(例如安西他滨、阿扎胞苷、6-氮杂尿苷、卡莫氟、阿糖胞苷、去氧氟尿苷、乙嘧替氟、依诺他滨、氟尿苷、氟尿嘧啶、吉西他滨、替加氟)、氟轻松、曲安西龙(triaminolone)、醋酸阿奈可他、氟米龙、甲羟松和泼尼松(prednislone)。在一些变通方案中,免疫抑制剂是地塞米松。在其它变通方案中,免疫抑制剂是环孢菌素A。
在其它变通方案中,制剂包含一种或多种治疗物质的组合。
可以在本文所述的制剂中使用的治疗物质的其它非限制性示例包括抗细菌抗生素:氨基糖苷类(例如阿米卡星、安普霉素、阿贝卡星、班贝霉素类、布替罗星、地贝卡星、双氢链霉素、福帖霉素类、庆大霉素、异帕米星、卡那霉素、小诺霉素、新霉素、十一碳烯酸新霉素、奈替米星、巴龙霉素、核糖霉素、西索米星、大观霉素、链霉素、妥布霉素、丙大观霉素)、氯霉素类(例如叠氮氯霉素、氯霉素、氟苯尼考、甲砜霉素)、安莎霉素类(例如利福米特、利福平、利福霉素SV、利福喷汀、利福昔明)、P-内酰胺类(例如碳头孢烯类(例如氯碳头孢)、碳青霉烯类(例如比阿培南、亚胺培南、美罗培南、帕尼培南)、先锋霉素类(例如头孢克洛、头孢羟氨苄、头孢孟多、头孢曲秦、头孢西酮、头孢唑林、头孢卡品匹酯、头孢克定、头孢地尼、头孢托仑、头孢吡肟、头孢他美、头孢克肟、头孢甲肟(cefinenoxime)、头孢地秦、头孢尼西、头孢哌酮、头孢雷特、头孢噻肟、头孢替安、头孢唑兰、头孢咪唑、头孢匹胺、头孢匹罗、头孢泊肟酯、头孢丙烯、头孢沙定、头孢磺啶、头孢他啶、头孢特仑、头孢替唑、头孢布烯、头孢唑肟、头孢曲松、头孢呋辛、头孢唑南、头孢赛曲钠、头孢氨苄、头孢来星、头孢噻啶、头孢菌素、头孢噻吩、头孢匹林钠、头孢拉定、特头孢氨苄(pivcefalexin))、头霉素类(例如头孢拉宗、头孢美唑(cefinetazole)、头孢米诺、头孢替坦、头孢西丁)、单环内酰胺类(例如氨曲南、卡芦莫南、替吉莫南)、氧头孢烯类(氟氧头孢、拉氧头孢)、青霉素类(例如氮脒青霉素、氮脒青霉素匹酯、阿莫西林、氨苄西林、阿帕西林、阿扑西林、阿度西林、阿洛西林、巴氨西林、苄基青霉酸、青霉素钠、羧苄西林、卡茚西林、氯甲西林、氯唑西林、环青霉素、双氯西林、依匹西林、芬贝西林、氟氯西林、海他西林、仑氨西林、美坦西林、甲氧西林钠、美洛西林、奈夫西林钠、苯唑西林、培那西林、氢碘酸喷沙西林、苯明青霉素、苄星青霉素、青霉素G二苯甲胺(penicillin g benzhydrylamine)、青霉素G钙、海巴明青霉素G、青霉素G钾、普鲁卡因青霉素G、青霉素N、青霉素O、苯青霉素V、苄星青霉素V、海巴明青霉素V、青哌环素、非奈西林钾、哌拉西林、匹氨西林、丙匹西林、喹那西林、磺苄西林、舒他西林、酞氨西林、替莫西林、替卡西林)、其它(例如利替培南)、林可酰胺类(例如克林霉素、林可霉素)、大环内酯类(例如阿奇毒素、卡波霉素、克拉霉素、地红霉素、红霉素、醋硬脂红霉素、依托红霉素、葡庚糖酸红霉素、乳糖酸红霉素、丙酸红霉素、硬脂酸红霉素、交沙霉素、白霉素类、麦迪霉素类、美欧卡霉素、竹桃霉素、普利霉素、罗他霉素、罗沙米星、罗红霉素、螺旋霉素、醋竹桃霉素)、多肽类(例如安福霉素、杆菌肽、卷曲霉素、多粘霉素E(colistin)、持久杀菌素(enduracidin)、恩维霉素、夫沙芬净、短杆菌肽类、短杆菌肽、米卡霉素、多粘菌素、普那霉素、利托菌素、替考拉宁、硫链丝菌肽、结核放线菌素、短杆菌酪肽、短杆菌素、万古霉素、紫霉素、维吉霉素、短杆菌锌)、四环素类(例如阿哌环素、金霉素、氯莫环素、地美环素、多西环素、胍甲环素、赖甲环素、甲氯环素、美他环素、米诺环素、土霉素、青哌环素、匹哌环素、罗利环素、山环素、四环素)和其它(例如环丝氨酸、莫匹罗星、抗结核菌素);合成的抗菌素:2,4-二胺基嘧啶类(例如溴莫普林、四氧普林、甲氧苄啶)、硝基呋喃类(例如呋喃他酮、呋唑氯铵、硝呋拉定、硝呋太尔、硝呋复林、硝呋吡醇、硝呋拉嗪、硝呋妥因醇、呋喃妥因)、喹诺酮类和类似物(例如西诺沙星、环丙沙星、克林沙星、二氟沙星、依诺沙星、氟罗沙星、氟甲喹、格帕沙星、洛美沙星、米洛沙星、那氟沙星、萘啶酸、诺氟沙星、氧氟沙星、奥索利酸、帕珠沙星、培氟沙星、吡哌酸、吡咯米酸、罗索沙星、芦氟沙星、司帕沙星、替马沙星、托氟沙星、曲伐沙星)、磺酰胺类(例如醋磺胺甲氧嗪、苄磺胺、氯胺-b、氯胺-t、双氯胺-t、N2-甲磺酰胺异二甲嘧啶(n2-formylsulfisomidine)、n4-β-d-葡萄糖基磺胺、磺胺米隆、4′-(甲基氨磺酰基)磺胺(sulfanilanilide)、诺丙磺胺、酞磺醋胺、酞磺胺噻唑、柳氮磺嘧啶、琥珀磺胺噻唑、磺胺苯酰、磺胺醋酰、磺胺氯达嗪、磺胺柯定、磺胺西汀、磺胺嘧啶、磺胺戊烯、磺胺地索辛、磺胺多辛、磺胺乙二唑、磺胺脒、磺胺二甲噁唑脒(sulfaguanol)、磺胺林、磺胺洛西酸、磺胺甲嘧啶、磺胺对甲氧嘧啶、磺胺二甲嘧啶、磺胺甲二唑、磺胺托嘧啶、磺胺甲噁唑、磺胺甲氧嗪、磺胺美曲、磺胺米可定、磺胺噁唑、磺胺、磺胺水杨酸、n4-磺胺酰磺胺、磺胺酰脲、n-磺胺酰-3,4-二甲苯甲酰胺、磺胺硝苯、磺胺培林、磺胺苯吡唑、磺胺普罗林、磺胺吡嗪、磺胺吡啶、磺胺异噻唑、磺胺均三嗪、磺胺噻唑、磺胺硫脲、磺胺托拉米、磺胺索嘧啶、磺胺异噁唑)、砜类(例如醋氨苯砜、醋地砜、磺胺苯砜钠、氨苯砜、地百里砜、葡氨苯砜钠、苯丙砜、琥珀氨苯砜、磺胺酸、对磺胺酰基苄胺、阿地砜钠、噻唑砜)、和其它(例如氯福克酚、海克西定、乌洛托品、脱水亚甲柠檬酸乌洛托品、马尿酸乌洛托品、扁桃酸乌洛托品、磺基水杨酸乌洛托品、硝羟喹啉、牛磺罗定、希波酚(xibomol));抗真菌抗生素:多烯类(例如两性霉素B、克念菌素、制皮菌素、非律平、制霉色基素、曲古霉素、哈霉素、鲁斯霉素、美帕曲星、那他霉素、制霉菌素、培西洛星、表霉素)、其它(例如偶氮丝氨酸、灰黄霉素、寡霉素类、十一烯酸新霉素、吡咯尼群、西卡宁、杀结核菌素、绿胶霉素),合成的抗真菌剂类:烯丙胺类(例如布替奈芬、萘替芬、特比萘芬)、咪唑类(例如联苯苄唑、布康唑、氯登妥因、氯米达唑、氯康唑、克霉唑、益康唑、恩康唑、芬替康唑、氟曲马唑、异康唑、酮康唑、拉诺康唑、咪康唑、奥莫康唑、硝酸奥昔康唑、舍他康唑、硫康唑、噻康唑)、硫代氨基甲酸酯类(例如托西拉酯、托林达酯、托萘酯)、三唑类(例如氟康唑、伊曲康唑、沙康唑、特康唑)、其它(例如吖啶琐辛、阿莫罗芬、珍尼柳酯、溴柳氯苯胺、丁氯柳胺、丙酸钙、氯苯甘醚、环吡酮、氯羟喹、科帕腊芬内特(coparaffinate)、地马唑二盐酸盐、依沙酰胺(exalarnide)、氟胞嘧啶、哈利他唑、海克替啶、氯氟卡班、硝呋太尔、碘化钾、丙酸、吡硫翁、水杨苯胺、丙酸钠、舒苯汀、替诺尼唑、三醋汀、苄硫噻二嗪乙酸(ujothion)、十一烯酸、丙酸锌);抗肿瘤药、抗生素和类似物(例如阿克拉霉素类、放线菌素f1、安曲霉素、偶氮丝氨酸、博来霉素类、放线菌素C、卡柔比星、嗜癌素、色霉素类、放线菌素D、柔红霉素、6-重氮基-5-氧代-L-正亮氨酸、多柔比星、表柔比星、伊达比星、美诺立尔、丝裂霉素、麦考酚酸、诺拉霉素、橄榄霉素类、培洛霉素、吡柔比星、普卡霉素、泊非霉素、嘌呤霉素、链黑霉素、链佐星、杀结核菌素、净司他丁、佐柔比星)、抗代谢药(例如叶酸类似物(例如二甲叶酸、依达曲沙、甲氨蝶呤、吡曲克辛、蝶罗呤、拓忧得、三甲曲沙)、嘌呤类似物(例如克拉屈滨、氟达拉滨、6-巯基嘌呤、硫咪嘌呤、硫鸟嘌呤)、嘧啶类似物(例如安西他滨、阿扎胞苷、6-氮杂尿苷、卡莫氟、阿糖胞苷、去氧氟尿苷、乙嘧替氟、依诺他滨、氟尿苷、氟尿嘧啶、吉西他滨、替加氟(tagafur)),抗炎剂:甾体抗炎剂:乙酸基孕烯醇酮、阿氯米松、阿尔孕酮、安西奈德、氯地米松、倍他米松、布地奈德、氯泼尼松、氯倍他索、氯倍他松、氯可托龙、氯泼尼醇、皮质酮、可的松、可的伐唑、地夫可特、地奈德、去羟米松、地塞米松、二氟拉松、二氟可龙、二氟泼尼酯、甘草次酸、氟扎可特、氟氯奈德、氟米松、氟尼缩松、氟轻松、醋酸氟轻松、氟可丁酯、氟可龙、氟米龙、醋酸氟培龙、醋酸氟泼尼定、氟泼尼龙、氟轻缩松、丙酸氟替卡松、福莫可他、氯氟舒松、丙酸卤倍他索、卤米松、醋酸卤泼尼松、氢可他酯、氢化可的松、氯替泼诺依碳酸酯、马泼尼酮、甲羟松、甲泼尼松、甲泼尼龙、康酸莫米松、帕拉米松、泼尼卡酯、泼尼松龙、泼尼松龙25-二乙氨基-乙酸酯、泼尼松龙磷酸钠、泼尼松、强的松龙戊酸酯、泼尼立定、利美索龙、替可的松、曲安西龙、曲安奈德、苯曲安奈德和己曲安奈德;非甾体抗炎剂:氨基芳基羧酸衍生物(例如苯乙氨茴酸、依托芬那酯、氟芬那酸、异尼辛、甲氯芬那酸、甲芬那酸、尼氟酸、他尼氟酯、特罗芬那酯、托芬那酸)、芳基乙酸衍生物(例如醋氯芬酸、阿西美辛、阿氯芬酸、氨芬酸、呱氨托美丁、溴芬酸、丁苯羟酸、桂美辛、氯吡酸、双氯芬酸钠、依托度酸、联苯乙酸、芬克洛酸、芬替酸、葡美辛(giucametacin)、异丁芬酸、吲哚美辛、三苯唑酸、伊索克酸、氯那唑酸、甲嗪酸、莫苯唑酸、奥沙美辛、吡拉唑酸、丙谷美辛、舒林酸、噻拉米特、托美丁、托哌辛(tropesin)、佐美酸)、芳基丁酸衍生物(例如布马地宗(bumadizon)、布替布芬、芬布芬、联苯丁酸)、芳基甲酸类(例如环氯茚酸、酮咯酸、替诺立定)、芳基丙酸衍生物(例如阿明洛芬、苯噁洛芬、柏莫洛芬、布氯酸、卡洛芬、非诺洛芬、氟诺洛芬、氟比洛芬、布洛芬、异丁普生、吲哚洛芬、酮洛芬、洛索洛芬、萘普生、奥沙普秦、吡酮洛芬、吡洛芬、普拉洛芬、丙替嗪酸、舒洛芬、噻洛芬酸、希莫洛芬、扎托洛芬)、吡唑类(例如二苯米唑、依匹唑)、吡唑啉酮类(例如阿扎丙宗、苄哌立隆、非普拉宗、莫非布宗、吗拉宗、羟布宗、保泰松、哌布宗、异丙安替比林、雷米那酮、琥布宗、噻唑啉并保泰松(thiazolinobutazone))、水杨酸衍生物(例如醋氨沙洛、阿司匹林、贝诺酯、溴水杨醇、阿司匹林钙、二氟尼柳、依特柳酯、芬度柳、龙胆酸、水杨酸乙二醇酯、水杨酸咪唑、赖氨酸乙酰水杨酸、美沙拉秦、水杨吗啉、水杨酸1-萘酯、奥沙拉秦、帕沙米特、乙酰水杨酸苯酯、水杨酸苯酯、醋水杨胺、水杨酰胺-O-乙酸、水杨酰硫酸酯、双水杨酯、柳氮磺吡啶)、噻嗪甲酰胺类(例如安吡昔康、屈噁昔康、伊索昔康、氯诺昔康(lomoxicam)、吡罗昔康、替诺昔康)、ε-乙酰胺基己酸、s-腺苷甲硫胺酸、3-氨基-4-羟基丁酸、阿米西群、苄达酸、苄达明、a-红没药醇、布可隆、联苯吡胺、地他唑、依莫法宗、非普地醇、愈创蓝油烃、萘丁美酮、尼美舒利、奥沙西罗、瑞尼托林、派立索唑、普罗喹宗、超氧化物歧化酶、替尼达普和齐留通。
治疗物质还可以与其它治疗物质和治疗联合使用,所述其它治疗物质和治疗包括但不限于用于治疗、预防、抑制血管生成或新血管生成(特别是CNV)、延迟其发作或致使其消退的物质或治疗。在一些变通方案中,另外的物质或治疗用于治疗并使血管生成或新血管生成(特别是CNV)消退。所述另外的物质或治疗的非限制性示例包括吡咯烷二硫代氨基甲酸酯(NFκB抑制剂);角鲨胺;TPN 470类似物和夫马洁林;PKC(蛋白激酶C)抑制剂;Tie-1和Tie-2激酶抑制剂;VEGF受体激酶抑制剂;蛋白体抑制剂例如VelcadeTM(硼替佐米,注射用);雷珠单抗(LucentisTM)和指向同样靶点的其它抗体;培加他尼(MacugenTM);玻连蛋白受体拮抗剂,例如玻连蛋白受体型整联蛋白的环肽拮抗剂;α-v/β-3整联蛋白拮抗剂;α-v/β-1整联蛋白拮抗剂;噻唑烷二酮类例如罗格列酮或曲格列酮;干扰素,包括γ-干扰素或通过利用右旋糖苷和金属配位作用而靶向CNV的干扰素;色素上皮源性因子(PEDF);内皮抑制素;血管抑素;肿瘤抑素;人血管能抑素;乙酸阿奈可他;丙酮化合物;曲安西龙;四硫钼酸盐;血管生成因子的RNA沉默或RNA干扰(RNAi),包括靶向VEGF表达的核酶;AccutaneTM(13-顺维生素A酸);ACE抑制剂,包括但不限于喹那普利、卡托普利和培哚普利;mTOR(雷帕霉素的哺乳动物靶点)抑制剂;3-氨基沙利度胺;己酮可可碱;2-甲氧基雌二醇;秋水仙碱;AMG-1470;环氧合酶抑制剂,例如奈帕芬胺、罗非昔布、双氯芬酸、罗非昔布、NS398、塞来昔布、万络和(E)-2-烷基-2-(4-甲磺酰苯基)-1-苯乙烯;t-RNA合成酶调节剂;金属蛋白酶13抑制剂;乙酰胆碱酯酶抑制剂;钾通道阻滞剂;endorepellin;6-硫鸟嘌呤的嘌呤类似物;环状过氧化物ANO-2;(重组)精氨酸脱亚氨基酶;表没食子儿茶素-3-没食子酸酯;西立伐他汀;舒拉明类似物;VEGF捕获分子;肝细胞生长因子抑制剂(生长因子或其受体的抗体、c-met酪氨酸激酶的小分子抑制剂、HGF的截断片段,例如NK4);凋亡抑制剂;维速达尔(VisudyneTM)、snET2和用于光动力学疗法(PDT)的其它光敏剂;和激光凝固术。
制剂
除非上下文中另外清楚地说明,否则意味着本文所述的任何一种或多种治疗物质可以用于本文所述的稳定制剂。除非上下文中另外清楚地说明,否则意味着本文所述的任何一种或多种稳定制剂可以用于治疗、预防、抑制本文所述的任何一种或多种疾病或病症或者延迟其发作。除非上下文中另外清楚地说明,否则意味着本文所述的稳定制剂可以(但不必须是)用本文所述的任何一种或多种方法制成。
本文所述的制剂包含治疗物质,且通常是任何液体制剂,包括但不限于溶液剂、混悬剂和乳剂。在一些变通方案中,液体制剂是原位胶化制剂。在一些变通方案中,置于水介质中后,所述液体制剂形成相对于周围介质的非分散的块(mass)。在一些变通方案中,本文所述的稳定制剂包括描述在下列待审的专利申请中的、但是通过本文所述的方法制备的制剂:2005年2月9日提交的US 60/651,790,题目为“用于眼睛治疗的制剂”;2005年2月9日提交的US 60/664,040,题目为“用于疾病或病症治疗的液体制剂”;2005年3月21日提交的US 60/664,119,题目为“用于治疗疾病或病症的药物递送系统”;2005年3月21日提交的US 60/664,306,题目为“用于治疗疾病或病症的原位胶化制剂和液体制剂”;2006年2月9日提交的US 11/351,844,题目为“用于眼睛治疗的制剂”;2006年2月9日提交的US 11/351,761,题目为“用于疾病或病症治疗的液体制剂”;2006年3月21日提交的US 11/386,290,题目为“用于治疗疾病或病症的药物递送系统”;2006年2月9日提交的US 11/352,092,题目为“雷帕霉素制剂和它们的使用方法”;2006年2月9日提交的US 60/772,018,题目为“稳定制剂以及它们的制备和使用方法”;US 2005/0187241和US2005/0064010;将其各自以全部内容引入文中作为参考。
在一些变通方案中,液体制剂中的治疗物质占制剂总重量的约0.01%至约30%、约0.05%至约15%、约0.1%至约10%、约1%至约5%或者约5%至约15%、约8%至约10%、约0.01%至约1%、约0.05%至约5%、约0.1%至约0.2%、约0.2%至约0.3%、约0.3%至约0.4%、约0.4%至约0.5%、约0.5%至约0.6%、约0.6%至约0.7%、约0.7%至约1%、约1%至约5%、约5%至约10%、约15%至约30%、约20%至约30%或者约25%至约30%。
制剂成分的“约”某一定量是指该所述量的90-110%。
在本文指导下,通过例如以多种量或浓度将治疗物质给药至疾病模型系统,例如体外或体内模型系统,并将模型系统的结果与各种量或浓度的雷帕霉素的结果进行比较,本领域技术人员能确定给定治疗物质的什么量或浓度相当于雷帕霉素的量或浓度。在本文指导下,通过参阅记载将雷帕霉素与其它治疗物质进行比较的实验的科学文献,本领域技术人员也能确定给定治疗物质的什么量或浓度相当于雷帕霉素的量或浓度。应当理解,例如当用不同的疾病或病症进行评估时,或者当使用不同的制剂类型时,即使同样的治疗物质可能相当于不同的雷帕霉素当量水平。关于雷帕霉素和其它治疗物质在眼科疾病方面的比较研究的非限制性示例是Ohia等人,甾体和免疫抑制药物对兔子内毒素-葡萄膜炎的作用(Effects of steroidsand immunosuppressive drugs on endotoxin-uveitis in rabbits),眼科药理学杂志(J.Ocul.Pharmacol.),8(4):295-307(1992);Kulkarni,在内毒素诱导的葡萄膜炎中的甾体和非甾体药物(Steroidal and nonsteroidal drugsin endotoxin-induced uveitis),眼科药理学杂志,10(1):329-34(1994);Hafizi等人,雷帕霉素、环孢菌素A和FK506对人冠状动脉平滑肌细胞增殖和信号发生的不同作用(Differential effects of rapamycin,cyclosporine A,andFK506 on human coronary artery smooth muscle cell proliferation andsignaling),血管药理学(Vascul Pharmacol.),41(4-5):167-76(2004);和US2005/0187241。
例如,在湿性AMD模型中,如果发现一种治疗物质在治疗湿性AMD中比雷帕霉素的效力或功效大约小10倍,则10ng/ml浓度的该治疗物质相当于1ng/ml浓度的雷帕霉素。或者如果发现一种治疗物质在治疗湿性AMD中比雷帕霉素的效力或功效大约小10倍,则相对于雷帕霉素的量,将给药10倍量的该治疗物质。
在一些变通方案中,制剂包含治疗物质和溶剂成分。溶剂成分可以占例如制剂总重量的约0.01%至约99.9%、约0.1%至约99.9%、约25%至约55%、约30%至约50%或者约35%至约45%、约0.1%至约10%、约10%至约20%、约20%至约30%、约30%至约40%、约40%至约45%、约40%至约45%、约45%至约50%、约50%至约60%、约50%至约70%、约70%至约80%、约80%至约90%或者约90%至约100%。在一些变通方案中,溶剂成分占制剂最终重量的约0.1%至约10%。
本文所述的制剂可以包含稀释成分。稀释成分可以占例如制剂总重量的约1%至约99%、约20%至约99%、约50%至约99%、约60%至约99%或者约70%至约99%、约80%至约99%、约90%至约99%,或者占制剂最终重量的约92%至约96%。在一些变通方案中,稀释成分占制剂量的大于约50%、大于约60%、大于约70%、大于约80%或者大于约90%。
制剂的一些变通方案包含占总重量约0.01%至约20%的一种或多种治疗物质例如但不限于雷帕霉素、占总重量约0.5%至约15%的溶剂以及占总重量约70%至约96%的稀释成分。在一些变通方案中,制剂还包含占总重量约0%至约40%的稳定剂、赋形剂、辅助剂或抗氧化剂。
在一些变通方案中,液体制剂可以包含占总重量约2%的治疗物质(包括但不限于雷帕霉素)、占总重量约4%的溶剂和占总重量约94%的稀释成分。
在一些变通方案中,本文所述的液体制剂具有40%至120%厘泊的粘度。在一些变通方案中,本文所述的液体制剂具有60%至80%厘泊的粘度。
用于递送治疗物质的制剂和液体制剂
本文所述的用于给药的治疗物质的“有效量”(本文中也称为“治疗有效量”)是当给药至个体时所寻求的产生治疗效果的治疗物质的量。获得不同的治疗效果可能需要不同有效量的治疗物质。例如,用于预防疾病或病症的治疗物质的治疗有效量与用于治疗、抑制疾病或病症、延迟其发作或致使其消退的治疗有效量可以是不同的。另外,治疗有效量可能取决于个体的年龄、体重和其它健康状况,这对于熟悉所述疾病或病症的专业人员来说是众所周知的。因此,在给药治疗物质的每一个体中,治疗有效量可以是不相同的。
用于治疗、预防、抑制疾病或病症、延迟其发作或致使其消退的治疗有效量在本文中也指有效治疗、预防、抑制疾病或病症、延迟其发作或致使其消退的治疗物质的量。
为了测定治疗物质的水平对于治疗、预防、抑制描述在“疾病和病症”部分的疾病和病症、延迟其发作或致使其消退是否是“治疗有效量”,可以将液体制剂给药至有关疾病或病症的动物模型,效果可以得以观察。
治疗有效量的治疗物质的长时间递送可以通过液体制剂的单次给药实现,或者可以通过液体制剂的两个或多个剂量给药实现。作为所述多次施用的非限制性示例,使用于治疗、预防、抑制湿性AMD、延迟其发作或致使其消退的雷帕霉素的治疗量维持3个月可以通过下述方法实现:将递送3个月治疗量的单剂量液体制剂给药;或连续使用多剂量液体制剂。最佳剂量方案取决于需要递送的治疗物质的治疗量、需要递送治疗物质的时期和液体制剂的递送动力学。熟悉这类长期治疗物质递送给药的技术人员在本文所述指导下应当懂得如何确定可以使用的给药方案。
当使用某些治疗物质用于治疗、预防、抑制某些疾病、延迟其发作或致使其消退时,一旦将制剂放进眼睛部位,治疗物质的递送不立即开始,而是有些延迟后才开始递送,这是合乎需要的。例如,但没有任何限制,所述缓释在治疗物质抑制或延缓伤口治愈时可能是有用的,且一旦制剂放入就使任何伤口治愈发生时,缓释是所需的。根据被递送的治疗物质和/或被治疗、预防、抑制、延迟其发作或致使其消退的疾病和病症,在开始递送治疗物质前,延缓期可以是约1h、约6h、约12h、约18h、约1天、约2天、约3天、约4天、约5天、约6天、约7天、约8天、约9天、约10天、约11天、约12天、约13天、约14天、约21天、约28天、约35天或约42天。其它延缓期也是可能的。可以使用的缓释制剂对于熟悉本文所述的技术的人员是清楚的。
通常来说,治疗物质可以配制成任何制剂或液体制剂,所述制剂或液体制剂在需要的递送期间能够将治疗有效量的治疗物质递送到个体或个体的眼睛。制剂包括液体制剂。
治疗物质的溶解
可以使用的一种制剂或液体制剂是其中治疗物质溶解在溶剂成分中的制剂或液体制剂。通常来说,可以使用治疗物质可在其中溶解的具有所需作用的任何溶剂。在一些变通方案中,溶剂是含水的。在一些变通方案中,溶剂是非水的。“含水溶剂”是包含至少约50%的水的溶剂。
通常来说,可以使用具有期望效果的任何浓度的溶解的治疗物质。溶剂成分可以是单一溶剂或者可以是溶剂混合物。溶剂和溶液类型对于熟悉此类药物递送技术的人员是众所周知的。参见例如Remington,药剂学和药剂学方法(Remington:The Science and Practice of Pharmacy),第20版,Lippincott Williams&Wilkins,第20版(2000年12月15日);Ansel氏药物剂型和药物递送系统(Ansel′s Pharmaceutical Dosage Forms and DrugDelivery Systems),第8版,Lippincott Williams&Wilkins(2004年8月);药物赋形剂手册2003,美国药学会,华盛顿,DC,USA和药物出版社,伦敦,UK;和Strickley,口服制剂和注射制剂中的增溶赋形剂(solubilizingExcipients in Oral and Injectable Formulations),药学研究(PharmaceuticalResearch),第21卷,第2期,2004年2月。
如前面所提到的,一些溶剂还可以作为增溶剂。
可以被使用的溶剂包括但不是限于下列溶剂中的任何一种或多种:DMSO、乙醇、甲醇、异丙醇;蓖麻油、丙二醇、甘油、聚山梨酯80、苄醇、二甲基乙酰胺(DMA)、二甲基甲酰胺(DMF)、甘油缩甲醛、乙氧基二甘醇(二乙二醇单乙醚(Transcutol),佳法塞公司(Gattefosse))、三乙二醇二甲醚(三甘醇二甲醚(Triglyme))、三醋精、二醋精、玉米油、乙酰基柠檬酸三乙酯(ATC)、乳酸乙酯、二甲基异山梨醇酯(DMI)、γ-丁内酯、N-甲基-2-吡咯烷酮(NMP)、各种分子量的聚乙二醇(包括但不限于PEG 300和PEG 400)、聚羟乙酸辛酸甘油酯(Labrasol,佳法塞公司)。
在一些变通方案中,溶剂是聚乙二醇。聚乙二醇以各种名字为大家所知,且可以通过各种制备方法得到,包括但不限于大粒凝胶(macrogel)、大粒凝胶400、大粒凝胶1500、大粒凝胶4000、大粒凝胶6000、大粒凝胶20000、聚乙二醇(macrogola)、breox PEG、碳蜡(carbowax)、carbowaxsentry、Hodag PEG、Lipo、Lipoxol、Lutrol E、PEG、Pluriol E、聚氧乙烯二醇和α-氢-ω-羟基-聚(氧基-1,2-乙烷二基)。
其它溶剂包括足以使治疗物质增溶量的C6-C24脂肪酸。
也可以使用磷脂溶液,例如卵磷脂、磷脂酰胆碱或各种连接到磷酸胆碱酯的硬脂酸、棕榈酸和油酸的二甘油酯的混合物、氢化大豆磷脂酰胆碱(HSPC)、二硬脂酰磷脂酰甘油(DSPG)、L-α-二肉豆蔻酰磷脂酰胆碱(DMPC)、L-α-二肉豆蔻酰磷脂酰甘油(DMPG)。
溶解治疗物质的成分的其它示例包括例如如下成分,如醇类、丙二醇、各种分子量的聚乙二醇、丙二醇酯类、脂肪酸(例如油酸、硬脂酸、棕榈酸、癸酸、亚油酸等)酯化的丙二醇;中链单、二或三甘油酯、长链脂肪酸、天然存在的油类和它们的混合物。溶剂系统的油类成分包括商业可购买的油类以及天然存在的油脂。油类还可以是植物油或矿物油。油类可以具有非表面活性油类的特征,其通常没有亲水亲油平衡值。可以商业购得的物质包括中链三甘油酯类,包括但不是限于Captex 100、Captex 300、Captex355、Miglyol 810、Miglyol 812、Miglyol 818、Miglyol 829和Dynacerin 660。可以商业购得的丙二醇酯制剂包括Captex 200和Miglyol 840等。商业产品Capmul MCM包括包含单甘油酯类和双甘油酯类的许多合理的中链混合物之一。
其它溶剂包括天然存在的油类例如薄荷油和种子油。示例性的天然油类包括油酸、蓖麻油、红花籽油、大豆油、橄榄油、葵花籽油、芝麻油和花生油。还可以使用大豆脂肪酸。完全饱和的非水溶剂的示例包括但不限于中链至长链脂肪酸的酯类(例如链长约C6至约C24的脂肪酸三甘油酯)。还可以使用氢化的豆油和其它植物油。脂肪酸的混合物可以从天然油(例如椰子油、棕榈仁油、巴巴苏油等)中分离并精制。在一些实施方案中,还可以使用中链(约C8至约C12)的三甘油酯类(例如衍生自椰子油或棕榈仁油的辛酸/癸酸三甘油酯类)。还可以使用中链的单和双甘油酯。其它完全饱和的非水溶剂包括但不限于饱和的椰子油(其通常包含月桂酸、肉豆蔻酸、棕榈酸、癸酸和己酸的混合物),所述椰子油包括来自海斯(Huls)的以商标MiglyolTM出售的和带有商品标示810、812、829和840的那些。还应提及由德鲁化学(Drew Chemicals)出售的NeoBeeTM产品。非水溶剂包括肉豆蔻酸异丙酯。合成油类的示例包括具有6至24个碳原子的饱和或不饱和脂肪酸的三甘油酯和丙二醇二酯,所述饱和脂肪酸例如己酸、辛酸(羊脂酸)、壬酸(天竺葵酸)、癸酸(羊蜡酸)、十一酸、月桂酸、十三酸、十四酸(肉豆蔻酸)、十五酸、十六酸(棕榈酸)、十七酸、十八酸(硬脂酸)、十九酸、十七酸、花生酸、二十一酸、二十二酸和二十四酸等。不饱和羧酸的示例包括油酸、亚油酸、亚麻酸等。非水溶剂可以包括脂肪酸的单、二和三甘油酯或混酸甘油酯和/或丙二醇的单或双酯,其中至少一分子的甘油被不同碳原子长度的脂肪酸酯化。用作溶剂的“非油”的非限制性示例是聚乙二醇。
示例性植物油包括棉籽油、玉米油、芝麻油、大豆油、橄榄油、分馏椰子油、花生油、葵花子油、红花油、杏仁油、鳄梨油、棕榈油、棕榈仁油、巴巴苏油、山毛榉油(beechnut oil)、亚麻籽油、菜籽油等。植物油的单、双和三甘油酯(包括但不限于玉米)也可以使用。
交联的或不交联的聚乙烯吡咯烷酮(PVP)也可以用作溶剂。其它溶剂包括但不限于C6-C24脂肪酸、油酸、Imwitor 742、Capmul、F68、F68(Lutrol)、普流罗尼克类(PLURONICS)(包括但不是限于普流罗尼克F108、F127和F68、泊洛沙姆类、聚醚胺类(Jeffamines))、Tetronics、F127;环糊精例如α-环糊精、β-环糊精、羟丙基-β-环糊精、磺丁基醚-β-环糊精(Captisol);CMC、聚脱水山梨糖醇20、Cavitron、各种分子量的聚乙二醇(包括但不限于PEG 300和PEG 400)。
蜂蜡和d-α-生育酚(维生素E)也可以用做溶剂。
用于液体制剂的溶剂可以根据本领域公知的各种方法确定,包括但不限于(1)采用本领域的标准方程,理论上估计它们的溶解度参数值,并选择与治疗物质匹配的溶剂;和(2)实验测定治疗物质在溶剂中的饱和溶解度,选择显示期望溶解度的溶剂。
雷帕霉素的溶解
当治疗物质是雷帕霉素时,溶剂包括但不限于如上的任何溶剂,包括但不限于下列溶剂中的任何一种或多种:DMSO、甘油、乙醇、甲醇、异丙醇;蓖麻油、丙二醇、三甘醇、三醋精、二醋精、玉米油、乙酰基柠檬酸三乙酯(ATC)、乳酸乙酯、聚乙烯丙烯、聚山梨酯80、苄醇、二甲基乙酰胺(DMA)、二甲基亚砜(DMF)、甘油缩甲醛、乙氧基二甘醇(Transcutol,佳法塞公司(Gattefosse))、三乙二醇二甲醚(三甘醇二甲醚)、二甲基异山梨醇酯(DMI)、γ-丁内酯、N-甲基-2-吡咯烷酮(NMP)、各种分子量的聚乙二醇(包括但不限于PEG 300和PEG 400)和聚羟乙酸辛酸甘油酯(Labrasol,佳法塞公司)。
其它溶剂包括但不限于C6-C24脂肪酸、油酸、Imwitor 742、Capmul、F68、F68(Lutrol)、普流罗尼克类(包括但不限于普流罗尼克F108、F127和F68、泊洛沙姆类、聚醚胺类)、Tetronics、F127、β-环糊精、CMC、聚脱水山梨糖醇20、Cavitron、softigen 767、captisol和芝麻油。
其它可以用于溶解雷帕霉素的方法描述在雷帕霉素的溶解,P.Simamora等人,Int′l J.Pharma,213:(2001)25-29,将其以全部内容引入文中作为参考。
作为非限制性示例,雷帕霉素可以溶解在5%DMSO或甲醇的盐平衡溶液中。雷帕霉素溶液可以是雷帕霉素的不饱和、饱和或过饱和溶液。雷帕霉素溶液可以与固体雷帕霉素接触。在一个非限制性示例中,雷帕霉素可以以高达约400mg/ml的浓度溶解。雷帕霉素还可以例如溶解在脂肪酸(例如油酸、硬脂酸、棕榈酸、癸酸、亚油酸等)酯化的丙二醇中。
许多其它溶剂是可用的。根据本文所述,本领域普通技术人员将发现确定用于雷帕霉素的溶剂是常规的。
增溶剂
通常来说,任何增溶剂或增溶剂的组合可以用于本文所述的液体制剂。
在一些变通方案中,增溶剂是表面活性剂或表面活性剂的组合。许多表面活性剂是可用的。还可以使用表面活性剂的组合,包括各种类型的表面活性剂的组合。例如,可以使用非离子的、阴离子的(即肥皂、磺酸盐)、阳离子的(即CTAB)、两性离子的、多聚体的或两性的表面活性剂。
能被使用的表面活性剂可以通过下述确定:把所关注的治疗物质和假定的溶剂及假定的表面活性剂混合,在暴露于介质后观察制剂的性质。
表面活性剂的示例包括但不限于脂肪酸酯类或酰胺类或醚类似物或它们的亲水衍生物;单酯或二酯或它们的亲水衍生物;或它们的混合物;甘油单酯或甘油二酯或它们的亲水衍生物;或它们的混合物;富含甘油单酯或/和甘油二酯的混合物或它们的亲水衍生物;用亲水基团部分衍生化的表面活性剂;其它醇类、多元醇类、糖类或寡糖类或多糖类、氧基烯基寡聚体或多聚体或嵌段聚合体的单酯或二酯或多酯,或它们的亲水衍生物,或它们的酰胺类似物;胺类、多胺类、多亚胺类、氨基醇类、氨基糖类、羟基烷基胺类、羟基多亚胺类、肽类、多肽类的脂肪酸衍生物,或它们的醚类似物。
亲水亲油平衡(″HLB″)是表面活性剂对水和油(或对所关注的乳剂系统的两相)的同时的相对吸引力的表示。
表面活性剂根据它们的分子的亲水和亲油部分的平衡进行分类。亲水亲油平衡(HLB)数表明分子的极性在1-40的任意范围里,最常用的乳化剂具有1-20的值。HLB随着亲水性增加而增加。
可以使用的表面活性剂包括但不限于HLB大于10、11、12、13或14的那些。表面活性剂的示例包括氢化植物油的聚氧乙烯产物、聚乙氧基化的蓖麻油或聚乙氧基化的氢化蓖麻油、聚氧乙烯-脱水山梨糖醇-脂肪酸酯类、聚氧乙烯蓖麻油衍生物等,例如Nikkol HCO-50、Nikkol HCO-35、Nikkol HCO-40、Nikkol HCO-60(来自日高化学有限责任公司(NikkoChemicals Co.Ltd.));Cremophor(来自巴斯夫(BASF))例如CremophorRH40、Cremophor RH60、Cremophor EL;吐温类(来自ICI化学(ICIChemicals))例如吐温20、吐温21、吐温40、吐温60、吐温80、吐温81,Cremophor RH 410、Cremophor RH 455等。
表面活性剂成分可以选自具有至少一个醚的化合物,所述醚由至少约1至100个环氧乙烷单元和至少一个具有至少约12至22个碳原子的脂肪醇链形成;具有至少一个酯的化合物,所述酯由至少约1至100个环氧乙烷单元和至少一个具有至少约12至22个碳原子的脂肪酸链形成;具有至少一个醚、酯或酰胺的化合物,所述醚、酯或酰胺由至少约1至100个环氧乙烷单元和至少一个维生素或维生素衍生物形成;和它们的组合,其由不超过两种表面活性剂组成。
表面活性剂的其它示例包括Lumulse GRH-40、TGPS、聚山梨醇酯-80(吐温-80)、聚山梨醇酯-20(吐温-20)、聚氧乙烯(20)脱水山梨糖醇单油酸酯、甘油基丙二醇酯、聚乙二醇酯、聚乙二醇化的(polyglycolyzed)甘油酯等或它们的混合物;聚乙烯脱水山梨糖醇脂肪酸酯、聚氧乙烯甘油酯,例如Tagat TO、Tagat L、TagatI、tagatI2和Tagat 0(可从德国Essen的高施米特化学公司(Goldschmidt Chemical Co.)商业购买);乙二醇酯,例如硬脂酸乙二醇酯和二硬脂酸乙二醇酯;丙二醇酯,例如肉豆蔻酸丙二醇酯;脂肪酸甘油酯,例如硬脂酸甘油酯和单硬脂酸甘油酯;脱水山梨糖醇酯,例如司盘类和吐温类;聚甘油酯,例如聚甘油基4-油酸酯;脂肪醇乙氧基化物例如布里杰(Brij)型乳化剂;乙氧基化丙氧基化的嵌段共聚物,例如泊洛沙姆类;脂肪酸的聚乙二醇酯,例如PEG 300亚油酸甘油酯或Labrafil 2125CS、PEG 300油酸甘油酯或Labrafi1 M 1944CS、PEG 400辛酸/癸酸甘油酯或Labrasol,和PEG 300辛酸/癸酸甘油酯或Softigen 767;cremophors例如Cremophor E、聚氧乙烯(polyoxyl)35蓖麻油或Cremophor EL、Cremophor EL-P、Cremophor RH 4OP、聚氧乙烯40氢化蓖麻油、Cremophor RH40;聚氧乙烯60氢化蓖麻油或Cremophor RH 60;单辛酸/癸酸甘油酯,例如Campmul CM 10;聚氧乙基化脂肪酸(PEG-硬脂酸酯、PED-月桂酸酯、)、聚氧乙烯化的(polyoxylated)脂肪酸甘油酯、聚氧乙烯化的甘油脂肪酸酯即Solutol HS-15;PEG-醚类脱水山梨糖醇衍生物(吐温类),脱水山梨糖醇单油酸酯或司盘20、芳香化合物PEG-甘油酯(PECEOLTM)、PEG-PPG(聚丙二醇)共聚物(普流罗尼克类包括但不限于普流罗尼克F108、F127和F68、泊洛沙姆、聚醚胺类)、Tetronics、聚甘油、PEG-生育酚类、PEG-LICOL 6-油酸酯;丙二醇衍生物、糖和多糖烷基和酰基衍生物(辛基蔗糖、蔗糖硬脂酸酯、月桂酰葡聚糖等)和/或它们的混合物;基于与环氧乙烷共聚的多元醇的油酸酯或月桂酸酯的表面活性剂;Labrasol Gelucire 44/14;聚氧乙烯硬脂酸酯;饱和的聚乙二醇化的甘油酯;或泊洛沙姆;所有上述物质是可以商业购买的。聚氧乙烯脱水山梨糖醇脂肪酸酯可以包括聚山梨酯类,例如聚山梨酯20、聚山梨酯40、聚山梨酯60和聚山梨酯80。聚氧乙烯硬脂酸酯可以包括聚氧乙烯6硬脂酸酯、聚氧乙烯8硬脂酸酯、聚氧乙烯12硬脂酸酯和聚氧乙烯20硬脂酸酯。饱和的聚乙二醇化的甘油酯是例如GELUCIRE 44/14或GELUCIRETM 50/13(佳法赛(Gattefosse),westwood,N.J.,U.S.A.)。本文所用的泊洛沙姆包括泊洛沙姆124和泊洛沙姆188。
表面活性剂包括d-α-生育酚基聚乙二醇1000琥珀酸酯(TPGS)、聚氧乙烯8硬脂酸酯(PEG 400单硬脂酸酯)、聚氧乙烯40硬脂酸酯(PEG 1750单硬脂酸酯)和薄荷油。
在一些变通方案中,使用HLB小于10的表面活性剂。这些表面活性剂可以任选与其它作为共表面活性剂的表面活性剂组合使用。HLB小于或等于10的一些表面活性剂、混合物和其它相当的制剂的示例是丙二醇类、甘油基脂肪酸类、甘油基脂肪酸酯类、聚乙二醇酯类、甘油基乙二醇酯类、聚乙二醇化的甘油酯类和聚氧乙基甾基(steryl)醚类。丙二醇酯类或部分酯类形成商业产品制剂,例如Lauroglycol FCC,Lauroglycol FCC包含丙二醇月桂酸酯。可以商业购买的赋形剂Maisine 35-1包含长链脂肪酸,例如亚油酸甘油酯。还可以使用包含聚氧乙烯硬脂酰基醚的产品,例如AccononE。Labrafil M 1944CS是其中制剂包含甘油基乙二醇酯类和聚乙二醇酯类的混合物的表面活性剂的一个示例。
雷帕霉素的增溶剂
许多增溶剂可以被用于雷帕霉素,包括但不限于本文所述的那些。
在一些变通方案中,增溶剂是表面活性剂。可以用于雷帕霉素的表面活性剂的非限制性示例包括但不限于HLB大于10、11、12、13或14的表面活性剂。一个非限制性示例是Cremophor EL。在一些变通方案中,表面活性剂可以是聚合物表面活性剂,所述聚合物表面活性剂包括但不限于普流罗尼克F108、F127和F68及Tetronics。如上所述,一些溶剂也可以用途表面活性剂。在本文指导下,本领域的普通技术人员将发现可以常规地确定可以用于雷帕霉素的增溶剂和表面活性剂。
粘度改性剂
本文所述的液体制剂可以和粘度改性剂一起给药或另外包含粘度改性剂。
一种可以使用的示例性粘度改性剂是透明质酸。透明质酸是一种糖胺聚糖。它由重复序列的葡糖醛酸和葡糖胺组成。透明质酸存在于身体的许多组织和器官中,且促成那些组织和器官的粘度和稠度。透明质酸存在于眼睛中,包括眼睛的玻璃体,且和胶原一起促成它的粘度。本文所述的液体制剂可以另外包含透明质酸或和透明质酸一起给药。
粘度改性剂的其它非限制性示例包括聚环氧烷、甘油、羧甲基纤维素、海藻酸钠、壳聚糖、葡聚糖、硫酸葡聚糖和胶原。这些粘度改性剂可以是化学修饰的。
其它可以使用的粘度改性剂包括但不限于角叉菜胶、纤维素凝胶、胶体二氧化硅、明胶、碳酸丙烯、碳酸、海藻酸、琼脂、羧基乙烯基聚合物或卡波姆和聚丙烯酰胺、阿拉伯胶(acacia)、酯胶、瓜尔胶、阿拉伯胶(gumarabic)、茄替胶、刺梧桐树胶、黄蓍胶、胶土(terra)、果胶、罗望子种子、落叶松阿拉伯半乳聚糖、藻酸盐、角豆、黄原胶、淀粉、硅酸镁铝、黄蓍胶、聚乙烯醇、结冷胶(gellan gum)、水胶体混合物和聚维酮。还可以使用本领域公知的其它粘度改性剂,包括但不限于羧甲基纤维素钠、褐藻胶(algin)、鹿角菜胶、半乳甘露聚糖、羟基丙基甲基纤维素、羟基丙基纤维素、聚乙二醇、聚乙烯吡咯烷酮、羧甲基壳多糖钠、羧甲基葡聚糖钠、羧甲基淀粉钠、黄原胶和玉米蛋白。
药物制剂
除非上下文中另外清楚地说明,否则本文所述的任何制剂可以用于本文所述的任何药物制剂。
本文所述的制剂还可以包含各种其它成分例如稳定剂。
在本文所述的制剂中,稳定剂不是必需的。然而,在一些变通方案中,可能需要加入稳定剂。在本文所述的制剂中可以使用的稳定剂的非限制性示例包括但不限于如下物质,所述物质能(1)改善赋形剂与包封材料例如明胶的相容性;(2)提高治疗物质例如雷帕霉素和/或雷帕霉素衍生物的稳定性(例如防止治疗物质例如雷帕霉素的晶体生长);和/或(3)提高制剂稳定性。应注意,在稳定剂成分和溶剂、增溶剂或表面活性剂成分之间有重叠,并且同一成分可以起到不止一种的作用。
稳定剂可以选自脂肪酸类、脂肪醇类、醇类、长链脂肪酸酯类、长链醚类、脂肪酸的亲水衍生物、聚乙烯吡咯酮类、聚乙烯醚类、聚乙烯醇类、碳氢化合物、疏水聚合物、吸湿聚合物和它们的组合。还可以使用上述稳定剂的酰胺类似物。所选的稳定剂可以改变制剂的疏水性(例如油酸、蜡)或改善制剂中各种成分的混合(例如乙醇),控制制剂的水分水平(例如PVP),控制相的流动性(熔点高于室温的物质例如长链脂肪酸、醇、酯、醚、酰胺等或它们的混合物;蜡),和/或改善制剂与包封材料的相容性(例如油酸或蜡)。这些稳定剂中的一些可以用做溶剂/共溶剂(例如乙醇)。稳定剂可以以足够抑制治疗物质(例如雷帕霉素)结晶的量存在。
稳定剂的示例包括但不限于饱和的、单烯的、多烯的、支链的、含环的、炔的、二羧基的和含官能团的脂肪酸例如油酸、辛酸、癸酸、己酸、月桂酸、肉豆蔻酸、棕榈酸、硬脂酸、山嵛酸、亚油酸、亚麻酸、二十碳五烯酸(EPA)、DHA;脂肪醇例如硬脂醇、鲸蜡醇、ceteryl醇;其它醇例如乙醇、异丙醇、丁醇;长链脂肪酸酯、醚或酰胺,例如硬脂酸甘油酯、硬脂酸鲸蜡酯、油烯基醚、硬脂酰基醚、鲸蜡基醚、鲸蜡基酰胺、油烯基酰胺、硬脂酰基酰胺;脂肪酸的亲水衍生物,例如聚甘油脂肪酸、聚乙二醇脂肪酸酯、聚乙烯吡咯酮、聚乙烯醇(PVA)、蜡、二十二碳六烯酸、脱氢枞酸等。
所述的制剂还可以包含胶凝剂,该胶凝剂通过形成凝胶改变最终制剂的质地。
可以将如本文所述使用的治疗物质例如雷帕霉素进行常规药学操作,例如灭菌,并且包含治疗物质的制剂还可以包含常规的辅助剂例如防腐剂、稳定剂、湿润剂、乳化剂、缓冲剂等。治疗物质还可以与药学上可接受的临床应用的赋形剂一起配制,以便生产药物制剂。用于眼科给药的制剂可以以下列形式存在:溶液剂、混悬剂、固体物质的颗粒、固体物质的离散团块(掺入到聚合物基质中的)、液体制剂存在或用于眼科给药的任何其它形式。治疗物质可以用来制备用于治疗、预防、抑制本文所述的任何病症、延迟其发作或致使其消退的药物。在一些变通方案中,治疗物质可以用来制备用于治疗本文所述的任何病症的药物。
包含治疗物质例如雷帕霉素的制剂可以包含一种或多种适于指定的给药途径的辅助剂。治疗物质可以与之混合的辅助剂包括但不限于乳糖、蔗糖、淀粉粉末、链烷酸的纤维素酯类、硬脂酸、滑石粉、硬脂酸镁、氧化镁、磷酸和硫酸的钠盐和钙盐、阿拉伯胶、明胶、海藻酸钠、聚乙烯吡咯烷酮和/或聚乙烯醇。当需要溶解的制剂时,治疗物质可以是在溶剂中,所述溶剂包括但不限于各种分子量的聚乙二醇、丙二醇、羧甲基纤维素胶体溶液、甲醇、乙醇、DMSO、玉米油、花生油、棉籽油、芝麻油、黄蓍胶和/或各种缓冲液。其它辅助剂和给药方式是制药领域众所周知的,且可以用于实施本文所述的方法、制剂和液体制剂。载体或稀释剂可以包括延时材料,例如单独的单硬脂酸甘油酯或二硬脂酸甘油酯,或与蜡一起,或本领域众所周知的其它材料。如本文所述使用的制剂还可以包含凝胶制剂、可侵蚀的和不可侵蚀的聚合物、微球和脂质体。
其它可以被使用的辅助剂和赋形剂包括但不限于C8-C10脂肪酸酯例如softigen 767、聚山梨醇酯80、普流罗尼克类、Tetronics、Miglyol和Transcutol。
通常在制药领域中使用的添加剂和稀释剂可以任选地加入到药物制剂和液体制剂中。这些包括增稠剂、成粒剂、分散剂、矫味剂、甜味剂、着色剂和稳定剂(包括pH稳定剂)、其它赋形剂、抗氧化剂(例如生育酚、BHA、BHT、TBHQ、醋酸生育酚、抗坏血酸棕榈酸酯、抗坏血酸没食子酸丙酯等)、防腐剂(例如对羟基苯甲酸酯类)等。示例性防腐剂包括但不限于苄醇、乙醇、苯扎氯铵、苯酚、三氯叔丁醇等。一些有用的抗氧化剂为制剂提供氧气或过氧化物抑制剂,所述抗氧化剂包括但不限于丁基化羟基甲苯、丁基羟基茴香醚、没食子酸丙酯、抗坏血酸棕榈酸酯、α-生育酚等。增稠剂例如卵磷脂、羟基丙基纤维素、硬脂酸铝等可以改善制剂的质地。
另外,可以将粘稠的聚合物加入到混悬剂中,以有助于定位和易于放置和处理。在液体制剂的一些使用中,可以经外科手术形成在巩膜中的囊,以便接受液体制剂的注射。巩膜的水凝胶结构可作为控速膜。形成混悬液的治疗物质颗粒可以通过公知的方法制备,包括但不限于通过球磨研磨,例如利用陶瓷珠。例如,Cole Parmer球磨机如Labmill 8000可以与得自东曹达(Tosoh)或诺斯顿(Norstone)公司的0.8mm YTZ陶瓷珠一起使用。
另一方面,提供了如文中所述的治疗物质(包括但不限于雷帕霉素)的制剂或药物制剂在制备药物中的用途。具体而言,制备用于治疗如本文所述的病症的药物。此外,除非另外说明,各种本文所述的药物制剂也旨在用于制备治疗本文所述的病症的药物,并根据本文所述的方法使用。
用于制备和包装治疗物质的液体制剂的方法
可以用于制备本文所述的液体制剂(包括但不限于包含雷帕霉素的液体制剂)的一个非限制性方法是:将溶剂和治疗物质在室温或者略微升高的温度下混合在一起,直至得到溶液或混悬液,并任选使用超声波仪),接着冷却制剂。然后可以将其它成分(包括但不限于上述那些)与制剂混合。还可以使用其它制备方法,且在本文指导下,它们对于本领域技术人员是可识别的。
参照图1A-1F中显示的流程图,将用于制备和包装治疗物质的液体制剂的方法的示例和变通方案描述在本文中。在一些变通方案中,这些方法用于制备液体制剂,所述液体制剂包括但不限于描述在发明详述部分的那些,其包括描述在表格和实施例中的那些液体制剂。图1A-1F的流程图中所示的示例性方法的一些变通方案不包括所示的所有步骤。在一些变通方案中,在这些流程图中所示的一些步骤并不以所述的顺序执行。并且,所述方法的一些变通方案包括没有显示在流程图中的方法步骤。
参照一种制备和包装一种或多种治疗物质的液体制剂的示例性方法的图1A,在步骤110中,制备一种或多种储备溶液。在一些变通方案中,制备一种或多种治疗物质的储备溶液。当液体制剂包含多种治疗物质时,在一些变通方案中,制备包含几种治疗物质的储备溶液。在其它变通方案中,对于每一种治疗物质制备单独的储备溶液。在一些变通方案中,例如制备包含在液体制剂中的其它成分如稳定剂的储备溶液,或将一种或多种这类成分包含在治疗物质的储备溶液中。在一些变通方案中,液体制剂的一种或多种成分的储备溶液是可以商业得到的,而不是根据在图1A所示的部分方法制备的。
在一些变通方案中,在110中步骤中制备一种或多种储备溶液,以立即用于制备一种或多种治疗物质的液体制剂。在其它变通方案中,制备一种或多种储备溶液,然后贮存一段时间,这不会使一种或多种治疗物质的稳定性降低超过约10%。在一些变通方案中,将一种或多种储备溶液贮存长达约1小时、长达约2小时、长达约3小时、长达约4小时、长达约6小时、长达约8小时、长达约10小时、长达约16小时、长达约24小时、长达约2天、长达约3天、长达约5天、长达约7天、长达约1个月、长达约2个月、长达约3个月、长达约4个月、长达约5个月、长达约6个月、长达约7个月、长达约8个月、长达约9个月、长达约10个月、长达约11个月、长达约12个月或更长。在一些变通方案中,将一种或多种储备溶液贮存约1分钟至约两小时。在一些变通方案中,将一种或多种储备溶液贮存约1分钟至约1小时。在一些变通方案中,将一种或多种储备溶液贮存约30至约60分钟。通常,可以将储备溶液在任何条件下贮存任何一段时间,所述条件和时间是使一种或多种治疗物质的稳定性保持至少约50%、至少约60%、至少约70%、至少约80%、至少约90%、至少约92%、至少约94%、至少约96%、至少约98%或至少约99%的条件和时间。
用于制备储备溶液的溶剂包括但不限于溶剂、增溶剂和其它液体制剂成分例如描述在发明详述(包括表格和实施例)中的那些和它们的混合物。用于制备储备溶液的治疗物质包括但不是限于在治疗物质部分和在表格和实施例中列出的那些、以及它们的混合物。治疗物质例如可以以固体、粉末、溶液、混悬液或乳液形式提供。
在一些变通方案中,以使溶剂中的氧气水平减少的方式处理溶剂。在一些变通方案中,在图1B所示,将溶剂鼓泡通入惰性气体,例如稀有气体。在一些变通方案中,将溶剂鼓泡通入氮气。
在一些变通方案中,将治疗物质与溶剂混合,超声一段足以使治疗物质溶解在溶剂中的时间。在一些变通方案中,将混合物在使一种或多种治疗物质稳定性保持至少约50%、至少约60%、至少约70%、至少约80%、至少约90%、至少约92%、至少约94%、至少约96%、至少约98%或至少约99%的条件下超声一段时间。
在一些变通方案中,本文所述制剂的成分的稳定性是通过HPLC或质谱测定的。
在步骤120中,制备一种或多种稀释溶剂。在一些变通方案中,接着使用稀释溶剂(步骤130),以稀释一种或多种储备溶液,例如在步骤110中制备的那些。稀释溶剂也包括但不限于溶剂、增溶剂和液体制剂的其它成分例如描述在发明详述(包括表格和实施例)中的那些、以及它们的混合物。
在一些变通方案中,包括但不限于在图1C中所示的那些,将稀释溶剂脱气。在一些变通方案中,这种处理是为了降低气泡水平,因此降低在稀释溶剂中的氧气水平。在一些变通方案中,稀释溶剂通过离心脱气,包括但不限于使用双倒置离心机。在一些变通方案中,将稀释溶剂超声一段时间,所述时间足以降低在稀释溶剂中的氧气水平。在一些变通方案中,将稀释溶剂在使稀释溶剂稳定性保持至少约50%、至少约60%、至少约70%、至少约80%、至少约90%、至少约92%、至少约94%、至少约96%、至少约98%或至少约99%的条件下超声一段时间。在一些变通方案中,包括但不限于在图1C中所示的那些,将稀释溶剂鼓泡通入惰性气体,通气持续足以降低稀释溶剂中的氧气水平的一段时间。在一些变通方案中,将稀释溶剂超声并鼓泡通入惰性气体。在一些变通方案中,惰性气体是稀有气体,包括但不限于氮气、氩气或氦气。在一些变通方案中,惰性气体是氮气。
在一些变通方案中,将治疗物质或稀释溶剂用化学物质处理,以减少在稀释溶剂中的氧气或氧自由基的水平,所述化学物质包括但不限于抗氧化剂或除氧剂。在一些变通方案中,除氧剂是硫酸钠。在一些变通方案中,将稀释溶剂用物理力处理,以减少在稀释溶剂中的氧气水平,所述物理力包括但不限于物理压力,包括但不限于离心。在一些变通方案中,将稀释溶剂加热,以减少其中的氧气水平。在一些变通方案中,将稀释溶剂加热以减少其中的氧气水平,并在氮气覆盖下冷却。
在一些变通方案中,在步骤120中,制备一种或多种稀释溶剂,以立即用于制备一种或多种治疗物质的液体制剂。在其它变通方案中,制备一种或多种稀释溶剂,然后在使用前贮存一段时间。在一些变通方案中,将稀释溶剂贮存一段时间,以使它充分脱气。“充分脱气”是指将稀释溶剂处理如下的一段时间:当活性物质暴露于稀释溶剂时,相对于暴露于稀释溶剂之前的治疗物质的稳定性,治疗物质保留至少约90%的稳定性。在一些变通方案中,将稀释溶剂脱气到下述程度:贮存一段时间后,治疗物质保留至少约70%、至少约75%、至少约80%、至少约85%、至少约90%、至少约92%、至少约94%、至少约96%、至少约98%或至少约99%的稳定性。
在一些变通方案中,稀释溶剂贮存的时间长短取决于治疗物质对通过本文所述的一种或多种处理除去的气体的敏感性。在一些变通方案中,稀释溶剂贮存的时间长短取决于治疗物质对通过本文所述的一种或多种处理中除去的氧气的敏感性。
在一些变通方案中,稀释溶剂在制备后1小时内使用。在一些变通方案中,将稀释溶剂贮存约1分钟至约24小时、约1分钟至约12小时、约1分钟至约6小时、约1分钟至约4小时、约1分钟至约2小时或约1分钟至约1小时。
在步骤130中,将一种或多种储备溶液例如在步骤110中制备的那些与一种或多种稀释溶剂例如在步骤120中制备的那些合并。在一些变通方案中,这种方法如图1D所示。在一些变通方案中,将储备溶液与稀释溶剂通过在旋转蒸发仪上旋转足以使储备溶液与贮备溶液和稀释溶剂混合的一段时间来混合,同时相对于混合前的治疗物质,治疗物质的稳定性保留至少约70%、至少约75%、至少约80%、至少约85%、至少约90%、至少约92%、至少约94%、至少约96%、至少约98%或至少约99%。在一些变通方案中,采用形成均一混合物的任何方法,例如混合或涡旋,将一种或多种储备溶液与稀释溶剂混合。在一些变通方案中,液体制剂的其它成分的储备溶液或包含液体制剂的其它成分的储备溶液类似地制备。
参照图1D,在一些变通方案中,将一种或多种储备溶液与一种或多种稀释溶剂合并(图1A步骤130)包括:在步骤132中将一种或多种储备溶液与一种或多种稀释溶剂混合,在步骤134中将所得的溶液鼓泡通入惰性气体和在步骤136中填充惰性气体。在一些变通方案中,将一种或多种储备溶液与一种或多种稀释溶剂合并,并通过在旋转蒸发仪上将该溶液在一定温度下旋转一段时间进行混合,以得到储备溶液溶剂的期望终浓度。在一些变通方案中,所述一段时间是约10分钟至约6小时。在一些变通方案中,所述一段时间是约30分钟至约4小时。在一些变通方案中,所述一段时间是约1小时至约4小时。在一些变通方案中,使溶液温度保持低于导致治疗物质明显降解的水平。
在一些变通方案中,对从步骤130得到的混合物进行处理以便减少氧气或其它气体的水平。在一些变通方案中,通过用本文所述的惰性气体、化学物质或物理压力处理对混合物进行处理。在一些变通方案中,为了减少混合物暴露于周围环境,包括但不限于空气,对混合物进行处理。在一些变通方案中,将混合物用惰性气体覆盖,所述惰性气体例如稀有气体,包括但不限于氮气、氩气或氦气。
在一些变通方案中,从步骤130得到的混合物是溶液。
在步骤140中,将从步骤130得到的溶液浓缩。在一些变通方案中,包括但不限于在图1E中所示的那些,通过蒸发或其它方式除掉一些或所有的较低沸点溶剂,将溶液浓缩。在一些变通方案中,在步骤140中全部或部分除掉的溶剂是储备溶液的成分,所述成分是在步骤110中稀释前,将治疗物质或液体制剂的其他成分溶解在其中的成分。
在步骤150中,将从步骤140得到的溶液过滤。混合物可以用任何能除掉微生物的滤器过滤。在一些变通方案中,滤器是0.2微米的滤器。在一些变通方案中,膜或滤器是由PTFE(聚(四氟)乙烯)或PVDF(聚偏二氟乙烯)制成,包括但不限于由颇尔公司(Pall Corporation)生产的滤器和膜。
在一些变通方案中,包括但不限于在图1F中所示的那些,将经过滤的溶液处理,以减少溶液中的氧气或其它气体的水平。在一些变通方案中,将混合物用惰性气体处理,例如鼓泡通入稀有气体,或者用本文所述的化学物质或物理压力处理。在一些变通方案中,接着将混合物处理,以减少混合物暴露于周围环境,包括但不限于空气。在一些变通方案中,将混合物用惰性气体覆盖,所述气体例如稀有气体,包括但不限于氮气、氩气或氦气。
在步骤160中,将从步骤150得到的经过滤的溶液包装在一个或多个容器中。在一些变通方案中,包括但不限于在图1F中所示的那些,用使溶液对于空气的一种或多种成分的暴露降到最小的方式,将经过滤的溶液包装在一个或多个容器中。在一些变通方案中,将具有低的顶空的容器用于溶液,其中当与一种或多种成分暴露于空气前的活性水平或质量相比时,与空气的一种或多种成分(包括但不限于氧气)的接触改变溶液的活性水平或质量。
在一些变通方案中,相对于其中包含的液体制剂的体积而言,容器具备使顶空减少到最小的尺寸或形状。在一些变通方案中,通过使容器的填充体积增加到最大,将顶空减少到最小。在一些变通方案中,顶空小于约0.1%、小于约0.5%、小于约1%、小于约2%、小于约3%、小于约4%、小于约5%或小于约10%的溶液体积。在一些变通方案中,顶空是溶液体积的约0.1%至约0.5%、约0.5%至约1%、约1%至2%、约2%至约3%、约3%至约4%、约4%至约5%或约5%至约10%。
在一些变通方案中,顶空用空气填充。在一些变通方案中,顶空用惰性物质包括但不限于一种或多种惰性气体填充。在一些变通方案中,惰性气体是稀有气体,包括但不限于氮气、氩气或氦气。
在一些变通方案中,对容器进行设计,以使溶液和容器表面积之间的接触面积最小。在一些变通方案中,将溶液接触的容器部分处理或制造,以使溶液接触的容器部分与溶液的相互作用最小。
在一些变通方案中,容器包含塑料或玻璃或它们的组合,包括但不限于在本文指导下本领域技术人员使用的任何一种或多种塑料或玻璃。在一些变通方案中,溶液接触的容器部分由透明或棕色玻璃制成。在一些变通方案中,溶液接触的容器部分由透明玻璃制成,包括但不限于由West生产的那些。
在一些变通方案中,与液体形式制剂接触的容器部分由基本上保持它的形状,且不与液体形式的制剂以显著降低或改变液体形式的制剂活性的方式反应或互相作用的任何材料制成。在一些变通方案中,当与置于低容量容器之前的液体形式的制剂相比,液体形式的制剂活性降低或改变约0.1%至约1%、约1%至约2%、约2%至约3%、约3%至约5%、约5%至约10%、约10%至约15%、约15%至约20%、约20%至约25%、约25%至约50%或大于约50%。在一些变通方案中,当与置于容器之前的制剂相比时,液体形式的制剂活性降低或改变小于约20%、小于约15%、小于约13%、小于约10%、小于约8%、小于约6%、小于约4%或小于约2%。
在一些变通方案中,与制剂接触的容器部分包含玻璃。在一些变通方案中,与制剂接触的容器部分不包含硅。在一些变通方案中,与制剂接触的容器部分的确包含硅。在一些变通方案中,与制剂接触的容器部分是硅烷化的。在一些变通方案中,与制剂接触的容器部分包含不与制剂以显著降低或改变制剂的活性的方式反应或相互作用的塑料材料。
容器通常可以是由任何材料制成。在一些变通方案中,容器包含可塑的聚合物。在一些变通方案中,容器包含热塑性聚合物。在一些变通方案中,将热塑性聚合物与一种或多种其它聚合物(包括但不限于合成橡胶和增塑的聚烯烃)混合。
热塑性聚合物包括但不是限于聚烯烃类、聚酰胺类、聚酯类、聚碳酸酯类、聚砜类、聚缩醛类、聚内酯类、丙烯腈-丁二烯-苯乙烯树脂、聚苯醚、聚苯硫醚、苯乙烯-丙烯腈树脂、苯乙烯顺丁烯二酸酐、聚酰亚胺类、芳香聚酮类或上述两种或多种物质的混合物。聚烯烃类包括但不限于:包含一种或多种直链、支链或环状的C2至C40链烯烃的聚合物;包含与一种或多种C3至C40链烯烃、C3至C20α-链烯烃或C3至C10α-链烯烃共聚的丙烯的聚合物。聚烯烃类包括但不限于包含乙烯(包括但不限于与C3至C40链烯烃、C3至C20α-链烯烃或丙烯和/或丁烯共聚的乙烯)的聚合物。
合成橡胶包括但不限于乙烯丙烯橡胶、乙烯丙烯二烯单体橡胶、苯乙烯嵌段共聚物橡胶(包括SI、SIS、SB、SBS、SIBS等,其中S=苯乙烯,I=异丁烯和B=丁二烯)、丁基橡胶、卤代丁基橡胶、异丁烯和对烷基苯乙烯的共聚物、异丁烯和对烷基苯乙烯的卤代共聚物、天然橡胶、聚异戊二烯、丁二烯与丙烯腈的共聚物、聚氯丁烯、丙烯酸烷基酯橡胶、氯化的异戊二烯橡胶、丙烯腈氯化异戊二烯橡胶、聚丁二烯橡胶(顺式和反式)。
在一些变通方案中,容器包含一种或多种:聚丁烯、乙烯醋酸乙烯酯、低密度聚乙烯(密度0.915至小于0.935g/cm3)线性低密度聚乙烯、超低密度聚乙烯(密度0.86至小于0.90g/cm3)、极低密度聚乙烯(密度0.90至小于0.915g/cm3)、中等密度聚乙烯(密度0.935至小于0.945g/cm3)、高密度聚乙烯(密度0.945至0.98g/cm3)、乙烯醋酸乙烯酯、乙烯丙烯酸甲酯、丙烯酸共聚物、聚甲基丙烯酸甲酯或通过高压游离基方法聚合的任何其它聚合物、聚氯乙烯、聚1-丁烯、等规聚丁烯、ABS树脂、乙烯-丙烯橡胶(EPR)、硬化的EPR、EPDM、嵌段共聚物、苯乙烯嵌段共聚物、聚酰胺类、聚碳酸酯类、PET树脂、交联的聚乙烯、乙烯和乙烯醇共聚物(EVOH)、芳香单体的聚合物例如聚苯乙烯、聚-1酯类、聚缩醛、聚偏氟乙烯、聚乙二醇类和/或聚异丁烯。聚合物包括可以从埃克森化学公司(Exxon ChemicalCompany),Baytown,Tex购买的所用商标名为EXCEED和EXACT的那些。
容器可以通过任何合适的手段加工或成形。在一些变通方案中,容器是低容量注射器。在一些变通方案中,低容量注射器通过铸造、吹塑、压缩模型、注入塑型、热成型、注塑、滚塑成型或如描述在例如塑料加工(PLASTICS PROCESSING)(Radian Corporation,Noyes Data Corp.1986)中的其它加工方式,将该文献以全部内容引入文中作为参考。
在一些变通方案中,将与制剂接触的容器部分用与制成容器主体的材料不同的材料涂铺。在一些变通方案中,涂层是由不与制剂以显著减少或改变制剂的活性的方式反应或相互作用的材料构成。在一些变通方案中,制剂中的治疗物质基本上不被吸收或吸附到与之接触的容器部分的表面上。
在一些变通方案中,制剂是在密封容器中,且在25℃、5℃或-20℃中的一个或多个温度下能长时间稳定。在一些变通方案中,制剂是在密封容器中,且在-20℃能稳定至少约1、至少约2、至少约3、至少约4、至少约5、至少约6、至少约7、至少约8、至少约9、至少约10、至少约11、至少约12、至少约15、至少约18或至少约24个月的时间。在一些变通方案中,制剂是在密封容器中,且在5℃能稳定至少约1、至少约2、至少约3、至少约4、至少约5、至少约6、至少约7、至少约8、至少约9、至少约10、至少约11、至少约12、至少约15、至少约18或至少约24周的时间。在一些变通方案中,制剂是在密封容器中,且在5℃能稳定至少约1、至少约2、至少约3、至少约4、至少约5、至少约6、至少约7、至少约8、至少约9、至少约10、至少约11、至少约12、至少约15、至少约18或至少约24个月的时间。在一些变通方案中,制剂是在密封容器中,且在25℃能稳定至少约1、至少约2、至少约3、至少约4、至少约5、至少约6、至少约7、至少约8、至少约9、至少约10、至少约11、至少约12、至少约15、至少约18或至少约24周的时间。
在一些变通方案中,制剂是在密封容器中,且在-20℃,在至少约1、至少约2、至少约3、至少约4、至少约5、至少约6、至少约7、至少约8或至少约12个月的时间中是至少约95%稳定的。在一些变通方案中,制剂是在密封容器中,且在5℃,在至少约1、至少约2、至少约3、至少约4、至少约5、至少约6、至少约7、至少约8或至少约12个月的时间中是至少约95%稳定的。在一些变通方案中,制剂是在密封容器中,且在25℃,在至少约1、至少约2或至少约3个月的时间中是至少约95%稳定的。
在一些变通方案中,容器是低容量施药器(applicator),且低容量施药器是预填装的。
在一些变通方案中,在填装后,组合物在预填装的低容量施药器中能稳定至少约1、至少约2、至少约3、至少约4、至少约5、至少约6、至少约7、至少约14、至少约21、至少约28或至少约35天;至少约1个月、至少约2个月、至少约3个月、至少约4个月、至少约5个月、至少约6个月、至少约7个月、至少约8个月、至少约9个月、至少约10个月、至少约11个月或至少约12个月。
本文所述的是容器,该容器的壁是透明的、澄清的、着色的、不透明的、半透明的或它们的组合。在一些变通方案中,所述壁是半透明的和琥珀色的。在一些变通方案中,制剂容器是不透明的或半透明的,以保护制剂免受光线或其它的辐射形式影响,并带有透明或半透明部分。
在一些变通方案中,选择构成容器的至少一种材料,以保护或提高组合物的稳定性。在一些变通方案中,容器被设计用于容纳其中治疗物质或制剂的其它有关成分对光线或其它的辐射形式敏感的制剂。在一些变通方案中,容器减少或减弱将作用于或影响制剂的光线或其它辐射形式的水平、强度或形成。在一些变通方案中,将容器进行设计,以减少或减弱UV线(包括但不限于UVA、UVB和UVC)的水平、强度或形成。
在一些变通方案中,容器具有保护或提高组合物稳定性的次级包装。在一些变通方案中,次级包装减少或减弱作用于或影响制剂的光线或者其它辐射形式的水平、强度或形成。
在一些变通方案中,次级包装限制制剂与空气中的一种或多种成分接触。在一些变通方案中,次级包装作为对氧气的屏障。在一些变通方案中,次级包装用惰性气体包围,且对空气不渗透。在一些变通方案中,容器是在次级包装里,且容器和次级包装之间的空间中充满氮气。
在一些变通方案中,将容器设计为:当不是标准的室温温度和/或压力下贮存时,保持它的完整性和与制剂的一般水平的不反应性。在一些变通方案中,容器是预填装的,并且当将容器贮存在约-80℃至约40℃、约-40℃至约-10℃、约-25℃至约10℃、约0℃至约20℃或约20℃至约40℃时,保持它的完整性和与制剂的一般水平的不反应性。在一些变通方案中,当在上述温度范围贮存至少约1、至少约2、至少约3、至少约4、至少约5、至少约6、至少约7、至少约8、至少约9、至少约10、至少约11、至少约12、至少约15、至少约18或至少约24个月时,容器保持它的完整性和与制剂的一般水平的不反应性。
在一些变通方案中,对容器进行设计或选择,以使表面积与容积的比率减到最小。在一些变通方案中,对于填充体积小于约5ml、小于约4ml、小于约3ml、小于约2ml、小于约1ml、小于约0.7ml、小于约0.6ml、小于约0.5ml、小于约0.3ml、小于约0.2ml、小于约120μl、小于约100μl、小于约75μl、小于约60μl、小于约40μl、小于约30μl、小于约20μl、小于约10μl、小于约5μl、小于约2μl、约0.1至约20μl、约0.1至约10μl、约0.1至约5μl、约0.1至约50μl、约50至约100μl、约10至约200μl、约400至约600μl、约0.5ml至约1ml、约1ml至约2ml或约1ml至约5ml而言,对容器进行设计,以使表面积与容积的比率减到最小。
在一些变通方案中,将低容量施药器预先填装用于治疗眼科疾病或病症的治疗物质,包括但不限于用于治疗年龄相关性黄斑变性的莫司类化合物。本文所述的是预先填装包含雷帕霉素的制剂的预填装低容量施药器。在一些变通方案中,将低容量施药器预先填装稳定制剂,该稳定制剂包含雷帕霉素和聚乙二醇,并任选另外包含一种或多种其它成分(包括但不限于乙醇)。在一些变通方案中,预填装的低容量施药器预先填装包含约2%雷帕霉素、约94%PEG-400、约4%乙醇的稳定制剂。
本文所述的是包含一种或多种容器的药盒。在一些变通方案中,药盒包含一种或多种预先填装包含一种或多种治疗物质的一种或多种液体形式制剂的低容量施药器,所述液体形式制剂包括但不限于包含雷帕霉素的液体形式制剂、包含雷帕霉素和聚乙二醇并任选另外包含一种或多种其它成分(包括但不限于乙醇)的液体形式制剂以及包含约2%雷帕霉素、约94%PEG-400、约4%乙醇的液体形式制剂。在一些变通方案中,药盒包含一种或多种容器,包括但不限于预填装的低容量施药器,以及它的使用说明书。在另一变通方案中,药盒包含一种或多种预先填装雷帕霉素的低容量施药器以及它用于治疗眼睛疾病或病症的说明书。
在一些变通方案中,本文所述的容器是在次级包装中。在一些变通方案中,次级包装被配置,以保持相对于包装前治疗物质的稳定性的治疗物质稳定性。在一些变通方案中,对次级包装进行设计,以排除或减少制剂暴露于光线。在一些变通方案中,对次级包装进行设计,以排除或减少制剂暴露于一种或多种空气成分,例如氧气。在一些变通方案中,容器是安瓿、管形瓶或预填装的注射器。在一些变通方案中,容器是低容量施药器,例如描述在2005年10月11日提交的US临时专利申请号60/725,934,代理案卷号57796-30009.00中的那种。
在一些变通方案中,步骤110-160中的一些或全部在手套箱、洁净室或其它控制环境中进行。在一些变通方案中,将溶液在无菌环境中操作。在一些变通方案中,将溶液在氮气层下操作。在一些变通方案中,将溶液在惰性或稀有气体(包括但不限于氮气、氩气或氦气)层下操作。在一些变通方案中,当溶液放在容器中时,惰性气体覆盖在溶液的表面。
例如,在一些变通方案中,一个或多个步骤在氮气或其它惰性气体气氛下进行,以防止或减少液体制剂和它的成分与水、水蒸汽和氧气接触。
在一些变通方案中,惰性气体的级别是医用级别。在一些变通方案中,惰性气体是医用级别的稀有气体。在一些变通方案中,惰性气体是医用级别的压缩的氮气。在一些变通方案中,认为液体制剂的稳定性可以因此被提高。
在一些变通方案中,经过滤的溶液的容器在约-20℃、5℃或25℃的一个或多个温度下稳定至少约1周、至少约两周、至少约3周、至少约4周、至少约1个月、至少约两个月、至少约3个月、至少约4个月、至少约5个月、至少约6个月、至少约7个月、至少约8个月、至少约9个月、至少约10个月、至少约11个月、至少约12个月、至少约14个月、至少约16个月、至少约18个月、至少约20个月、至少约22个月、至少约24个月、至少约3年、至少约4年或至少约5年。在一些变通方案中,溶液在约-20℃的温度下稳定至少约3个月、至少约6个月、至少约9个月或至少约12个月。在一些变通方案中,溶液在约5℃的温度下稳定至少约1周、至少约两周、至少约4周、至少约1个月、至少约2个月、至少约3个月、至少约6个月、至少约9个月、至少约12个月、至少约18个月或至少约24个月。
在一些变通方案中,相对于在溶液被制备时治疗物质的量,测定稳定性。可以用质谱或HPLC测定治疗物质的稳定性。
在一些变通方案中,本文所述的制剂以一种或多种单位剂量形式提供,其中单位剂量形式包含一定量的本文所述的液体雷帕霉素制剂,所述量对于治疗或预防它被给药的疾病或病症是有效的。
在一些变通方案中,以将它给药的浓度制备单位剂量形式。在一些变通方案中,在给药至个体前,将单位剂量形式稀释。
在另一方面,本文提供的是包含如本文所述的一种或多种单位剂量形式的药盒。在一些实施方案中,药盒包含用于治疗一种或多种疾病和病症的一个或多个包装和说明书。在一些实施方案中,药盒包含与制剂或药物制剂没有身体接触的稀释剂。在一些实施方案中,药盒包含在一个或多个密封容器中的本文所述的一种或多种单位剂量形式中的任何一种。在一些实施方案中,药盒包含一种或多种无菌单位剂量形式中的任何一种。
可以被治疗、预防、抑制、延迟发作或致使消退的疾病或病症
本文所述的是采用本文所述的治疗物质和制剂、液体制剂和方法可以治疗、预防、抑制、延迟其发作或致使其消退的疾病或病症的非限制性示例。在一些变通方案中,用本文所述的治疗物质和制剂、液体制剂和方法,使疾病或病症得到治疗。除非上下文中另外说明,所有的治疗方法可以在其上施行的个体包括人类个体是可以想象的。
通常来说,对于用本文所述的治疗物质和制剂、液体制剂和方法的治疗、预防、抑制、延迟发作或致使消退敏感的任何眼睛的疾病或病症可以被治疗、预防、抑制、延迟发作或致使消退、治疗或预防。眼睛疾病或病症的示例包括但不限于与新生血管形成包括视网膜和/或脉络膜新生血管形成相关的疾病或病症。
下面参考文献,将其各自以全部内容引入文中作为参考,显示了一种或多种制剂,包括但不限于雷帕霉素制剂,可以通过本文所述的方法使所述制剂稳定,且所述文献描述了各种剂量的雷帕霉素和其它治疗物质用于治疗各种疾病或病症的用途:2005年2月9日提交的US 60/651,790,题目为“用于眼睛治疗的制剂”;2005年2月9日提交的US 60/664,040,题目为“用于疾病或病症治疗的液体制剂”;2005年3月21日提交的US60/664,119,题目为“用于治疗疾病或病症的药物递送系统”;2005年3月21日提交的US 60/664,306,题目为“用于治疗疾病或病症的原位胶化制剂和液体制剂”;2006年2月9日提交的US 11/351,844,题目为“用于眼睛治疗的制剂”;2006年2月9日提交的US 11/351,761,题目为“用于疾病或病症治疗的液体制剂”;2006年3月21日提交的US 11/386,290,题目为“用于治疗疾病或病症的药物递送系统”;2006年2月9日提交的US 11/352,092,题目为“雷帕霉素制剂和它们的使用方法”;2006年2月9日提交的US 60/772,018,题目为“稳定制剂以及它们的制备和使用方法”;US 2005/0187241和US 2005/0064010。
用本文所述的制剂、液体制剂和方法可以治疗、预防、抑制、延迟发作或致使消退的与视网膜和/或脉络膜新生血管形成相关的疾病或病症包括但不限于糖尿病视网膜病变、黄斑变性、湿性和干性AMD、早产儿视网膜病(晶状体后纤维组织增生症)、感染引起的视网膜炎或脉络膜炎、假定眼组织胞浆菌病、近视性变性、血管样条纹症和眼外伤。用本文所述的制剂、液体制剂和方法可以治疗、预防、抑制、延迟发作或致使消退的眼睛疾病或病症的其它非限制性示例包括但不限于弹性纤维假黄瘤、静脉闭塞、动脉闭塞、颈动脉闭塞疾病、镰状细胞性贫血、视网膜静脉周围炎、近视、慢性视网膜剥离、粘滞性过高综合征、弓形体病、外伤、息肉状脉络膜血管病变、激光损伤后(post-laser)并发症、特发性中心浆液脉络膜视网膜病并发症、脉络膜炎症的并发症、发红、与发红相关的疾病(角(angle)的新生血管形成)、新生血管性青光眼、葡萄膜炎和慢性葡萄膜炎、黄斑水肿、增殖性视网膜病、由维管和纤维组织异常增殖引起的疾病或病症包括所有形式的增殖性玻璃体视网膜病变(包括手术后的增殖性玻璃体视网膜病变),无论是否与糖尿病相关。
在一些变通方案中,当个体(包括但不限于人类个体)处于形成眼睛疾病或病症的高风险下时,将本文所述的制剂和药物制剂用于预防眼睛疾病或病症或者延迟其发作。处于形成眼睛疾病或病症的高风险的个体是具有疾病或病症可能在特定个体中形成的一种或多种适应征的个体。在一些变通方案中,具有形成湿性AMD高风险的个体是在至少一只眼睛中患有干性AMD的个体。在一些变通方案中,具有在对侧眼中形成湿性AMD高风险的个体是在另一只眼睛中患有湿性AMD的个体。在一些变通方案中,将本文所述的制剂和药物制剂用于在形成CNV的高风险个体中预防CNV或延迟其发作,包括但不限于在一只眼睛中患有AMD的个体(包括但不限于人类个体)的对侧眼中预防CNV或延迟其发作。在一些变通方案中,将本文所述的制剂和药物制剂用于在一只眼睛中患有湿性AMD的个体的对侧眼中预防CNV或延迟其发作。在一些变通方案中,制剂和药物制剂包含莫司类化合物,包括但不限于雷帕霉素。在一些变通方案中,将制剂和药物制剂结膜下给药至视力为20/40或更好的眼睛。
在一些变通方案中,将本文所述的制剂和药物制剂用于治疗、预防AMD或延迟其发作。在一些变通方案中,将本文所述的制剂和药物制剂用于治疗、预防干性AMD或延迟其发作。在一些变通方案中,对患有非中枢性地图状萎缩(non-central geographic atrophy)的个体(包括但不限于人类个体)给药本文所述的制剂或药物制剂,以治疗、预防中枢性地图状萎缩或延迟其发作。在一些变通方案中,制剂和药物制剂包含莫司类化合物,包括但不限于雷帕霉素。在一些变通方案中,将制剂和药物制剂结膜下给药至视力为20/40或更好的眼睛。在一些变通方案中,将本文所述的制剂和药物制剂给药,并且所述个体(包括但不限于人类个体)还被用治疗所述疾病或病症的第二种疗法治疗。在一些变通方案中,将本文所述的制剂和药物制剂用于治疗、预防湿性或干性AMD或延迟其发作,且在用本文所述的制剂或药物制剂治疗以前、期间或以后个体(包括但不限于人类个体)还被用激光疗法例如光动力激光疗法治疗。
在一些变通方案中,将本文所述的制剂和药物制剂用于治疗眼葡萄膜炎、变应性结膜炎、黄斑水肿、青光眼或干眼中的一种或多种。
在一些变通方案中,制剂或药物制剂包含莫司类化合物例如雷帕霉素,并且将其给药用于治疗、预防干眼或延迟其发作。在一些变通方案中,制剂或药物制剂包含莫司类化合物例如雷帕霉素,并且将其给药用于治疗、预防变应性结膜炎或延迟其发作。
在一些变通方案中,将本文所述的制剂和药物制剂用于治疗青光眼。在一些变通方案中,用于治疗青光眼的本文所述的制剂和药物制剂包含莫司类化合物例如雷帕霉素,且被用作预防、减少或延迟外科并发症的外科佐药。在一些变通方案中,用于治疗青光眼的本文所述的制剂和药物制剂包含莫司类化合物例如雷帕霉素,且被用于提高或延长外科手术移植的成功。在一些变通方案中,用于治疗青光眼的本文所述的制剂和药物制剂包含莫司类化合物例如雷帕霉素,且被用于提高或延长氩激光小梁切除术或其它青光眼相关的手术的成功。在一些变通方案中,本文所述的制剂和药物制剂具有神经保护作用,并被用于治疗青光眼。
在一些变通方案中,将本文所述的制剂和药物制剂用于治疗色素性视网膜炎。在一些变通方案中,用于治疗青光眼的本文所述的制剂和药物制剂包含莫司类化合物例如雷帕霉素,且被用于治疗、预防色素性视网膜炎或延迟其发作。在一些变通方案中,本文所述的制剂和药物制剂具有神经保护作用,并被用于治疗色素性视网膜炎。
在一些变通方案中,将本文所述的制剂和药物制剂用于治疗视网膜中央静脉闭塞性疾病(CRVO)、分支视网膜静脉闭塞(BRVO)、视网膜血管疾病和病症、黄斑水肿、糖尿病性黄斑水肿、虹膜新生血管形成、糖尿病性视网膜病变、角膜新生血管形成或角膜移植排斥中的一种或多种。在一些变通方案中,制剂或药物制剂包含莫司类化合物例如雷帕霉素,并且将其给药用于治疗、预防一种或多种这些疾病或病症或者延迟其发作。在一些变通方案中,将制剂和药物制剂结膜下给药至视力为20/40或更好的眼睛。
当用于治疗、预防、抑制眼葡萄膜炎、延迟其发作或致使其消退时,可以将本文所述的制剂和药物制剂通过本领域公知的各种途径给药,包括但不限于通过眼睛或口服给药。其它给药途径在本领域中是公知的,并是常规的。在一些变通方案中,本文所述的制剂包含雷帕霉素,且被用于治疗葡萄膜炎。
用本文所述的制剂、液体制剂和方法可以治疗、预防、抑制、延迟发作或致使消退的一种疾病是湿性形式的AMD。在一些变通方案中,将湿性AMD用本文所述的制剂、液体制剂和方法治疗。湿性形式的AMD特征在于:血管从它们在脉络膜的正常位置生长到视网膜下不期望的位置。从这些新血管的渗漏和出血导致视力丧失并可能失明。
本文所述的制剂、液体制剂和方法还可以用于预防或减缓从干性形式的AMD(其中视网膜色素上皮或RPE退化,且导致光感受器细胞死亡和视网膜下的称作玻璃疣的黄色沉着物的形成)到湿性形式的AMD的转变。
“黄斑变性”是以纤维沉着物在斑(macula)和视网膜的过度堆积以及视网膜色素上皮萎缩为特征的。正如本文所用的,将受黄斑变性折磨的眼睛理解为用于指眼睛显示至少一种可检测到的与黄斑变性疾病相关的物理特征。给药雷帕霉素显示使血管发生受到限制和消退,其在没有治疗情况下可能出现,所述血管发生例如是在年龄相关性黄斑变性(AMD)中的脉络膜新生血管形成。正如本文所用的,术语“血管发生”指新的血管产生(“新血管形成”)到组织或器官中。眼睛或视网膜的“血管发生介导的疾病或病症”是其中新的血管以致病的方式在眼睛或视网膜中发生,导致视力降低或丧失或者其它问题(例如与AMD相关的脉络膜新生血管形成)的疾病或病症。
本文所述的制剂和液体制剂(包括但不限于包含雷帕霉素的制剂和液体制剂)还可以用于治疗、预防、抑制下列疾病、延迟其发作或致使其消退,所述疾病是各种免疫相关的疾病和病症,包括但不限于在宿主中的器官移植排斥、移植物抗宿主病、自体免疫疾病;炎症疾病、过度增殖性血管疾病、实体肿瘤、眼瘤和真菌感染。在一些变通方案中,本文所述的制剂和液体制剂(包括但不限于包含雷帕霉素的制剂和液体制剂)还可以用于治疗各种免疫相关的疾病和病症,包括但不限于在宿主中的器官移植排斥、移植物抗宿主病和自体免疫疾病;炎症疾病、过度增殖性血管疾病、实体肿瘤、眼瘤和真菌感染。本文所述的制剂和液体制剂(包括但不限于包含雷帕霉素的制剂和液体制剂)可以用作免疫抑制剂。本文所述的制剂和液体制剂(包括但不限于包含雷帕霉素的制剂和液体制剂)可以用于治疗、预防、抑制移植的器官或组织的排斥或延迟其发作,所述的移植的器官或组织包括但不限于移植的心脏、肝脏、肾、脾、肺、小肠、胰腺和骨髓)。在一些变通方案中,将本文所述的制剂和液体制剂用于治疗移植的器官或组织排斥的发作,所述移植的器官或组织包括但不限于移植的心脏、肝脏、肾、脾、肺、小肠、胰腺和骨髓。当用于治疗、预防、抑制免疫相关疾病(包括但不限于移植排斥)、延迟其发作或致使其消退时,可以将本文所述的制剂和药物制剂通过本领域公知的各种途径给药,包括但不限于通过口服给药。
全身给药可以通过液体制剂的口服给药来实现。其它全身给药途径在本领域是公知的并是常规的。一些它们的示例列在详述部分。
正如本文所用,通过给药治疗物质“抑制”疾病或病症指与没有给药治疗物质的疾病或病症的进展相比,给药治疗物质后,疾病或病症的至少一种可检测到的物理特征或症状的进展被减慢或停止。
正如本文所用,通过给药治疗物质“预防”疾病或病症指给药治疗物质后,疾病或病症的可检测到的物理特征或症状没有形成。
正如本文所用,通过给药治疗物质“延迟疾病或病症发作”指与没有给药治疗物质的疾病或病症的进展相比,给药治疗物质后,疾病或病症的至少一种可检测到的物理特征或症状在时间上更迟地形成。
正如本文所用,通过给药治疗物质“治疗”疾病或病症指与没有给药治疗物质的疾病或病症的进展相比,给药治疗物质后,疾病或病症的至少一种可检测到的物理特征或症状被减慢、停止或逆转。
正如本文所用,通过给药治疗物质“致使疾病或病症消退”指给药治疗物质后,疾病或病症的至少一种可检测到的物理特征或症状的进展在某种程度上被逆转。
具有易患病体质或需要预防的个体(包括但不限于人类个体)可以被熟练的开业医生参考本文所述通过相关领域中已建立的方法和标准鉴别。参考本文所述,熟练的开业医生也可以根据在鉴别血管发生和/或新生血管形成的领域中已建立的标准容易地诊断需要抑制或治疗的个体。
正如本文所用,“个体”通常是可以从本文所述的治疗物质的给药获益的任何动物。在一些变通方案中,将治疗物质给药至哺乳动物个体。在一些变通方案中,将治疗物质给药至人类个体。在一些变通方案中,可以将治疗物质给药至兽医的动物个体。在一些变通方案中,可以将治疗物质给药至模型实验的动物个体。
用本文所述的方法可以治疗、预防、抑制、延迟发作或致使消退的其它疾病和病症包括公开在以下专利和出版物中的那些,将其各自以全部内容引入文中作为参考:2004年4月1日公开的PCT公开文本WO2004/027027,题目为“抑制脉络膜新生血管形成的方法”,转让给宾西法尼亚大学的托管人;1995年2月7日授权的US专利号5,387,589,题目为“治疗眼睛炎症的方法”,发明人Prassad Kulkarni,转让给路易斯维尔大学研究基金会;2003年4月23日授权的US专利号6,376,517,题目为“用于视觉和记忆障碍的2-哌啶酸衍生物”,转让给GPI NIL控股有限公司(GPI NIL Holdings,Inc);2004年4月8日公开的PCT公开文本WO2004/028477,题目为“:包含甾体类的治疗物质的视网膜下给药方法:使药效学作用定位于脉络膜和视网膜的方法;以及治疗和/或预防视网膜疾病的相关方法”,转让给伊诺克斯公司(Innorx,Inc);2002年7月9日授权的美国专利号6,416,777,题目为“眼科药物递送装置”,转让给爱尔康全球有限公司(Alcon Universal Ltd);2004年3月30日授权的美国专利号6,713,081,题目为“眼科治疗物质递送装置及制造和使用这些装置的方法”,转让给卫生和健康服务部;1996年7月16日授权的美国专利号5,536,729,题目为“用于眼科给药的雷帕霉素制剂(Rapamycin Formulations for OralAdministration)”,转让给美国家庭用品公司(American Home ProductsCorp)。
给药途径
本文所述的制剂、方法和液体制剂将一种或多种治疗物质递送到个体,包括但不限于人类个体。
在一些变通方案中,本文所述的制剂、方法和液体制剂将一种或多种治疗物质递送到个体(包括但不限于人类个体)的含水介质中。
在一些变通方案中,本文所述的制剂、方法和液体制剂将一种或多种治疗物质递送到要被治疗、预防、抑制、延迟发作或致使消退的疾病或病症所在区域或与之接近区域的含水介质中。
液体制剂通常可以以具有期望效果的任何体积给药;在一些变通方案中,将液体制剂给药至玻璃体,且液体制剂小于玻璃体体积的一半。在一些变通方案中,将液体制剂以小于约50μl的体积给药至巩膜和结膜之间。
当将某一体积给药时,应当理解,可以用于给药液体制剂的各种注射器的准确度有一定的不精确性。在某一体积是特定的时,应当理解,这是目标体积。然而,某些注射器例如胰岛素注射器不准确性大于10%,且有时不准确性高达20%或更多。通常认为Hamilton HPLC型注射器精确到10%范围内,且被推荐用于10μl以下体积。
在一些变通方案中,将一定体积的本文所述液体制剂给药至兔眼睛或个体眼睛的玻璃体,所述体积小于约200μl、小于约100μl、小于约90μl、小于约80μl、小于约70μl、小于约60μl、小于约50μl、小于约40μl、小于约30μl、小于约20μl、小于约10μl、小于约5μl、小于约3μl或小于约1μl。在一些变通方案中,将小于约20μl体积的本文所述液体制剂给药至兔眼睛或个体眼睛的玻璃体。在一些变通方案中,将小于约10μl体积的本文所述液体制剂给药至玻璃体。在一些变通方案中,将一定体积的本文所述液体制剂给药至兔眼睛或个体眼睛的玻璃体,所述体积是约0.1μl至约200μl、约50μl至约200μl、约50μl至约150μl、约0.1μl至约100μl、约0.1μl至约50μl、约1μl至约40μl、约1μl至约30μl、约1μl至约20μl、约1μl至约10μl或约1μl至约5μl。在一些变通方案中,将约1μl至约10μl体积的本文所述液体制剂给药至兔眼睛或个体眼睛的玻璃体。在一些变通方案中,将约1μl至约5μl体积的本文所述液体制剂给药至兔眼睛或个体眼睛的玻璃体。在一些变通方案中,将约1μl至约5μl体积的本文所述液体制剂给药至兔眼睛或个体眼睛的玻璃体。在一些变通方案中,将约0.1μl至约200μl体积的本文所述液体制剂给药至兔眼睛或个体眼睛的玻璃体。
在一些变通方案中,将一定总体积的本文所述液体制剂结膜下给药至兔眼睛或个体眼睛,所述总体积是小于约1000μl、小于约600μl、小于约500μl、小于约400μl、小于约200μl、小于约100μl、小于约90μl、小于约80μl、小于约70μl、小于约60μl、小于约50μl、小于约40μl、小于约30μl、小于约20μl、小于约10μl、小于约5μl、小于约3μl或小于约1μl的总体积。在一些变通方案中,将小于约20μl体积的本文所述液体制剂结膜下给药至兔眼睛或个体眼睛。在一些变通方案中,将小于约10μl体积的本文所述液体制剂结膜下给药至兔眼睛或个体眼睛。在一些变通方案中,将一定体积的本文所述液体制剂结膜下给药至兔眼睛或个体眼睛,所述体积为约0.1μl至约200μl、约50μl至约200μl、约100μl至约300μl、约300μl至约400μl、约400μl至约500μl、约500μl至约1000μl、约50μl至约150μl、约0.1μl至约100μl、约0.1μl至约50μl、约1μl至约40μl、约1μl至约30μl、约1μl至约20μl、约1μl至约10μl或约1μl至约5μl。在一些变通方案中,将约1μl至约10μl体积的本文所述液体制剂结膜下给药至兔的眼睛或个体的眼睛。在一些变通方案中,将约1μl至约5μl体积的本文所述液体制剂结膜下给药至兔的眼睛或个体的眼睛。在一些变通方案中,将约1μl至约5μl体积的本文所述液体制剂结膜下给药至兔的眼睛或个体的眼睛。在一些变通方案中,将约0.1μl至约200μl体积的本文所述液体制剂结膜下给药至兔的眼睛或个体的眼睛。
在一些变通方案中,本文所述的液体制剂包含不大于约250μl的聚乙二醇。在一些变通方案中,本文所述的液体制剂包含不大于约250μl、不大于约200μl、不大于约150μl、不大于约125μl、不大于约100μl、不大于约75μl、不大于约50μl、不大于约25μl、不大于约20μl、不大于约15μl、不大于约10μl、不大于约7.5μl、不大于约5μl、不大于约2.5μl、不大于约1.0μl、不大于约0.5μl的聚乙二醇。包含聚乙二醇的制剂可以包含例如PEG 300或PEG 400。
在一些变通方案中,将本文所述的液体制剂各自在一段时间内(包括但不限于在一小时内)于多处结膜下的区域给药。不受理论限制,认为由于局部眼组织的吸收较大体积的潜在受限能力,所以,与单剂量相比,所述多次给药例如多次注射,能使更大的总剂量结膜下给药。
在一些变通方案中,本文所述的制剂、方法和液体制剂以一定量和持续时间将一种或多种治疗物质递送到个体的眼睛包括斑和视网膜脉络膜组织,所述量和持续时间是有效治疗、预防、抑制在疾病和病症部分所述的疾病和病症、延迟其发作或致使其消退的量和持续时间。
正如本文所用,“视网膜脉络膜”和“视网膜脉络膜组织”是同义词,指眼睛的视网膜和脉络膜组织的组合。
正如本文所用,“结膜下”放置或注射指在巩膜和结膜之间放置或注射。
作为非限制性示例,本文所述的制剂、液体制剂和方法可以以一定量和持续时间给药至玻璃体、眼房水、巩膜、结膜、巩膜和结膜之间、视网膜脉络膜组织、斑或个体眼睛或与之接近的其它区域,所述给药通过直接给药至这些组织或通过眼周途径给药,所述量和持续时间是有效治疗、预防、抑制CNV和湿性AMD、延迟其发作或致使其消退的量和持续时间。其它到达靶组织的非限制性给药途径包括但不限于玻璃体内、前房内和眼周途径。对于治疗、预防、抑制CNV和湿性AMD、延迟其发作或致使其消退中的每一种和递送的每一不同位置而言,有效的量和持续时间可以是不同的。
与一些其它类型的眼睛操作相比,玻璃体内给药是更具侵害性的。因为潜在的副作用风险,对于治疗相对健康的眼睛而言,玻璃体内给药不是最佳的。比较而言,眼周给药例如结膜下给药比玻璃体内给药的侵害性要小得多。当治疗物质通过眼周途径递送时,治疗具有比可以用玻璃体内给药治疗的更健康的眼睛的患者可能是可行的。在一些变通方案中,当个体眼睛具有20/40或更好的视力时,结膜下注射用于预防眼睛疾病或病症或者延迟其发作。
可以用于给药液体制剂的给药途径包括但不限于将液体制剂置入(例如通过注射)个体的含水介质中,包括但不限于置入(例如通过注射)个体的眼睛中。液体制剂可以全身给药,包括但不限于下面的给药途径:直肠、阴道、输注、肌内、腹膜内、动脉内、鞘内、支气管内、脑池内、皮肤、皮下、真皮内、经皮、静脉、颈内、腹内、颅内、眼内、肺内、胸内、气管内、鼻、颊、舌下、口服、肠胃外或喷雾或采用气雾抛射剂的气雾化给药。在一些变通方案中,将自乳化制剂结膜下给药。在一些变通方案中,将自乳化制剂玻璃体内给药。
包含治疗物质的组合物和液体制剂可以通过各种方法直接给药至眼睛,包括但不限于如下方法,其中(1)采用注射器和皮下针通过注射给药治疗物质;(2)用特别设计的装置注射治疗物质;(3)注射治疗物质前,通过外科手术在巩膜内形成囊,以便作为治疗物质或治疗物质组合物的容器。例如,在一种给药方法中,外科医生在眼睛的巩膜内造成一个囊,接着将包含治疗物质的溶液或液体制剂注射到囊中。
其它给药方法包括但不限于如下方法,其中,(1)通过特别设计的弯曲的套管注射治疗物质的制剂,以便直接将治疗物质置于靠近眼睛的部位;(2)将压制形式的治疗物质直接置于靠近眼睛的部位;(3)通过特别设计的注射器或插入器,将治疗物质插进巩膜中;(4)将包含治疗物质的液体制剂混合到聚合物里;(5)外科医生造出一个小的结膜切口,通过切口穿过缝合线和任何治疗物质递送结构(structure),以便将所述结构缝合至靠近巩膜处;(6)将针直接插进眼睛的玻璃体中或插到任何其它上述位置,用于注射。
本文所述的液体制剂可以通过注射使用,作为酏剂,用于局部给药,包括但不限于通过滴眼剂或其它方法局部给药至眼睛。在一些变通方案中,本文所述的液体制剂是在硬明胶或软明胶或淀粉胶囊中。胶囊可以被绑扎,例如用于防止渗漏。
可以用于递送本文所述的制剂和液体制剂的一些变通方案是通过注射递送。在该方法中,可以将制剂和液体制剂注射到个体中或注射到个体眼睛中的或与个体眼睛接近的位置,用于递送到个体或个体的眼睛中。个体眼睛中的或与个体眼睛接近的位置的非限制性示例如下。
注射治疗物质到玻璃体中可以在玻璃体和视网膜中提供治疗物质的高的局部浓度。另外,发现在玻璃体中药物的清除半衰期随着分子量而增加。
前房内注射或注入到它们眼睛的前房的注射也可以被使用。在一个示例中,可以前房内注射高达约100μl。
眼周途径递送可以递送治疗物质到视网膜,而没有玻璃体内递送的一些风险。眼周途径包括但不限于结膜下、眼睛筋膜囊下、眼球后、眼球周或后部巩膜旁递送。给药的“眼周”途径指置于眼睛的附近或周围,对于视网膜药物递送的眼周途径的示例性描述而言,参见视网膜药物递送的眼周途径(Periocular routes or retinal drug delivery),Raghava等人(2004),药物递送的专家观点(Expert Opin.Drug Deliv.),1(1):99-114,将其以全部内容引入文中作为参考。
在一些变通方案中,将本文所述的液体制剂眼内给药。眼内给药包括在眼睛内,包括在玻璃体内的放置或注射。
结膜下注射可以是在结膜下或者在巩膜和结膜之间注射治疗物质。在一个示例中,可以结膜下注射高达约500μl。作为一个非限制性示例,可以使用高达约25至约30号和约30mm长的针。对治疗物质给药的结膜下位置的局部压力通过减少局部脉络膜血流可以提高治疗物质至后段的递送。
眼筋膜囊下注射可以是将治疗物质注射到环绕在眼睛上面部分的眼球筋膜里和注射到上直肌的凸起中。在一个示例中,可以眼筋膜囊下注射高达约4ml。作为一个非限制性示例,可以使用约2.5cm长的钝头套管。
眼球后注射指注射到在眼球后面的四块直肌肌肉和它们的肌间隔膜的圆锥室里。在一个示例中,可以眼球后注射高达约5ml。作为一个非限制性示例,可以使用约25号或约27号的钝头针。
眼球周注射可以是在四块直肌肌肉和它们的肌间隔膜的范围外部的位置,即肌肉圆锥的外面。可以眼球周注射例如高达约10ml的体积。作为一个非限制性示例,可以使用约1.25英寸长和约25号的钝头套管。
后部巩膜旁递送指将治疗物质置于斑的周围和上面,直接与巩膜的外表面接触,且没有穿刺眼球。在一个示例中,可以后部巩膜旁注射高达约500ml。作为一个非限制性示例,将钝头弯曲的套管(尤其设计成56°的)用于将治疗物质置于巩膜的切口处。
对于用于视网膜药物递送的通过眼周途径的示例性注射方法的描述,参见视网膜药物递送的眼周途径,Raghava等人(2004),药物递送的专家观点,1(1):99-114,将其以全部内容引入文中作为参考。
制剂和液体制剂可以给药的位置包括但不限于玻璃体、眼房水、巩膜、结膜、巩膜和结膜之间、视网膜脉络膜组织、斑或其它眼周部位。可以用于制剂和液体制剂的放置的方法包括但不限于注射。
在一些可以使用的变通方案中,将治疗物质溶解在溶剂或溶剂混合物中,然后根据任何一种上述方法,注射到玻璃体、眼房水、巩膜、结膜、巩膜和结膜之间、视网膜脉络膜组织、斑中或它们附近、个体眼睛中的其它部位或接近个体眼睛的部位、或者个体的其它介体中。在一个可以被使用的所述方法中,治疗物质是在液体制剂中的雷帕霉素。在一些变通方案中,液体制剂是原位胶化制剂。
当治疗物质是雷帕霉素时,可以将组合物和液体制剂用于在眼睛组织中递送或维持一定量的雷帕霉素,所述眼睛组织没有限制地包括视网膜、脉络膜或玻璃体,所述雷帕霉素的量对治疗AMD是有效的。在一个非限制性示例中,认为以能够在玻璃体中提供约0.01pg/ml至约2μg/ml浓度的雷帕霉素的量递送雷帕霉素的液体制剂可以用于治疗湿性AMD。在另一个非限制性示例中,认为在视网膜脉络膜组织中递送约0.01pg/ml至约1μg/ml浓度的雷帕霉素的液体制剂可以用于治疗湿性AMD。其它有效浓度由本领域技术人员根据本文所述可以容易地确定。
可以将本文所述的制剂和液体制剂递送到能够递送治疗物质的眼睛部位的各种位置,包括但不限于眼内或眼周递送;递送到玻璃体、眼房水、巩膜、结膜、巩膜和结膜之间、视网膜脉络膜组织、斑、眼周组织、眼球筋膜区域、和个体眼睛中的或与个体眼睛接近的其它区域、或者其它环境。其它递送位置和给药途径例如全身途径如上所述。
包含治疗物质的制剂和液体制剂可以用各种方法直接给药到眼睛,包括但不限于如下方法,其中,(1)采用注射器和皮下针通过注射给药治疗物质;(2)用特别设计的装置注射治疗物质;(3)注射治疗物质前,通过外科手术在巩膜内形成囊,以便作为治疗物质或治疗物质制剂的容器。例如,在一种给药方法中,外科医生在眼睛的巩膜内造成一个囊,接着将包含治疗物质的溶液或液体制剂注射到囊中。
其它给药方法包括但不限于如下方法,其中,(1)通过特别设计的弯曲的套管注射治疗物质的制剂,以便直接将治疗物质置于靠近眼睛的部位;(2)将压制形式的治疗物质直接置于靠近眼睛的部位;(3)通过特别设计的注射器或插入器,将治疗物质插进巩膜中;(4)将包含治疗物质的液体制剂混合到聚合物里;(5)外科医生造出一个小的结膜切口,通过切口穿过缝合线和任何治疗物质递送结构,以便将所述结构缝合至靠近巩膜处;(6)将针直接插进眼睛的玻璃体中或插到任何其它上述位置,用于注射。
用于治疗、预防、抑制AMD、延迟其发作或致使其消退的雷帕霉素的玻璃体内和结膜下递送
在本文所述的一些变通方案中,将包含雷帕霉素的稳定制剂结膜下递送或递送到个体(包括但不限于人类个体)眼睛的玻璃体中,以预防、治疗、抑制眼睛中的血管发生、延迟其发作或致使其消退,包括但不限于治疗例如在AMD中观察到的CNV。在一些变通方案中,稳定制剂用于治疗眼睛中的血管发生,包括但不限于治疗例如在AMD中观察到的CNV。雷帕霉素已经显示出在兔子和小鼠模型中抑制CNV,正如在U.S.申请号10/665,203中所述,将其以全部内容引入文中作为参考。当被全身和视网膜下给药时,雷帕霉素已被观察到抑制基质胶(MatrigelTM)和激光诱导的CNV。
可以被递送到眼睛(包括但不限于眼睛的玻璃体)用于治疗、预防、抑制眼睛的血管发生(例如CNV)、延迟其发作或致使其消退的其它治疗物质是除雷帕霉素外的莫司类化合物成员,包括但不限于依维莫司和他克莫司(FK-506)。
正如本文所述,治疗物质的剂量取决于所述的病症(不论病症是要被治疗、预防、抑制、延迟发作,还是被致使消退)、具体的治疗物质和其它临床因素例如个体的重量和情况以及治疗物质的给药途径。应当理解,本文所述的方法、包括原位胶化制剂的液体制剂和制剂可用于人类使用和兽用,包括但不限于实验室动物、实验动物、宠物或农业上重要的动物。如本文所述,用质量/体积的单位表示的治疗物质的组织浓度通常涉及主要是眼房水的组织例如玻璃体。用质量/质量的单位表示的治疗物质的组织浓度通常涉及其它组织,例如巩膜或视网膜脉络膜组织。
在本文所述的方法中可以使用的雷帕霉素的一种浓度是其在组织水平提供给个体约0.01pg/ml或pg/mg或更多的雷帕霉素的浓度。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约0.1pg/ml或pg/mg或更多。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约1pg/ml或pg/mg或更多。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约0.01ng/ml或ng/mg或更多。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约0.1ng/ml或ng/mg或更多。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约0.5ng/ml或ng/mg或更多。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约1ng/ml或ng/mg或更多。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约2ng/ml或ng/mg或更多。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约3ng/ml或ng/mg或更多。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约5ng/ml或ng/mg或更多。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约10ng/ml或ng/mg或更多。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约15ng/ml或ng/mg或更多。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约20ng/ml或ng/mg或更多。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约30ng/ml或ng/mg或更多。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约50ng/ml或ng/mg或更多。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约100ng/ml或ng/mg或更多。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约200ng/ml或ng/mg或更多。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约300ng/ml或ng/mg或更多。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约400ng/ml或ng/mg或更多。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约500ng/ml或ng/mg或更多。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约1μg/ml或μg/mg或更多。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约1.5μg/ml或μg/mg或更多。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约2μg/ml或μg/mg或更多。可以使用的另一种浓度是该种浓度:其在组织水平提供给个体约5μg/ml或μg/mg或更多。在一些变通方案中,所述组织是玻璃体。在一些变通方案中,所述组织是视网膜脉络膜。在一些变通方案中,所述组织是巩膜。参照本文所述,根据所用的给药途径和持续时间,本领域普通技术人员将知道如何达到合适的浓度。
通常来说,以液体制剂给药的雷帕霉素的量是足以在所需时间内治疗、预防、抑制眼睛疾病或病症、延迟其发作或致使其消退的量。在一些变通方案中,以液体制剂给药的雷帕霉素的量是足以在所需或指定时间内治疗眼睛疾病或病症的量。
在一些变通方案中,将总量小于约5mg的雷帕霉素结膜下给药。在一些变通方案中,将总量小于约5.0mg的雷帕霉素结膜下给药。在一些变通方案中,将总量小于约4.5mg的雷帕霉素结膜下给药。在一些变通方案中,将总量小于约4.0mg的雷帕霉素结膜下给药。在一些变通方案中,将总量小于约3.5mg的雷帕霉素结膜下给药。在一些变通方案中,将总量小于约3.0mg的雷帕霉素结膜下给药。在一些变通方案中,将总量小于约2.5mg的雷帕霉素结膜下给药。在一些变通方案中,将总量小于约2mg的雷帕霉素结膜下给药。在一些变通方案中,将总量小于约1.2mg的雷帕霉素结膜下给药。在一些变通方案中,将总量小于约1.0mg的雷帕霉素结膜下给药。在一些变通方案中,将总量小于约0.8mg的雷帕霉素结膜下给药。在一些变通方案中,将总量小于约0.6mg的雷帕霉素结膜下给药。在一些变通方案中,将总量小于约0.4mg的雷帕霉素结膜下给药。在一些变通方案中,将一定体积的制剂给药,所述体积包含本文所述量的雷帕霉素。
在一些变通方案中,将总量小于约200μg的雷帕霉素玻璃体内给药。在一些变通方案中,将总量小于约200μg的雷帕霉素玻璃体内给药。在一些变通方案中,将总量小于约300μg的雷帕霉素玻璃体内给药。在一些变通方案中,将总量小于约400μg的雷帕霉素玻璃体内给药。在一些变通方案中,将总量小于约500μg的雷帕霉素玻璃体内给药。在一些变通方案中,将总量小于约600μg的雷帕霉素玻璃体内给药。在一些变通方案中,将总量小于约800μg的雷帕霉素玻璃体内给药。在一些变通方案中,将总量小于约1mg的雷帕霉素玻璃体内给药。在一些变通方案中,将总量小于约2mg的雷帕霉素玻璃体内给药。在一些变通方案中,将总量小于约2.5mg的雷帕霉素玻璃体内给药。在一些变通方案中,将总量小于约3mg的雷帕霉素玻璃体内给药。在一些变通方案中,将总量小于约3.5mg的雷帕霉素玻璃体内给药。在一些变通方案中,将总量小于约4mg的雷帕霉素玻璃体内给药。在一些变通方案中,将一定体积的制剂给药,所述体积包含本文所述量的雷帕霉素。
在一些变通方案中,将包含约1μg至约5mg量的雷帕霉素的如本文所述的稳定制剂给药至人类个体用于治疗湿性AMD。在一些变通方案中,将包含约20μg至约4mg量的雷帕霉素的如本文所述的稳定制剂给药至人类个体用于治疗湿性AMD。在一些变通方案中,将包含约20μg至约1.2mg量的雷帕霉素的如本文所述的液体制剂给药至人类个体用于治疗湿性AMD。在一些变通方案中,将约10μg至约0.5mg量的雷帕霉素给药至人类个体用于治疗湿性AMD。在一些变通方案中,将约10μg至约90μg量的雷帕霉素给药至人类个体用于治疗湿性AMD。在一些变通方案中,将约60μg至约120μg量的雷帕霉素给药至人类个体用于治疗湿性AMD。在一些变通方案中,将约100μg至约400μg量的雷帕霉素给药至人类个体用于治疗湿性AMD。在一些变通方案中,将约400μg至约1mg量的雷帕霉素给药至人类个体用于治疗湿性AMD。在一些变通方案中,将约1mg至约5mg量的雷帕霉素给药至人类个体用于治疗湿性AMD。在一些变通方案中,将约3mg至约7mg量的雷帕霉素给药至人类个体用于治疗湿性AMD。在一些变通方案中,将约5mg至约10mg量的雷帕霉素给药至人类个体用于治疗湿性AMD。
在一些变通方案中,将包含约1μg至约5mg量的雷帕霉素的如本文所述的稳定制剂给药至人类个体用于预防湿性AMD。在一些变通方案中,将包含约20μg至约4mg量的雷帕霉素的如本文所述的稳定制剂给药至人类个体用于预防湿性AMD。在一些变通方案中,将包含约20μg至约1.2mg量的雷帕霉素的如本文所述的液体制剂给药至人类个体用于预防湿性AMD。在一些变通方案中,将约10μg至约0.5mg量的雷帕霉素给药至人类个体用于预防湿性AMD。在一些变通方案中,将约10μg至约90μg量的雷帕霉素给药至人类个体用于预防湿性AMD。在一些变通方案中,将约60μg至约120μg量的雷帕霉素给药至人类个体用于预防湿性AMD。在一些变通方案中,将约100μg至约400μg量的雷帕霉素给药至人类个体用于预防湿性AMD。在一些变通方案中,将约400μg至约1mg量的雷帕霉素给药至人类个体用于预防湿性AMD。在一些变通方案中,将约1mg至约5mg量的雷帕霉素给药至人类个体用于预防湿性AMD。在一些变通方案中,将约3mg至约7mg量的雷帕霉素给药至人类个体用于预防湿性AMD。在一些变通方案中,将约5mg至约10mg量的雷帕霉素给药至人类个体用于预防湿性AMD。
在一些变通方案中,将包含约1μg至约5mg量的雷帕霉素的如本文所述的稳定制剂给药至人类个体用于治疗干性AMD。在一些变通方案中,将包含约20μg至约4mg量的雷帕霉素的如本文所述的稳定制剂给药至人类个体用于治疗干性AMD。在一些变通方案中,将包含约20μg至约1.2mg量的雷帕霉素的如本文所述的液体制剂给药至人类个体用于治疗干性AMD。在一些变通方案中,将约10μg至约0.5mg量的雷帕霉素给药至人类个体用于治疗干性AMD。在一些变通方案中,将约10μg至约90μg量的雷帕霉素给药至人类个体用于治疗干性AMD。在一些变通方案中,将约60μg至约120μg量的雷帕霉素给药至人类个体用于治疗干性AMD。在一些变通方案中,将约100μg至约400μg量的雷帕霉素给药至人类个体用于治疗干性AMD。在一些变通方案中,将约400μg至约1mg量的雷帕霉素给药至人类个体用于治疗干性AMD。在一些变通方案中,将约1mg至约5mg量的雷帕霉素给药至人类个体用于治疗干性AMD。在一些变通方案中,将约3mg至约7mg量的雷帕霉素给药至人类个体用于治疗干性AMD。在一些变通方案中,将约5mg至约10mg量的雷帕霉素给药至人类个体用于治疗干性AMD。
在一些变通方案中,将包含约1μg至约5mg量的雷帕霉素的如本文所述的液体制剂给药至人类个体用于治疗血管发生,包括但不限于脉络膜新生血管形成。在一些变通方案中,将约20μg至约4mg量的雷帕霉素给药至人类个体;将约20μg至约1.2mg、约10μg至约0.5mg给药至人类个体用于治疗湿性AMD;将约10μg至90μg、约60μg至120μg给药至人类个体;将约100μg至400μg、约400μg至1mg给药至人类个体;在一些变通方案中,将约1mg至5mg量的雷帕霉素给药至人类个体;在一些变通方案中,将约3mg至7mg量的雷帕霉素给药至人类个体;在一些变通方案中,将约5mg至10mg量的雷帕霉素给药至人类个体用于治疗血管发生,包括但不限于脉络膜新生血管形成。
在一些变通方案中,如本文所述的液体制剂包含与雷帕霉素的量相当的治疗物质的量。在一些变通方案中,将包含相当于约1μg至约5mg量的雷帕霉素的量的治疗物质的如本文所述的液体制剂给药至人类个体用于治疗湿性AMD。在一些变通方案中,将相当于约1μg至约5mg量的雷帕霉素的量的治疗物质给药至人类个体;将约20μg至约1.2mg、约10μg至约0.5mg给药至人类个体用于治疗湿性AMD;将约10μg至90μg、约60μg至120μg给药至人类个体;将约100μg至400μg、约400μg至1mg给药至人类个体;在一些变通方案中,将相当于约1mg至5mg量的雷帕霉素的量的治疗物质给药至人类个体;在一些变通方案中,将相当于约3mg至7mg量的雷帕霉素的量的治疗物质给药至人类个体;在一些变通方案中,将相当于约5mg至10mg量的雷帕霉素的量的治疗物质给药至人类个体。
在一些变通方案中,将包含相当于约1μg至约5mg量的雷帕霉素的量的治疗物质的如本文所述的液体制剂给药至人类个体用于治疗干性AMD。在一些变通方案中,将相当于约20μg至约4mg量的雷帕霉素的量的治疗物质给药至人类个体;将约20μg至约1.2mg、约10μg至约0.5mg给药至人类个体用于治疗湿性AMD;将约10μg至90μg、约60μg至120μg给药至人类个体;将约100μg至400μg、约400μg至1mg给药至人类个体;在一些变通方案中,将相当于约400μg至1mg量的雷帕霉素的量的治疗物质给药至人类个体;在一些变通方案中,将相当于约1mg至5mg量的雷帕霉素的量的治疗物质给药至人类个体;在一些变通方案中,将相当于约3mg至7mg量的雷帕霉素的量的治疗物质给药至人类个体;在一些变通方案中,将相当于约5mg至10mg量的雷帕霉素的量的治疗物质给药至人类个体用于治疗干性AMD。
在一些变通方案中,将包含相当于约1μg至约5mg量的雷帕霉素的量的治疗物质的如本文所述的液体制剂给药至人类个体用于预防湿性AMD。在一些变通方案中,将相当于约20μg至约4mg量的雷帕霉素的量的治疗物质给药至人类个体;将约20μg至约1.2mg、约10μg至约0.5mg给药至人类个体用于预防湿性AMD;将约10μg至90μg、约60μg至120μg给药至人类个体;将约100μg至400μg、约400μg至1mg给药至人类个体;在一些变通方案中,将相当于约400μg至1mg量的雷帕霉素的量的治疗物质给药至人类个体;在一些变通方案中,将相当于约1mg至5mg量的雷帕霉素的量的治疗物质给药至人类个体;在一些变通方案中,将相当于约3mg至7mg量的雷帕霉素的量的治疗物质给药至人类个体;在一些变通方案中,将相当于约5mg至10mg量的雷帕霉素的量的治疗物质给药至人类个体用于预防湿性AMD。
在一些变通方案中,将包含相当于约20μg至约10mg量的雷帕霉素的量的治疗物质的如本文所述的液体制剂给药至人类个体用于治疗血管发生,包括但不限于脉络膜新生血管形成。在一些变通方案中,将相当于约30μg至约9mg量的雷帕霉素的量的治疗物质给药至人类个体;在一些变通方案中,将相当于约10μg至90μg量的雷帕霉素的量的治疗物质给药至人类个体;在一些变通方案中,将相当于约60μg至120μg量的雷帕霉素的量的治疗物质给药至人类个体;在一些变通方案中,将相当于约100μg至400μg量的雷帕霉素的量的治疗物质给药至人类个体;在一些变通方案中,将相当于约400μg至1mg量的雷帕霉素的量的治疗物质给药至人类个体;在一些变通方案中,将相当于约1mg至5mg量的雷帕霉素的量的治疗物质给药至人类个体;在一些变通方案中,将相当于约3mg至7mg量的雷帕霉素的量的治疗物质给药至人类个体;在一些变通方案中,将相当于约5mg至10mg量的雷帕霉素的量的治疗物质给药至人类个体。
在一些变通方案中,将本文所述的制剂中的任何一种或多种每3个或更多个月、每6个或更多个月、每9个或更多个月或者每12个或更多个月或者更长时间进行玻璃体内给药,用于治疗脉络膜新生血管形成、湿性AMD、干性AMD中的一种或多种或者用于预防湿性AMD。在一些变通方案中,将本文所述的制剂中的任何一种或多种每3个或更多个月、每6个或更多个月、每9个或更多个月或者每12个或更多个月或者更长时间进行结膜下给药,用于治疗脉络膜新生血管形成、湿性AMD、干性AMD中的一种或多种或者用于预防湿性AMD。
在一些变通方案中,将本文所述的雷帕霉素制剂中的任何一种或多种每3个或更多个月、每6个或更多个月、每9个或更多个月或者每12个或更多个月或者更长时间进行玻璃体内给药,用于治疗脉络膜新生血管形成、湿性AMD、干性AMD中的一种或多种或者用于预防湿性AMD。在一些变通方案中,将本文所述的雷帕霉素制剂中的任何一种或多种每3个或更多个月、每6个或更多个月、每9个或更多个月或者每12个或更多个月或者更长时间进行结膜下给药,用于治疗脉络膜新生血管形成、湿性AMD、干性AMD中的一种或多种或者用于预防湿性AMD。在一些变通方案中,雷帕霉素的作用持续超过它用LCMS在眼组织中可测量的时期。
根据给药的途径和持续时间,本文所述的治疗物质的递送可以例如以约1ng/天至约100μg/天的剂量或者以高于或低于这个范围的剂量递送。在本文所述方法中使用的液体制剂或制剂的一些变通方案中,治疗物质以约0.1μg/天至约10μg/天的剂量递送;在本文所述方法中使用的稳定制剂的一些变通方案中,治疗物质以约1μg/天至约5μg/天的剂量递送。用于治疗、预防、抑制本文所述的各种疾病和病症、延迟其发作或致使其消退的各种治疗物质的剂量可以利用临床实验进行精缩(refine)。
当将治疗有效量的雷帕霉素给药至患有湿性AMD的个体时,雷帕霉素可以治疗、抑制湿性AMD或致使其消退。对于治疗、抑制或致使消退而言,可能需要不同的治疗有效量。患有湿性AMD的个体可能具有CNV损害,且不受理论限制,认为给药治疗有效量的雷帕霉素可能具有多种作用,包括但不限于致使CNV损害消退、稳定CNV损害和预防活跃的CNV损害的进展。
当将治疗有效量的雷帕霉素给药至患有干性AMD的个体时,认为雷帕霉素可以预防或减缓干性AMD到湿性AMD的进展。
实施例
当乙醇被使用时,它是来自Gold Shield Distributors,Hayward,CA的100%乙醇。当雷帕霉素被使用时,它来自LC实验室(LC laboratories),Woburn,MA或者中化合成生技有限公司(Chunghwa Chemical Synthesis&Biotech Co.,LTD)(CCSB)Taipei Hsien,Taiwan,ROC。当PEG 400被使用时,它来自陶氏化学公司(Dow Chemical Company),New Milford,CT。
实施例1-通过超声制备包含雷帕霉素的溶液
通过超声将雷帕霉素溶解于100%乙醇中。将过量乙醇通过强制蒸发除去。将PEG 400超声。将雷帕霉素-乙醇溶液加到PEG 400中,将混合物超声直至形成溶液。使用超声,以便使混合物的温度在很长时间内不超过40℃。作为最终制剂重量百分比的终浓度大约是雷帕霉素2%w/w、乙醇4%w/w和PEG 40094%w/w。将溶液通过0.2微米的滤器过滤灭菌。
将2ml透明玻璃小瓶填装2ml的上述经过滤的溶液,使每个容器顶空剩余高达约400μl。将2ml琥珀色玻璃小瓶填装0.5ml经过滤的溶液,使每个容器顶空剩余高达约1900μl。
将结果显示在表1中。对每种小瓶构成(configuration)进行分析,每种小瓶构成在表1中有一个编号。通常每种小瓶构成有2-3个重复(replicates)。通常每种小瓶构成的重复的3个样品通过标准HPLC进行分析。
当将0.5ml制剂置于2ml琥珀色玻璃小瓶中时,在25摄氏度放置1个月后,相对于制剂中的雷帕霉素的起始量,制剂的雷帕霉素水平减少约29%。当将0.5ml制剂置于2ml琥珀色玻璃小瓶中时,在5摄氏度放置1、2、3和6个月后,相对于在制剂中的雷帕霉素的起始量,制剂的雷帕霉素水平减少约5.2%、14%、22.3%和26.7%。当将0.5ml制剂置于2ml琥珀色玻璃瓶中时,在-20摄氏度放置1、2、3和6个月后,相对于在制剂中的雷帕霉素的起始量,制剂的雷帕霉素水平减少约1.2%、5.1%、8.8%和21.5%。不受理论限制,认为治疗物质的这种减少的水平部分是由相对于制剂体积的大的顶空体积以及琥珀色玻璃的组分引起的。琥珀色玻璃含有已知可氧化对氧化作用敏感的成剂的组分,例如金属。
当将2ml制剂置于2ml透明玻璃瓶中时,在25摄氏度放置1、2和3个月后,相对于在制剂中的雷帕霉素的起始量,制剂的雷帕霉素水平分别减少约3%、4%和9%。
有本领域技术人员公知的标准化的转换,通过该转换,贮存在升高的温度下的制剂或制剂中治疗物质的稳定性可预示贮存在较低温度下的制剂或制剂中的治疗物质的稳定性。该转换是基于ICH协调性三方指南(ICHHarmonized Tripartite Guideline)“新原料药和产品的稳定性试验Q1A(R2)(Stability Testing of New Drug Substances and ProductsQ1A(R2))”。根据这个指南,在25℃贮存一段时间预示在5℃下在两倍的这段时间内制剂或治疗物质是稳定的。还参见药物稳定性、原理和实践(Drug Stability,Principles and Practices),第三版,Jens T.Cartensen,ChrisT.Rhodes,由Marcel Dekker出版。假定降解动力学符合Arrhenius,每升高10℃以约为2的因子加速有效贮存期。因此,ICH指南估计在40℃贮存6个月相当于在室温贮存两年。因此该转换认为:在25℃和60%相对湿度贮存6个月与在5℃制剂的两年存贮期限相似。
制剂中的氧气和氮气水平可以通过本领域技术人员公知的任何方法测量。作为一个非限制性示例,在顶空中或制剂的溶解的气体中的氧气百分数可以通过在实施例10中描述的方法测量。作为一个非限制性示例,在顶空中或制剂的溶解的气体中的氮气百分数可以通过100减去用实施例10中描述的方法测得的氧气百分数估测。
本文所述是雷帕霉素的液体制剂,包括但不限于约2%w/w雷帕霉素、约4%w/w乙醇和94%w/w PEG 400的制剂,其中所述制剂的溶解的氧气水平小于或约等于如实施例1中所述方法制备的制剂中所溶解的氧气水平,所述氧气水平用描述在实施例10中的荧光法测量。本文所述是雷帕霉素的液体制剂,包括但不限于约2%w/w雷帕霉素、约4%w/w乙醇和94%w/w PEG 400的制剂,其中所述制剂的溶解的氮气水平约等于如实施例1中所述方法制备的制剂中所溶解的氮气水平,这是通过描述在实施例1中的荧光法测量的。
实施例2-通过旋转蒸发制备含有雷帕霉素的溶液
在一些实施例中,在制备西罗莫司(雷帕霉素)的储备溶液之前,将BHT(丁基化羟基甲苯)加入到乙醇中。将雷帕霉素加到100%乙醇中,该乙醇含有或不含BHT。将混合物超声足以减少溶解的氧气的一段时间,且直到所有雷帕霉素进入溶液中形成雷帕霉素储备溶液。通过将PEG 400超声足以减少溶解的氧气的一段时间,制备稀释溶剂。
然后将雷帕霉素储备溶液和稀释溶剂在旋转蒸发仪中在约室温下旋转一段时间,所述时间足以使储备溶液与稀释溶剂混合。通过提高溶液温度,在一段较长时间内保持不超过40℃,且持续旋转溶液,将一部分乙醇从溶液中蒸发掉。
得到的溶液包含约2%w/w雷帕霉素、约4%w/w乙醇和约94%w/w的PEG 400。
然后将溶液通过0.2微米滤器过滤。将透明的2ml玻璃小瓶填装2ml或者0.5ml的经过滤的溶液,在每个容器中分别留下约400或1900μl的顶空。接着将小瓶用例如特氟隆塞住,并用铝封条束缚。
根据描述在实施例1中的方法测定雷帕霉素稳定性。对每种小瓶构成进行分析,每种小瓶构成在表1中有一个编号。结果显示在表1中。
当将2ml不含BHT的制剂置于2ml透明玻璃小瓶中,在25摄氏度放置1、2和3个月后,相对于制剂中的雷帕霉素的起始量,制剂的雷帕霉素水平分别减少约7.0%、6.8%和9.6%。当将2ml制剂置于2ml透明玻璃小瓶中,在5摄氏度放置1、2、3和6个月后,相对于制剂中的雷帕霉素的起始量,制剂的雷帕霉素水平分别减少约4.9%、5.4%、7.7%和9.3%。当将2ml制剂置于2ml透明玻璃小瓶中,在-20摄氏度放置1、2、3和6个月后,相对于制剂中的雷帕霉素的起始量,制剂的雷帕霉素水平分别减少约0.6%、0.2%、1.7%和1.7%。
当将2ml含有BHT的制剂置于2ml透明玻璃小瓶中,在25摄氏度放置1、2和3个月后,相对于制剂中的雷帕霉素的起始量,制剂的雷帕霉素水平分别减少约4.2%、6.0%和10.8%。当将2ml含有BHT的制剂置于2ml透明玻璃小瓶中,在5摄氏度放置1、2、3和6个月后,相对于制剂中的雷帕霉素的起始量,制剂的雷帕霉素水平分别减少约2.3%、1.5%、4.4%和5.2%。当将2ml含有BHT的制剂置于2ml透明玻璃小瓶中,在-20摄氏度放置1、2、3和6个月后,相对于制剂中的雷帕霉素的起始量,制剂的雷帕霉素水平分别减少约0.9%、0.7%、3.1%和2.4%。不受理论限制,一般来说,对于这种小瓶构成而言,相对于不含BHT的制剂,BHT的作用可能是在某些温度下导致制剂稳定性提高,即使可能没有在所有的温度下发现这种作用。不受理论限制,认为因为顶空减小,与2ml小瓶中的0.5ml填充体积相比,其导致制剂更小程度地暴露于空气的成分下,所以相对于0.5ml填充体积,含有2ml填充体积的该种小瓶构成具有提高的雷帕霉素的稳定性。
当将0.5ml含有BHT的制剂置于2ml透明玻璃小瓶中,在25摄氏度放置1、2和3个月后,相对于制剂中的雷帕霉素的起始量,制剂的雷帕霉素水平分别减少约5.2%、5.8%和10.8%。当将0.5ml含有BHT的制剂置于2ml透明玻璃小瓶中,在5摄氏度放置1、2、3和6个月后,相对于制剂中的雷帕霉素的起始量,制剂的雷帕霉素水平分别减少约3.3%、2.0%、4.1%和6.0%。当将0.5ml含有BHT的制剂置于2ml透明玻璃小瓶中,在-20摄氏度放置1、2、3和6个月后,相对于制剂中的雷帕霉素的起始量,制剂的雷帕霉素水平分别减少约1.5%、1.4%、3.0%和2.2%。不受理论限制,认为对于这种小瓶构成,在-20摄氏度贮存得到比在5摄氏度贮存更好的雷帕霉素稳定性,且在-20或5摄氏度贮存得到比在25摄氏度贮存更好的雷帕霉素稳定性。不受理论限制,一般来说,对于这种小瓶构成而言,相对于不含BHT的制剂,BHT的作用可能是导致制剂稳定性提高。不受理论限制,认为因为顶空更大,与2ml小瓶中的2ml填充体积相比,其导致制剂更高程度地暴露于空气的成分下,所以含有0.5ml填充体积的该种小瓶构成具有降低的雷帕霉素的稳定性。
在这些制剂中的氧气和氮气水平可以用在实施例1或实施例10的一个或多个中描述的方法测定。
本文所述是雷帕霉素的液体制剂,包括但不限于约2%w/w雷帕霉素、约4%w/w乙醇和94%w/w PEG 400的制剂,其中制剂的溶解的氧气水平小于或约等于如实施例2中所述方法制备的制剂中所溶解的氧气水平,所述氧气水平用描述在实施例10中的荧光法测量。本文所述是雷帕霉素的液体制剂,包括但不限于约2%w/w雷帕霉素、约4%w/w乙醇和94%w/wPEG 400的制剂,其中制剂的溶解的氮气水平约等于如实施例2中所述方法制备的制剂中所溶解的氮气水平,所述氮气水平通过描述在实施例1中的荧光法测量。
实施例3-通过超声、旋转蒸发和鼓泡通入氮气制备包含雷帕霉素的溶液
在一个制备和包装液体制剂的实例中,将约320g 100%乙醇鼓泡通入医用级别的压缩氮气约10分钟。在一些实例中,制备雷帕霉素的储备溶液之前,将BHT(丁基化羟基甲苯)加到乙醇中。将40g雷帕霉素加到乙醇中,所述乙醇含有或不含BHT。将混合物超声约20分钟,到所述20分钟结束时,所有雷帕霉素进入溶液形成西罗莫司储备溶液。通过超声约1880gPEG 400约60分钟,接着向溶剂鼓泡通入氮气约10分钟,制备稀释溶剂。
然后将雷帕霉素储备溶液和稀释溶剂(PEG 400)在旋转蒸发仪中在约室温下旋转约10分钟,以便使储备溶液与稀释溶剂混合。混合后,将溶液通入医用级别压缩氮气约10分钟。通完后,通过升高溶液温度,在一段长的时间内保持温度不超过40℃,且继续旋转溶液约2.5h,将约240g过量乙醇从溶液中蒸发掉。
得到的溶液包含约2%最终重量的雷帕霉素、约4%最终重量的乙醇和约94%最终重量的PEG 400。将溶液鼓泡通入氮气约10分钟。然后,将溶液通过0.2微米滤器过滤。
将规则透明的2ml玻璃小瓶各填充2ml经过滤的溶液,每个容器剩余约400μl的顶空。将透明的2ml玻璃小瓶各填充0.5ml或2ml经过滤的溶液,每个容器分别剩余约1900和400μl的顶空。然后将玻璃小瓶用例如特氟隆塞住,并用铝封条束缚。
根据描述在实施例1中的方法测量雷帕霉素稳定性。对于每种小瓶构成进行分析,每种小瓶构成在表1中有一个编号。结果显示在表1中。
当将2ml含有BHT的制剂置于2ml透明玻璃小瓶中时,在25摄氏度放置1、2和3个月后,相对于制剂中的雷帕霉素的起始量,制剂的雷帕霉素水平分别减少约0.29%、4.8%和8.7%。当将2ml含有BHT的制剂置于2ml透明玻璃小瓶中,在5摄氏度放置1、2、3和6个月后,相对于制剂中的雷帕霉素的起始量,制剂的雷帕霉素水平分别减少约0%、0%、1.7%和2.5%。当将2ml含有BHT的制剂置于2ml透明玻璃小瓶中,在-20摄氏度放置1、2、3和6个月后,相对于制剂中的雷帕霉素的起始量,制剂的雷帕霉素水平分别减少约0%、0%、2.2%和1.4%。不受理论限制,一般来说,对于这种小瓶构成而言,相对于不含BHT的制剂,BHT的作用可能是在某些温度下导致制剂稳定性提高,即使可能没有在所有的温度下发现这种作用。不受理论限制,认为由于减小的顶空,与2ml玻璃小瓶中的0.5ml填充体积相比,其导致制剂更小程度地暴露于空气的成分下,相对于0.5ml填充体积,含有2ml填充体积的该种小瓶构成具有提高的雷帕霉素稳定性。
当将0.5ml含有BHT的制剂置于2ml透明玻璃小瓶中时,在25摄氏度放置1、2和3个月后,相对于制剂中的雷帕霉素的起始量,制剂的雷帕霉素水平分别减少约0%、4.7%和9.5%。当将0.5ml含有BHT的制剂置于2ml透明玻璃小瓶中时,在5摄氏度放置1、2、3和6个月后,相对于制剂中的雷帕霉素的起始量,制剂的雷帕霉素水平分别减少约0%、0%、2.4%和2.5%。当将0.5ml含有BHT的制剂置于2ml透明玻璃小瓶中时,在-20摄氏度放置1、2、3和6个月后,相对于制剂中的雷帕霉素的起始量,制剂的雷帕霉素水平分别减少约0%、0.6%、1.3%和1.4%。不受理论限制,一般来说,对于该种小瓶构成而言,相对于不含BHT的制剂,BHT的作用可能是导致制剂提高稳定性,即使没有在所有的温度下发现这种作用。不受理论限制,认为由于更大的顶空,与2ml小瓶中的2ml填充体积相比,其导致制剂更大程度地暴露于空气的成分下,含有0.5ml填充体积的该种小瓶构成具有减少的雷帕霉素稳定性。
当将2ml不含BHT的制剂置于2ml透明玻璃小瓶中时,在25摄氏度放置1、2和3个月后,相对于制剂中的雷帕霉素的起始量,制剂的雷帕霉素水平分别减少约6.3%、5.5%和9.9%。当将2ml不含BHT的制剂置于2ml透明玻璃小瓶中时,在5摄氏度放置1、2、3和6个月后,相对于制剂中的雷帕霉素的起始量,制剂的雷帕霉素水平分别减少约1.1%、1.3%、7.0%和6.9%。当将2ml不含BHT的制剂置于2ml透明玻璃小瓶中时,在-20摄氏度放置1、2、3和6个月后,相对于制剂中的雷帕霉素的起始量,制剂的雷帕霉素水平分别减少约0.2%、0%、1.8%和0.9%。不受理论限制,认为对于这种小瓶构成而言,相对于含有BHT的制剂,BHT的缺失可能导致制剂稳定性提高。不受理论限制,认为由于更小的顶空,与2ml小瓶中0.5ml填充体积相比,其导致制剂更低程度地暴露于空气的成分下,含有2ml填充体积的该种小瓶构成具有提高的雷帕霉素稳定性。
在这些制剂中的氧气和氮气水平可以用实施例1或实施例10中的一个或多个中描述的方法测量。
本文所述是雷帕霉素的液体制剂,包括但不限于约2%w/w雷帕霉素、约4%w/w乙醇和94%w/w PEG 400的制剂,其中制剂的溶解的氧气水平小于或约等于如实施例3中所述方法制备的制剂中所溶解的氧气水平,所述氧气水平用描述在实施例10中的荧光法测量。本文所述是雷帕霉素的液体制剂,包括但不限于约2%w/w雷帕霉素、约4%w/w乙醇和94%w/wPEG 400的制剂,其中制剂的溶解的氮气水平约等于如用实施例3中所述方法制备的制剂中所溶解的氮气水平,其通过描述在实施例1中的荧光法测量。
实施例4通过超声、旋转蒸发、鼓泡通入氮气和氮气覆盖制备包含雷帕霉素的溶液
完成描述在实施例3中的方法,但是在(a)除掉乙醇的旋转蒸发步骤,(b)过滤溶液和(c)填充小瓶的每一步后面,加入用医用级别压缩氮气覆盖雷帕霉素溶液约5分钟的步骤。在这些实验中,没有BHT添加到样品中。所有的玻璃小瓶是2ml透明玻璃,且用0.5ml或2.0ml制剂填充。
这个实验的三个重复用于进行含有2ml填充体积的实验,且两个重复以0.5ml填充体积进行。根据描述在实施例1中的方法测定雷帕霉素稳定性。对每种小瓶构成进行分析,其在表1中有编号。结果显示在表1中。对于所示的第一个和第三个重复,在60%相对湿度下测定。
当将0.5ml不含BHT的制剂置于2ml透明玻璃小瓶中时,在接下来的观测中,重复总体上显示一致性。不受理论限制,认为由于更大的顶空,与在2ml小瓶中的2ml填充体积相比,其导致制剂更大程度地暴露于空气的成分下,与2ml填充体积相比,含有0.5ml填充体积的小瓶构成具有降低的雷帕霉素稳定性。不受理论限制,认为相对于贮存在琥珀色玻璃中不含BHT的如在实施例1中制剂,含有0.5ml填充体积的该种小瓶构成具有提高的稳定性。
当将2ml不含BHT的制剂置于2ml透明玻璃小瓶中时,在接下来的观测中,重复总体上显示一致性。至少在较后面的时间点,相对于贮存在琥珀色玻璃中不含BHT的如实施例1中的制剂,含有2ml填充体积的该种小瓶构成具有提高的稳定性。在大多数时间点,相对于贮存在透明玻璃中不含BHT的如实施例2中的制剂,含有2ml填充体积的该种小瓶构成具有提高的稳定性。在大多数时间点,相对于贮存在透明玻璃中不含BHT的如实施例3中的制剂,含有2ml填充体积的该种小瓶构成具有提高的稳定性。
图2描述了制备稳定制剂的方法。
在这些制剂中的氧气和氮气水平可以用描述在实施例1或实施例10的一个或多个中的方法测定。
本文所述是雷帕霉素的液体制剂,包括但不限于约2%w/w雷帕霉素、约4%w/w乙醇和94%w/w PEG 400的制剂,其中制剂的溶解的氧气水平小于或约等于如用实施例4中所述方法制备的制剂中所溶解的氧气水平,所述氧气水平用描述在实施例10中的荧光法测量。本文所述是雷帕霉素的液体制剂,包括但不限于约2%w/w雷帕霉素、约4%w/w乙醇和94%w/wPEG 400的制剂,其中制剂的溶解的氮气水平约等于如用实施例4中所述方法制备的制剂中所溶解的氮气水平,所述氮气水平通过描述在实施例1中的荧光法测量。
实施例5
列举在表2中的任何一种或多种液体制剂可以通过超声制备。一般来说,为了制备包含对空气中一种或多种成分(包括但不限于氧气)敏感的治疗物质的稳定制剂,将制剂的一种或多种成分进行处理以减少氧气含量。将液体制剂中的一种或多种成分被超声一段时间,所述时间足以使一种或多种成分脱气。将所述一种或多种成分在它们与液体制剂的其它成分混合之前或之后超声。相对于超声前的治疗物质而言,在保持治疗物质稳定性的条件下,进行超声。当液体制剂的一种或多种成分对温度敏感时,超声在一种或多种温度敏感成分的稳定性被保持的条件下进行。当治疗物质是雷帕霉素时,温度优选在不超过40摄氏度保持一段长的时间。当液体制剂的一种或多种成分对光敏感时,超声在一种或多种温度敏感成分的稳定性被保持的条件下进行。
单独实施或与一种或多种生产稳定制剂的其它方法组合实施该方法。
在这些制剂中的氧气和氮气水平可以用描述在实施例1或实施例10的一个或多个中的方法测定。
本文所述是雷帕霉素的液体制剂,包括但不限于约2%w/w雷帕霉素、约4%w/w乙醇和94%w/w PEG 400的制剂,其中制剂的溶解的氧气水平小于或约等于如用实施例5中所述方法制备的制剂中所溶解的氧气水平,所述氧气水平用描述在实施例10中的荧光法测量。本文所述是雷帕霉素的液体制剂,包括但不限于约2%w/w雷帕霉素、约4%w/w乙醇和94%w/wPEG 400的制剂,其中制剂的溶解的氮气水平约等于如用实施例5中所述方法制备的制剂中所溶解的氮气水平,所述氮气水平通过描述在实施例1或10的一个或多个中的荧光法测量。
实施例6
在表2中所述的任何一种或多种液体制剂可以用本文所述的方法制备。一般来说,为了制备包含对空气中的一种或多种成分(包括但不限于氧气)敏感的治疗物质的稳定制剂,将制剂的一种或多种成分进行处理以减少氧气含量。液体制剂中的一种或多种成分鼓泡通入惰性气体,例如稀有气体,包括但不限于氮气、氩气或氦气。
单独实施或与一种或多种生产稳定制剂的其它方法组合实施该方法。
在一些实例中,治疗物质是雷帕霉素,且在实施例5-7中所述方法的各个阶段,将雷帕霉素制剂中的一种或多种成分鼓泡通入惰性气体例如氮气。
治疗物质的稳定性可以根据描述在实施例1中的方法测定。
在这些制剂中的氧气和氮气水平可以用描述在实施例1或10的一个或多个中的方法测定。
本文所述是雷帕霉素的液体制剂,包括但不限于约2%w/w雷帕霉素、约4%w/w乙醇和94%w/w PEG 400的制剂,其中制剂的溶解的氧气水平小于或约等于如用实施例6中所述方法制备的制剂中所溶解的氧气水平,所述氧气水平用描述在实施例10中的荧光法测量。本文所述是雷帕霉素的液体制剂,包括但不限于约2%w/w雷帕霉素、约4%w/w乙醇和94%w/wPEG 400的制剂,其中制剂的溶解的氮气水平约等于如用实施例6中所述方法制备的制剂中所溶解的氮气水平,所述氮气水平通过描述在实施例1中的荧光法测量。
实施例7
在表2中所述的任何一种或多种液体制剂可以用本文所述的方法制备。一般来说,为了制备包含对空气中的一种或多种成分(包括但不限于氧气)敏感的治疗物质的稳定制剂,将制剂的一种或多种成分进行处理以减少氧气含量。将液体制剂中的一种或多种成分用惰性气体覆盖,所述惰性气体例如稀有气体,包括但不限于氮气、氩气或氦气。
单独实施或与一种或多种生产稳定制剂的其它方法组合实施该方法。
在一些实例中,治疗物质是雷帕霉素,且在实施例5-7中所述方法的各个阶段,将雷帕霉素制剂中的一种或多种成分用惰性气体例如氮气覆盖。
治疗物质的稳定性可以根据描述在实施例1中的方法测定。
在这些制剂中的氧气和氮气水平可以用描述在实施例1或10的一个或多个中的方法测定。
本文所述是雷帕霉素的液体制剂,包括但不限于约2%w/w雷帕霉素、约4%w/w乙醇和94%w/w PEG 400的制剂,其中制剂的溶解的氧气水平小于或约等于如用实施例7中所述方法制备的制剂中所溶解的氧气水平,所述氧气水平用描述在实施例10中的荧光法测量。本文所述是雷帕霉素的液体制剂,包括但不限于约2%w/w雷帕霉素、约4%w/w乙醇和94%w/wPEG 400的制剂,其中制剂的溶解的氮气水平约等于如用实施例7中所述方法制备的制剂中所溶解的氮气水平,所述氮气水平通过描述在实施例1中的荧光法测量。
实施例8
通过描述在实施例5-7中的生产稳定制剂的方法中的任何一种或多种方法,制备稳定混悬剂。一般来说,为了制备包含对空气中的一种或多种成分(包括但不限于氧气)敏感的治疗物质的混悬剂,将制剂的一种或多种成分进行处理以减少氧气含量。通过超声、鼓泡通入惰性气体或用惰性气体覆盖中的一种或多种,将液体制剂中的一种或多种成分进行处理,其中惰性气体是稀有气体,其为氮气、氩气或氦气。
然后将混悬液中的一种或多种成分通过0.2微米滤器过滤用于灭菌。混悬剂要么包含足够小尺寸的以至于能通过0.2微米滤器过滤的颗粒,要么包含用本领域技术人员公知的其它方法灭菌的颗粒。颗粒任选是纯的治疗物质的颗粒或晶体,其在将颗粒或晶体加到制剂的其它成分之前或之后被灭菌。颗粒任选用γ-射线或电子束灭菌进行处理,它们是本领域技术人员所用的固体灭菌的标准方法的非限制性示例。
在一些实例中,治疗物质是雷帕霉素,且混悬剂是纳米混悬剂。在一些实例中,治疗物质是雷帕霉素,且雷帕霉素以用γ-射线或电子束处理灭菌的纯的雷帕霉素颗粒存在。
单独实施或与一种或多种生产稳定制剂的其它方法组合实施该方法。
治疗物质的稳定性可以根据描述在实施例1中的方法测定。
在这些制剂中的氧气和氮气水平可以用描述在实施例1或10的一个或多个中的方法测定。
本文所述是雷帕霉素的液体制剂,包括但不限于约2%w/w雷帕霉素、约4%w/w乙醇和94%w/w PEG 400的制剂,其中制剂的溶解的氧气水平小于或约等于如用实施例8中所述方法制备的制剂中所溶解的氧气水平,所述氧气水平用描述在实施例10中的荧光法测量。本文所述是雷帕霉素的液体制剂,包括但不限于约2%w/w雷帕霉素、约4%w/w乙醇和94%w/wPEG 400的制剂,其中制剂的溶解的氮气水平约等于如用实施例8中所述方法制备的制剂中所溶解的氮气水平,所述氮气水平通过描述在实施例1中的荧光法测量。
实施例10-溶解气体中的氧气的测量
总的来说,光纤氧传感器是用于检测气体和液体中氧分压的相位荧光计耦联传感器。用荧光法测量溶解的或气体的氧气的分压力。光纤将由蓝色LED产生的激发光传送到探针尖端的薄膜涂层。探针收集在尖端产生的荧光,并通过光纤将它传送到高灵敏度光谱仪。荧光淬灭程度与碰撞频率相关,因此与含有氧气的介质的浓度、压力和温度相关。
用于探针尖端的薄膜据报道不消耗氧气,从而可以持续与样品接触。另外,据报道FOXY传感器对于由pH值变化引起的干扰或者来自离子强度、盐度和生物污垢的变化干扰是有免疫力的。
测量如下进行。脉冲式蓝色LED发送在约475nm的光线到光纤。光线将光线传送到氧气探针。探针尖端的顶部由疏水性溶胶-凝胶材料组成。将钌络合物捕获在溶胶-凝胶基质中,所述溶胶-凝胶基质固定钌络合物,且保护它免于受水影响。来自LED的光线激发在探针尖端的钌络合物。激发的钌络合物发射荧光,释放能量在约600nm。
如果激发的钌络合物遇到氧气分子,多余的能量以非辐射转移形式转移到氧气分子,降低或淬灭荧光信号。
能量被探针收集,且通过光纤传送到光谱仪。A/D转换器将这种模拟数据转化为数字数据,该数字数据显示在OOISensors软件中。
实施例11氧气水平和制剂稳定性
将约2%w/w雷帕霉素、4%w/w乙醇、94%w/w PEG 400的制剂用实施例3中的方法制备,且用空气或表3中所示的气体覆盖。氮气覆盖导致在顶空中有0.8%的氧气。空气覆盖导致在顶空中有20.4%的氧气。氧气覆盖导致在顶空中有84.7%的氧气。
将100ml制剂填充到100ml琥珀色瓶中并贮存。对于每一个样品,将1ml该制剂置于2ml小瓶中。将样品用氧气鼓泡(冒泡)通入,通入时间如在表3中所示。在用实施例10中所述方法测量顶空中和溶解的气体中的氧气百分数前,使样品平衡24小时。
对于每个时间点的稳定性测量而言有3次重复。对于氧气百分含量的测量而言,处理组1、2、3和6中的每一组有3次重复,处理组4、5、7、8和12中的每一组有2次重复,处理组9、10、11和13中的每一组有1次重复。分析前,将样品保持在室温和在黑暗中。
通过计算在具体时间点雷帕霉素的相对于加到原始制剂的雷帕霉素的重量的重量百分含量,测定稳定性。用描述在实施例1中的方法,在1周、2周、1个月和2个月时测定稳定性。结果显示在表3中,且描述在图3、4和5中。
不受理论限制,由于乙醇挥发,所以用氧气鼓泡通入10或30分钟的样品可能显示较高的雷帕霉素百分数。
图3显示在1周、2周、1个月和2个月时,对于处理组1-13而言,在顶空中的氧气百分数对制剂强度百分数。将处理组在顶空处理内进行平均(例如将来自处理组1-7、8-12和处理组13的每一组的所有样品进行平均)。综观所有处理组,平均数据一致性地使较高的制剂强度百分数与较小的顶空中的氧气百分数相关联。
图4显示在1周、2周、1个月和2个月时,对于处理组1-13而言,在溶解的气体中的氧气百分数对制剂强度百分数。将处理组在顶空处理内进行平均(例如将来自处理组1-7的所有样品进行平均,将来自处理组8-12的所有样品进行平均,和将来自处理组13的所有样品进行平均)。综观所有处理组,平均数据一致性地使较高的制剂强度百分数与较小的顶空中的氧气百分数相关联。
图5显示在1周、2周、1个月和2个月时,对于处理组1、8和13(没有鼓泡通入氧气的处理组)而言,制剂强度百分数相对于顶空中的氧气百分数。在所有时间点,平均数据一致性地使较强的制剂强度与较小的顶空中的氧气百分数相关联。
实施例12-在2%雷帕霉素制剂中制剂强度与每毫克雷帕霉素的顶空中氧气毫升数之间的关系
就许多样品而言,计算在2%雷帕霉素制剂中的每毫克雷帕霉素的顶空中氧气的毫升数,且氧气毫升数/毫克雷帕霉素在一段时间内对制剂强度的作用显示在图6A、6C、7A和8A中。
对于表4的数据而言,如实施例4中所述制备雷帕霉素制剂。对于表5的数据而言,如实施例11中所述制备雷帕霉素制剂。在图6A、6B、7A、7B、8A和8B中分析的所有制剂已用氮气覆盖。具体地讲,使用来自于表1的在时间零时显示98.6%效价的0.5ml填充体积样品,并使用来自于表1的在时间零时显示96.1%效价的2ml填充体积样品。对于图6C,覆盖处理是来自实施例11的氮气覆盖处理组1(导致在顶空中有0.80%的氧气)、来自实施例11的空气覆盖处理组8(导致在顶空中有20.4%的氧气)和来自实施例11的氧气覆盖处理组13(导致在顶空中有84.7%的氧气)。
在顶空中的氧气的量如下计算。顶空中的氧气百分数用描述在实施例10中基于探针的光纤荧光进行测量。根据顶空中的氧气百分数和顶空体积,以μl为单位计算氧气的量。例如,如果顶空体积是2.0ml(2000μl),测得的氧气百分数是0.8%,在顶空中的氧气的量是2.0ml的0.8%,也就是16μl。
在填充体积中的雷帕霉素的mg数通过采用1.1的溶液密度将溶液体积转化成质量进行计算。将该质量乘以溶液中雷帕霉素的2%浓度。例如,对于0.5ml填充体剂而言,有0.55g溶液。作为0.55g中的2%,在填充体积中的雷帕霉素的量是11mg。
因此,在填充体积中的每毫克雷帕霉素的顶空中氧气的量是16μl/11mg或1.455μl/mg雷帕霉素。
对于25℃而言样品在各种时间点的制剂强度来自表3,且与氧气的毫升数/毫克雷帕霉素一起总结在表4和5中。来自处理组1、8和13的数据显示在表5中。对于5℃和-20℃而言样品在各种时间点的制剂强度来自表1,且与氧气的毫升数/毫克雷帕霉素一起总结在表4中。注意,尽管表1显示雷帕霉素百分数降低/雷帕霉素效价,但这是相对于时间零时制剂的百分数降低。那么,表4所示的制剂强度如下得到:从100中减去雷帕霉素效价中的百分数降低,并乘以时间零的制剂强度的结果数。
正如在图6A和7A中能看到的,在25℃和5℃温度下经过一段长的时间,具有较低的顶空中的氧气毫升数与在制剂中的雷帕霉素毫克数之比的组具有较强的制剂强度。不受理论限制,显示在-20℃组中较低温度的作用大于顶空中的氧气毫升数与制剂中雷帕霉素毫克数之比的作用。
实施例13-顶空/填充体积的比率与制剂强度的关系
顶空与填充体积的比率显示在图6B、7B和8B中。顶空与填充体积的比率通过用填充体积除顶空体积进行计算。顶空/填充体积的比率显示在表4中。注意,尽管小瓶全部是2ml的小瓶,在这些小瓶中有额外的顶空体积,其被考虑在计算顶空与填充体积的比率中。
正如在图6B和7B中能看到的,在25℃和5℃温度下经过一段长的时间,较低的顶空/填充体积组具有更高的制剂强度。不受理论限制,显示在-20℃组中,较低温度的作用大于顶空/填充体积的比率的作用。
将本文引用的所有文献,包括专利、专利申请和出版物,以其全部内容引入文中作为参考,无论之前是否已明确引入。
| 制剂编号 | 组成(mg),%(w/w) | 制剂类型 |
| 1 | DMSO=2000mg(20%)水=8000mg(80%) | S |
| 2 | F68=1000mg(10%)水=9000mg(90%) | S |
| 3 | F68=3000mg(30%)水=7000mg(70%) | S |
| 4 | F127=1000mg(10%)水=9000mg(90%) | S |
| 5 | F127=1500mg(15%)水=8500mg(85%) | S |
| 6 | β-环糊精=250mg(2.5%)水=9750mg(97.5%) | S |
| 7 | 雷帕霉素=10.2mg(0.101%)普流罗尼克,F68=1010mg(9.99%)水=9090mg(89.909%) | S |
| 8 | 雷帕霉素=10.2mg(0.102%)普流罗尼克,F68=3000mg(29.969%)水=7000mg(69.929%) | S |
| 9 | 雷帕霉素=10.5mg(0.104%)普流罗尼克,F127=1010mg(9.99%)水=9090mg(89.907%) | S |
| 10 | 雷帕霉素=10.5mg(0.105%)普流罗尼克,F127=1500mg(14.984%)水=8925mg(84.9%) | S |
| 11 | 雷帕霉素=10.7mg(0.105%)β-环糊精=255mg(2.497%)水=9945mg(97.398%) | S |
| 12 | 雷帕霉素=6.4mg(0.0999%)CMC=48mg(0.7493%)聚脱水山梨糖醇20=2.56mg(0.04%)水=6349.44mg(99.111%) | SP |
| 13 | 雷帕霉素=6.5mg(0.0999%)DMSO=325mg(4.995%)水=6175mg(94.905%) | S |
| 14 | 雷帕霉素=13.5mg(0.0999%)CMC=101.25mg(0.7493%)聚脱水山梨糖醇20=5.4mg(0.04%)水=13393.35mg(99.112%) | SP |
| 15 | 雷帕霉素=11.0mg(0.2%)EtOH=5500mg(99.8%) | S |
| 16 | 雷帕霉素=6.6mg(0.1%)EtOH=1054.6mg(15.933%)F127=833.64mg(12.595%)水=4723.96mg(71.372%) | S |
| 17 | 雷帕霉素=5mg(0.1%)Cavitron=0.25g(5%)乙醇,95%=57mg(1.1%)无菌水=4.753g(93.8%) | S |
| 18 | 雷帕霉素=5mg(0.1%)乙醇,95%=150mg(2.9%)PEG400=1.0g(19.4%)无菌水=4.01g(77.6%) | S |
| 制剂编号 | 组成(mg),%(w/w) | 制剂类型 |
| 19 | 雷帕霉素=5mg(0.1%)乙醇,95%=152mg(3.2%)PEG400=1.5227g(30.2%)无菌水=3.3592g(66.67%) | S |
| 20 | 雷帕霉素=6.6mg(0.1%)EtOH=505.1mg(7.618%)F127=917.8mg(13.843%)水=5200.6mg(78.44%) | S |
| 21 | 雷帕霉素=6.6mg(0.1%)EtOH=536mg(7.5%)普流罗尼克,F127=983.75mg(14.0%)水=5574.56mg(78.4%) | S |
| 22 | 雷帕霉素=5.2mg(0.1023%)EtOH=56.6mg(1.127%)Captisol=2008.9mg(39.5%)水=3013.3mg(59.3%) | S |
| 23 | 雷帕霉素=6.9mg(0.201%)EtOH=3418.0mg(99.799%) | S |
| 24 | 雷帕霉素=9.1mg(0.491%)EtOH=90.9mg(4.908%)F127=262.8mg(14.191%)水=1489.1mg(80.409%) | S |
| 25 | 雷帕霉素=0mg(0%)EtOH=310.2mg(5.144%)F127=858.1mg(14.228%)水=4862.6mg(80.628%) | S |
| 26 | 雷帕霉素=0mg(0%)EtOH=613.1mg(10.19%)F127=810.6mg(13.471%)水=4593.6mg(76.339%) | S |
| 27 | 雷帕霉素=53.5mg(1.095%)EtOH=414.8mg(8.488%)F127=662.8mg(13.563%)水=3755.7mg(76.854%) | S |
| 28 | 雷帕霉素=0.3g(10%)PVP K90=0.35g(12%)Eudragit RS30D=2.35g(78%) | ISG,SP |
| 29 | 雷帕霉素=0.2154g(7.31%)PVP K90=0.25g(8.5%)Eudragit RS30D=2.48g(84.19%) | ISG,SP |
| 30 | 雷帕霉素=53.9mg(1.103%)EtOH=413.6mg(8.463%)无菌水=3843.5mg(78.647%)F127(Lutrol)=576.0mg(11.786%) | S |
| 31 | 雷帕霉素=0mg(0%)EtOH=411.9mg(8.513%)无菌水=3849.3mg(79.554%)F127(Lutrol)=577.4mg(11.933%) | S |
| 32 | 雷帕霉素=54.1mg(1.256%)EtOH=416.8mg(9.676%)无菌水=3836.3mg(78.569%)F127(Lutrol)=577.5mg(10.499%) | S |
| 制剂编号 | 组成(mg),%(w/w) | 制剂类型 |
| 33 | 雷帕霉素=80.7g(1.964%)EtOH=65.0mg(0.158%)PEG400=4021.8mg(97.878%) | S |
| 34 | 雷帕霉素=106.9g(5.233%)EtOH=129.6mg(6.344%)PEG400=1806.5mg(88.424%) | S |
| 35 | 雷帕霉素=0mg(0%)PVP K90=0.204g(2.3%)乙醇,100%=0.4g(4.5%)Eudragit RL100=0.201g(2.3%)PEG 400=8.00g(90.9%) | ISG,SP |
| 36 | 雷帕霉素=0mg(0%)PVP K90=0.2g(2.2%)乙醇,100%=0.4g(4.4%)PVAP=0.4g(4.4%)PEG 400=8.00g(88.9%) | ISG,SP |
| 37 | 雷帕霉素=106.1mg(4.2%)PVP K90=55.2mg(2.2%)乙醇,100%=108mg(4.3%)Eudragit RL100=55mg(2.2%)PEG 400=2.2g(87.1%) | ISG.SP |
| 38 | 雷帕霉素=399.6mg(9.965%)F68(Lutrol)=40.6mg(1.012%)无菌水=3569.7mg(89.022%) | S |
| 39 | 雷帕霉素=53.8mg(1.1%)EtOH=415.2mg(8.489%)无菌水=3844.2mg(78.594%)F127=578.0mg(11.817%) | S |
| 40 | 雷帕霉素=208.1mg(3.148%)PEG400=6403.4mg(96.852%) | S |
| 41 | 雷帕霉素=200.4mg(5.148%)F68(Lutrol)=20.8mg(0.534%)PEG400=3569.3mg(91.697%)EtOH(95%)=102mg(2.62%) | SP |
| 42 | 雷帕霉素=200.4g(5.259%)PEG400=3561.4mg(93.46%)吐温80=48.8mg(1.281%) | SP |
| 43 | 雷帕霉素=30.9mg(1.03%)PEG 400=2.9624g(98.97%) | S |
| 44 | 雷帕霉素=61mg(1.96%)乙醇,100%=0.1860g(6%)PEG 400=2.8588g(92.04%) | S |
| 45 | 雷帕霉素=90.7mg(3.02%)乙醇,100%=0.2722g(9.06%)PEG 400=2.6423g(87.94%) | S |
| 46 | 雷帕霉素=101.6mg(4.997%)EtOH=331.6mg(16.308%)PEG400=1600.1mg(78.695%) | S |
| 47 | 雷帕霉素=120.9g(3.189%)F68(Lutrol)=42.4mg(1.118%)无菌水=3627.7mg(95.692%) | SP |
| 48 | 雷帕霉素=100.1g(1.999%)EtOH=305.1mg(6.092%)PEG400=4602.9mg(91.909%) | S |
| 制剂编号 | 组成(mg),%(w/w) | 制剂类型 |
| 49 | 雷帕霉素=150.5mg(3.004%)PEG400=4860.3mg(96.996%) | SP |
| 50 | 雷帕霉素=153.4mg(3.055%)F68(普流罗尼克)=50.6mg(1.008%)无菌水=4816.6mg(95.937%) | SP |
| 51 | 雷帕霉素=116.6mg(2.29%)EtOH=306.6mg(6.05%)PEG400=4647.5mg(91.66%) | S |
| 52 | 雷帕霉素=150.4mg(2.994%)F68 Lutrol=15.4mg(0.306%)无菌水=4859.1mg(96.7%) | SP |
| 53 | 雷帕霉素=306.5mg(6.088%)PEG 400=4727.7mg(93.912%) | SP |
| 54 | 雷帕霉素=309.3mg(6.146%)PEG 400=4723.3mg(93.854%) | SP |
| 55 | 雷帕霉素=303.3mg(6.061%)PEG 400=4700.6mg(93.939%) | SP |
| 56 | 雷帕霉素=305.4mg(6.088%)PEG 400=4711.0mg(93.912%) | SP |
| 57 | 雷帕霉素=306.9mg(6.098%)PEG 400=4725.5mg(93.902%) | SP |
| 58 | 雷帕霉素=302.5mg(6.021%)PEG 400=4721.6mg(93.979%) | SP |
| 59 | 雷帕霉素=304.5mg(6.053%)PEG 400=4726.4mg(93.947%) | SP |
| 60 | 地塞米松=251.4mg(5.011%)PEG 400=4765.2mg(94.989%) | SP |
| 61 | 地塞米松=252.4mg(5%)PEG 400=4600mg(92%)EtOH=150mg(3%) | SP |
| 62 | 雷帕霉素=32.2mg(0.641%)PEG 400=4677.9mg(93.096%)EtOH=314.7mg(6.263%) | S |
| 63 | 雷帕霉素=32.3mg(0.6%)PEG 400=5516.3mg(93.1%)EtOH=314.7mg(6.263%) | S |
| 64 | 雷帕霉素=54.4mg(1.007%)PEG 400=4638.9mg(92.702%)EtOH=314.8mg(6.291%) | S |
| 65 | 雷帕霉素=50.8mg(1.013%)PEG 400=4963.2mg(98.987%) | S |
| 66 | 雷帕霉素=52.1mg(1.035%)PEG 400=4868.6mg(96.718%)EtOH=113.1mg(2.247%) | S |
| 67 | 雷帕霉素=50.5mg(1.009%)PEG 400=4752.8mg(94.953%)EtOH=202.1mg(4.038%) | S |
| 68 | 雷帕霉素=101.8mg(2.030%)PEG 400=4712.4mg(93.970%)EtOH=200.6mg(4.000%) | S |
| 制剂编号 | 组成(mg),%(w/w) | 制剂类型 |
| 69 | 雷帕霉素=102.1mg(2.036%)PEG 400=4605.5mg(91.847%)EtOH=306.7mg(6.117%) | S |
| 70 | 雷帕霉素=101.6mg(2.025%)PEG 400=4510.6mg(89.892%)EtOH=405.6mg(8.083%) | S |
| 71 | 雷帕霉素=75.9mg(3.019%)PEG 400=2438.4mg(96.981%) | SP |
| 72 | 雷帕霉素=50.9mg(2.034%)PEG 400=2350.1mg(93.914%)EtOH=101.4mg(4.052%) | S |
| 73 | 雷帕霉素=12.5mg(0.620%)PEG 400=2004.8mg(99.380%) | SP |
| 74 | 雷帕霉素=1.20949g(2.0152%)EtOH=2.401g(4.000%)PEG 400=56.407g(93.9848%) | S |
| 75 | 雷帕霉素=16.0mg g(0.795%)EtOH=80.0mg(3.976%)PEG 400=1916.0mg(95.2298%) | S |
| 76 | 雷帕霉素=8.1mg(0.400%)PEG 400=2014.5mg(99.600%) | SP |
| 77 | 雷帕霉素=8.6mg(0.428%)PEG 400=2002.5mg(99.572%) | S |
| 78 | 雷帕霉素=8.2mg(0.410%)PEG 400=1992.0mg(99.590%) | S |
| 79 | 雷帕霉素=8.7mg(0.433%)PEG 400=1998.8mg(99.567%) | S |
| 80 | 雷帕霉素=8.6mg(0.427%)PEG 400=2003.2mg(99.573%) | S |
| 81 | 雷帕霉素=8.6mg(0.428%)PEG 400=1999.3mg(99.572%) | S |
| 82 | 雷帕霉素=9.0mg(0.448%)PEG 400=2000.8mg(99.552%) | S |
| 83 | 雷帕霉素=8.0mg(0.397%)PEG 400=2008.8mg(99.603%) | S |
| 84 | 雷帕霉素=8.5mg(0.422%)PEG 400=2006.8mg(99.578%) | S |
| 85 | 雷帕霉素=8.0mg(0.399%)PEG 400=1998.2mg(99.601%) | S |
| 86 | 雷帕霉素=8.5mg(0.422%)PEG 400=2004.3mg(99.578%) | S |
| 87 | 雷帕霉素=8.6mg(0.428%)PEG 400=2002.5mg(99.572%) | S |
| 88 | 雷帕霉素=0.7g(1.983%)EtOH=1.4g(3.966%)PEG 400=33.2g(94.051%) | S |
| 89 | 雷帕霉素=0g(0%)EtOH=0.574g(1.995%)PEG 400=28.2g(98.005%) | S |
| 90 | 雷帕霉素=1.95g(1.950%)EtOH=4.05g(4.050%)PEG 400=94.00g(94000.%) | S |
| 制剂编号 | 组成(mg),%(w/w) | 制剂类型 |
| 91 | 雷帕霉素=0.0107g(0.534%)EtOH=0.0805g(4.019%)PEG 400=1.912g(95.447%) | S |
| 92 | 雷帕霉素=0.0081g(0.403%)EtOH=0.0804g(4.003%)PEG 400=1.920g(95.594%) | S |
| 93 | 雷帕霉素=1.992g(2%)EtOH=3.9419(4%)PEG 400=93.95g(94%) | S |
| 94 | 雷帕霉素=0.405g(0.4%)EtOH=4.24g(4%)PEG 400=95.6(95.6%) | S |
| 95 | PEG 400=96g(96%)EtOH=3.9027(4%) | S |
| 96 | 雷帕霉素=0.4020g(0.402%)EtOH=3.970g(3.971%)PEG 400=95.600g(95.627%) | S |
| 97 | 雷帕霉素=2.000g(1.990%)EtOH=4.000g(3.980%)PEG 400=94.500g(94.030%) | S |
| 98 | PEG 400=96g(96%)EtOH=3.92g(4%) | S |
| 99 | 雷帕霉素=0.4036g(0.4%)EtOH=3.9054g(4%)PEG 400=95.6(95.6%) | S |
| 100 | 雷帕霉素=2.0025g(2%)EtOH=3.98g(4%)PEG 400=94.00g(94%) | S |
| 101 | 雷帕霉素=9.5mg(0.472%)EtOH=90.3mg(4.485%)PEG 600=1913.5mg(95.043%) | S |
| 102 | 雷帕霉素=44.6mg(2.21%)EtOH=86.1.0mg(4.26%)PEG 600=1891.1mg(93.53%) | S |
| 103 | 雷帕霉素=1.97g(2%)EtOH=4.10g(4%)PEG 400=94.15g(94%) | S |
| 104 | 雷帕霉素=1.95g(2%)EtOH=4.00g(4%)PEG 400=94.0g(94%) | S |
| 105 | 雷帕霉素=8.00g(2%)PEG 400=376.0gEtOH=16.0g(4%) | S |
| 106 | 雷帕霉素=6.00g(2%)PEG 400=282.0g(94%)EtOH=12.0g(4%) | S |
| 107 | 雷帕霉素=8.9mg(0.4434%)EtOH=80.3mg(4.0006%)PEG 300=1918.0mg(95.556%) | S |
| 108 | 雷帕霉素=40.8mg(2.00886%)EtOH=110.0mg(5.41605%)PEG 300=1880.2mg(92.57509%) | S |
| 制剂编号 | 组成(mg),%(w/w) | 制剂类型 |
| 109 | 雷帕霉素=9.9mg(0.488%)EtOH=86.7mg(4.277%)PEG 400/300(50/50)=1930.3mg(95.235%) | S |
| 110 | 地塞米松=142.5mg(4.994%)PEG 400=2710.7mg(95.006%) | SP |
| 111 | 地塞米松=134.3mg(4.891%)PEG 400=2611.4mg(95.109%) | SP |
| 112 | 曲安西龙=139.2mg(5.087%)PEG 400=2597.4mg(94.913%) | SP |
| 113 | 曲安西龙=135.3mg(5.089%)PEG 400=2523.5mg(94.911%) | SP |
| 114 | EtOH=206.4mg(4.121%)PEG 400=4801.6mg(95.879%) | S |
| 115 | 雷帕霉素=43.0mg(2.144%)PEG 400=1962.3mg(97.8567%) | SP |
| 116 | 雷帕霉素=40.0mg(2.001%)PEG 400=1959.1mg(97.999%) | SP |
| 117 | 雷帕霉素=42.9mg(2.142%)PEG 400=1959.7mg(97.858%) | SP |
| 118 | 雷帕霉素=100.8mg(2.013%)PEG 400=4906.0mg(97.987%) | SP |
| 119 | 雷帕霉素=20.9mg(0.42%)EtOH=209.1mg(4.17%)PEG 400=4784.9mg(95.41%) | S |
| 120 | 雷帕霉素=20.6mg(0.41%)EtOH=211.5mg(4.22%)苯扎氯铵=19.1mg(0.38%)PEG 400=4762.0mg(94.99%) | S |
| 121 | 雷帕霉素=20.1mg(0.40%)EtOH=211.5mg(4.22%)苯扎氯铵=2.3mg(0.05%)PEG 400=4782.3mg(95.34%) | S |
| 122 | 雷帕霉素=8.0g(2%)EtOH=16.0g(4%)PEG400=376.0g(94%) | S |
| 123 | 雷帕霉素=351.3mg(2.006%)EtOH=2353.1mg(4.093%)PEG 400=16448.2mg(93.901%) | S |
| 124 | 雷帕霉素=2.2035g(2%)EtOH=4.45g(4%)PEG 400=103.7g(94%( | S |
| 125 | 雷帕霉素=515.5mg(2.021%)PEG 400=24.993.8mg(97.979%) | SP |
| 126 | 雷帕霉素=0.3g(2%)EtOH=0.6g(4%)PEG 400=14.1g(94%)BHT=0.0002(0.002%) | S |
| 制剂编号 | 组成(mg),%(w/w) | 制剂类型 |
| 127 | 雷帕霉素=0.3g(2%)EtOH=0.6g(4%)PEG 400=14.1g(94%)BHT=0.00037(0.004%) | S |
| 128 | 雷帕霉素=0.3g(2%)EtOH=0.6g(4%)PEG 400=14.1g(94%)BHT=0.0081(0.05%) | S |
| 129 | 雷帕霉素=243.2mg(1.869%)EtOH=4.88.4mg(3.753%)PEG 400=12283.3mg(94.378%) | S |
| 130 | 雷帕霉素=0.404g(2%)EtOH =0.8g(4%)PEG 400=18.8g(94%)BHT=0.00051(0.002%) | S |
| 131 | 雷帕霉素=0.6024g(2%)EtOH=1.2g(4%)PEG 400=28.25g(94%) | S |
| 132 | 雷帕霉素=2.001g(2%)EtOH=4.05g(4%)PEG 400=94.45g(94%) | S |
| 133 | 雷帕霉素=0.5155g(2.057%)EtOH=1.0198g(4.070%)PEG 400=23.5225g(93.873%) | S |
| 134 | PEG 400=9.6g(96%)EtOH=0.4g(4%) | S |
| 135 | 雷帕霉素=0.610g(2%)EtOH=1.2g(4%)PEG 400=28.2g(94%) | S |
| 136 | 雷帕霉素=24.6mg(1.193%)EtOH=91.1mg(4.418%)泰洛沙泊=219.6mg(10.649%)BSS=1726.8mg(83.740%) | S |
| 137 | 雷帕霉素=100.0mg(1.993%)PEG 400=4916.9mg(98.007%) | SP |
| 138 | 雷帕霉素=201.6mg(4.005%)PEG 400=4831.5mg(95.995%) | SP |
| 139 | 雷帕霉素=102.4mg(2.036%)EtOH=209.0mg(4.154%)PEG 400=4719.3mg(93.810%) | S |
| 140 | 雷帕霉素=10.3mg(0.205%)EtOH=27.4mg(0.544%)PEG 400=4995.8mg(99.251%) | S |
| 141 | 雷帕霉素=10.6mg(0.211%)EtOH=208.4mg(4.150%)PEG 400=4802.3mg(95.639%) | S |
| 142 | 雷帕霉素=31.5mg(0.628%)EtOH=67.1mg(1.337%)PEG 400=4918.9mg(98.035%) | S |
| 143 | 雷帕霉素=30.8mg(0.613%)EtOH=204.5mg(4.073%)PEG 400=4786.1mg(95.314%) | S |
| 制剂编号 | 组成(mg),%(w/w) | 制剂类型 |
| 144 | 雷帕霉素=103.5mg(2.057%)EtOH=207.1mg(4.116%)PEG 400=4720.8mg(93.827%) | S |
| 145 | 雷帕霉素=283.0mg(2.020%)EtOH=566.1mg(4.041%)PEG 400=13.160.8mg(93.939%) | S |
| 146 | 雷帕霉素=280.1mg(1.998%)EtOH=565.2mg(4.033%)PEG 400=13.171.7mg(93.969%) | S |
| 147 | 雷帕霉素=201.6mg(3.000%)PEG 400=6518.8mg(97.000%) | SP |
| 148 | 雷帕霉素=31.9mg(1.019%)苄醇=1021.9mg(20.070%)芝麻油=4017.9mg(78.911%) | S |
| 149 | 雷帕霉素=51.5mg(1.03%)苄醇=259.9mg(5.19%)芝麻油=4694.3mg(93.78%) | S |
| 150 | 雷帕霉素=5.96g(2%)EtOH=12.0g(4%)PEG 400=282.0g.(94%) | S |
| 151 | 雷帕霉素=54.5mg(1.07%)苄醇=1014.3mg(19.95%)橄榄油=4014.8mg(78.98) | S |
| 152 | 雷帕霉素=0mg(0.00%)苄醇=269.4mg(5.421%)泰洛沙泊=608.2mg(12.238%)芝麻油=4092.2mg(82.341%) | S |
| 153 | 雷帕霉素=76.3mg(1.75%)苄醇=307.0mg(7.06%)泰洛沙泊=607.8mg(13.97%)芝麻油=3000.5mg(68.97%)司盘80=63.1mg(1.45%)EtOH=295.5mg(6.79%) | S |
| 154 | 150号制剂=200g(99.998)BHT=0.004g(0.002%) | S |
| 155 | 雷帕霉素=51.0mg(0.87%)EtOH=642.3mg(10.93%)苄醇=431.8mg(7.34%)芝麻油=4753.7mg(80.86%) | S |
| 156 | 雷帕霉素=51.4mg(1.03%)苄醇=518.4mg(10.34%)橄榄油=4444.7mg(88.64%) | S |
| 157 | 雷帕霉素=8.1g(2%)EtOH=16.0g(4%)PEG 400=376.0g(94%) | S |
| 158 | 157号制剂=225.00g(99.998%)BHT=0.0045g(0.002%) | S |
| 159 | 雷帕霉素=8.1g(2%)EtOH=16.0g(4%)PEG 400=376g(94%) | S |
| 160 | 159号制剂=112.0g(99.998%)BHT=0.00224g(0.002%) | S |
| 制剂编号 | 组成(mg),%(w/w) | 制剂类型 |
| 161 | 159号制剂=112.0g(99.998%)BHT=0.0019g(0.002%) | S |
| 162 | 雷帕霉素=55.4mg(1.10%)EtOH=112.7mg(2.25%)苄醇=157.8mg(3.15%)棉籽油=4688.0mg(93.50%) | S |
| 163 | 雷帕霉素=5.005g(1%)EtOH=10.0g(2%)PEG 400=485.5g(97%) | S |
| 164 | PEG 400=9.82g(98%)EtOH=0.235g(2%) | S |
| 165 | 163号制剂=100.25g(99.998%)BHT=0.0026g(0.002%) | S |
| 166 | 雷帕霉素=203.1mg(2.025%)F68=30.3mg(0.303%)无菌水=9792.6mg(97.672%) | SP |
| 167 | 雷帕霉素=201.4mg(2.0005%)吐温20=43.9mg(0.436%)无菌水=9822.8mg(97.564%) | SP |
| 168 | EtOH=0.8301g(4.144%)PEG 400=19.2014g(95.856%) | S |
| 169 | 168号制剂=300μl | S |
| 170 | 168号制剂=250μl 154号制剂=50μl | S |
| 171 | 168号制剂=200μl 154号制剂=100μl | S |
| 172 | 168号制剂=150μl 154号制剂=150μl | S |
| 173 | 154号制剂=300μl | S |
| 174 | 雷帕霉素=102.2mg(2.041%)F68=16.0mg(0.32%)无菌水=4889.0mg(97.639%) | SP |
| 175 | 雷帕霉素=101.1mg(2.010%)吐温20=27.7mg(0.551%)无菌水=4901.0mg(97.439%) | SP |
| 176 | BSS+=0μl无菌水=0μl154号制剂=1000μl | S |
| 177 | BSS+=200μl无菌水=0μl154号制剂=800μl | SP |
| 178 | BSS+=400μl154号制剂=600μl | SP |
| 179 | BSS+=500μl154号制剂=500μl | SP |
| 180 | BSS+=600μl154号制剂=400μl | SP |
| 181 | BSS+=800μl154号制剂=200μl | SP |
| 182 | 无菌水=200μl154号制剂=800μl | SP |
| 制剂编号 | 组成(mg),%(w/w) | 制剂类型 |
| 183 | 无菌水=400μl154号制剂=600μl | SP |
| 184 | 无菌水=500μl154号制剂=500μl | SP |
| 185 | 无菌水=600μl154号制剂=400μl | SP |
| 186 | 无菌水=800μl154号制剂=200μl | SP |
| 187 | BSS+=2536.9mg(49.98%)154号制剂=2538.7mg(50.02%) | SP |
| 188 | 无菌水=2515.6mg(49.84%)154号制剂=2532.2mg(50.16%) | SP |
| 189 | F68=12.6mg(0.25%)无菌水=2524.7mg(49.79%)154号制剂=2533.1mg(49.96%) | SP |
| 190 | 雷帕霉素=2.0225g(2%)EtOH=3.65g(4%)PEG 400=94.0g(94%)BHT=0.002g(0.002%) | S |
| 191 | F68=12.1mg无菌水=2558.9mg154号制剂=2556.4mg | SP |
| 192 | F68=19.8mg无菌水=2564.1mg154号制剂=25557.5mg | SP |
| 193 | F68=25.3mg无菌水=2575.1mg154号制剂=2572.9mg | SP |
| 194 | F68=32.4mg无菌水=2572.1mg154号制剂=2562.1mg | SP |
| 195 | F68=38.3mg无菌水=2563.2mg154号制剂=2573.5mg | SP |
| 196 | F68=43.6mg无菌水=2541.1mg154号制剂=2556.0mg | SP |
| 197 | F68=51.2mg无菌水=2594.5mg154号制剂=2594.1mg | SP |
| 198 | PEG 400=1920g(96%)EtOH=80g(4%) | S |
| 199 | 168号制剂=1000μl | S |
| 200 | 168号制剂=200μl154号制剂=800μl | S |
| 201 | 168号制剂=400μl154号制剂=600μl | S |
| 202 | 168号制剂=500μl154号制剂=500μl | S |
| 203 | 168号制剂=600μl154号制剂=400μl | S |
| 制剂编号 | 组成(mg),%(w/w) | 制剂类型 |
| 204 | 168号制剂=800μl154号制剂=200μl | S |
| 205 | PEG 400=200μl154号制剂=800μl | S |
| 206 | PEG 400=400μl154号制剂=600μl | S |
| 207 | PEG 400=500μl154号制剂=500μl | S |
| 208 | PEG 400=600μl154号制剂=400μl | S |
| 209 | PEG 400=800μl154号制剂=200μl | S |
| 210 | Phosal 50PG=6735.0mg(99.002%)吐温80=67.9mg(0.998%) | S |
| 211 | 雷帕霉素=2.0047g(2%)EtOH=4.00g(4%)PEG 400=94.05g(94%) | S |
| 212 | Phosal 50PG=20.0662g(98.999%)吐温80=0.2029g(1.001%) | S |
| 213 | 154号制剂=100μl168号制剂=900μl | S |
| 214 | 154号制剂=100μl168号制剂=900μl | S |
| 215 | 154号制剂=100μl168号制剂=900μl | S |
| 216 | 154号制剂=100μlPEG 400=900μl | S |
| 217 | 154号制剂=100μlPEG 400=900μl | S |
| 218 | 154号制剂=100μlPEG 400=900μl | S |
| 219 | 154号制剂=100μlBSS+=900μl | SP |
| 220 | 154号制剂=100μlBSS+=900μl | SP |
| 221 | 154号制剂=100μlBSS+=900μl | SP |
| 222 | 154号制剂=1000μl | S |
| 223 | 154号制剂=1000μl | S |
| 224 | 154号制剂=100μl168号制剂=900μl | S |
| 225 | 154号制剂=100μl168号制剂=900μl | S |
| 226 | 154号制剂=100μl168号制剂=900μl | S |
| 227 | 154号制剂=100μlPEG 400=900μl | S |
| 228 | 154号制剂=100μlPEG 400=900μl | S |
| 制剂编号 | 组成(mg),%(w/w) | 制剂类型 |
| 229 | 154号制剂=100μlPEG 400=900μl | S |
| 230 | 154号制剂=100μlBSS+=900μl | SP |
| 231 | 154号制剂=100μlBSS+=900μl | SP |
| 232 | 154号制剂=100μlBSS+=900μl | SP |
| 233 | 154号制剂=200μl168号制剂=800μl | S |
| 234 | 154号制剂=200μl168号制剂=800μl | S |
| 235 | 154号制剂=200μl168号制剂=800μl | S |
| 236 | 154号制剂=200μl168号制剂=800μl | S |
| 237 | 154号制剂=200μlPEG 400=800μl | S |
| 238 | 154号制剂=200μlPEG 400=800μl | S |
| 239 | 154号制剂=200μlBSS+=800μl | SP |
| 240 | 154号制剂=200μlBSS+=800μl | SP |
| 241 | 154号制剂=200μlBSS+=800μl | SP |
| 242 | 154号制剂=100μl168号制剂=900μl | S |
| 243 | 154号制剂=100μlPEG 400=900μl | S |
| 244 | 154号制剂=100μlBSS+=900μl | SP |
| 245 | 154号制剂=100μlBSS+/CMC(0.5%)=900μl | SP |
| 246 | 154号制剂=400μl168号制剂=900μl | S |
| 247 | 154号制剂=400μlPEG 400=900μl | S |
| 248 | 154号制剂=400μlBSS+=900μl | SP |
| 249 | 154号制剂=400μlBSS+/CMC(0.5%)=900μl | SP |
| 250 | 154号制剂=100μlBSS+/CMC(0.5%)=900μl | SP |
| 251 | 154号制剂=100μlBSS+/CMC(0.5%)=900μl | SP |
| 252 | 154号制剂=100μlBSS+/CMC(0.5%)=900μl | SP |
| 253 | 154号制剂=200μlBSS+/CMC(0.5%)=800μl | SP |
| 制剂编号 | 组成(mg),%(w/w) | 制剂类型 |
| 294 | 无菌水+1%CMC中=4909.1mg(97.99%)雷帕霉素=100.5mg(2.01%) | SP |
| 295 | 无菌水+1%CMC高=4903.8mg(97.96%)雷帕霉素=101.9mg(2.04%) | SP |
| 296 | 雷帕霉素=40.5mg(2.03%)NMP=1958.7mg(97.97%) | S |
| 297 | 雷帕霉素=20.5mg(2.0%)DMA=41.4mg(4.0%)PVP=35.0mg(3.4%)H2O=934.7mg(90.6%) | SP |
| 298 | 雷帕霉素=10.6mg(2.0%)DMA=10.6mg(2.0%)PEG 400=506.1mg(96%) | S |
| 299 | 雷帕霉素=5.2mg(2.0%)1%DMA在PEG400中=257.4mg(98%) | SP |
| 300 | 雷帕霉素=20.0mg(2.0%)DMA=7.8mg(0.8%)PEG 400=974mg(97.2%) | S |
| 301 | 雷帕霉素=20.1mg(1.3%)DMA=19.5mg(1.3%)PEG 400=1449.6mg(97.3%) | S |
| 302 | 雷帕霉素=20.0mg(2.0%)PVP=10.8mg(1.1%)PEG 400=994.5mg(97.0%) | SP |
| 303 | 雷帕霉素=20.4mg(2.0%)PVP=24.5mg(2.4%)PEG 400=990.7mg(95.7%) | SP |
| 304 | 雷帕霉素=25.5mg(2.4%)PVP=51.9mg(4.8%)PEG 400=1000.6mg(92.8%) | SP |
| 305 | 雷帕霉素=22.5mg(2.3%)BA=27.5mg(2.7%)PEG 400=950.7mg(95.0%) | S |
| 306 | 雷帕霉素=30.2mg(2.3%)PVP=240.9mg(18.6%)PEG 400=1021.2mg(79.0%) | SP |
| 307 | 雷帕霉素=8.7mg(3.1%)1%PVP在水中=273mg(96.9%) | SP |
| 308 | 雷帕霉素=12.6mg(2.53%)5%PVP在水中=501.6mg(97.5%) | SP |
| 309 | 雷帕霉素=20.3mg(3.8%)10%PVP在水中=513.9mg(96.2%) | SP |
| 310 | 雷帕霉素=100.5mg(2.0%)DMA=67.8mg(1.4%)PEG 400=4838.3mg(96.6%) | S |
| 311 | 雷帕霉素=96.8mg(1.9%)BA=157.5mg(3.2%)PEG 400=4748.7mg(94.9%) | S |
| 制剂编号 | 组成(mg),%(w/w) | 制剂类型 |
| 312 | 雷帕霉素=105.8mg(2.1%)DMA=5.63mg(0.1%)PEG 400=4888.9mg(97.8%) | S |
| 313 | 雷帕霉素=20.2mg(2.0%)PVP=99.2mg(9.9%)H2O=882.3mg(88.1%) | SP |
| 314 | 雷帕霉素=100.3mg(2.0%)PVP=251.4mg(5.0%)H2O=4662.8mg(93.0%) | SP |
| 315 | 雷帕霉素=20.3mg(2.0%)DMA=983.9mg(98%) | S |
| 316 | 曲安西龙=22.8mg(2.0%)DMA=12.0mg(1.1%)PEG 400=1104.5mg(96.9%) | S |
| 317 | 曲安西龙=1.0mg(0.1%)EtOH=49.30mg(4.0%)PEG 400=1191.9mg(96.0%) | S |
| 318 | 曲安西龙=18.7mg(0.9%)PEG 400=959.8mg(99.1%) | S |
| 319 | 曲安西龙=25.5mg(1.3%)EtOH=83.0mg(4.1%)PEG 400=1905.6mg(94.6%) | S |
| 320 | 地塞米松=20.4mg(1.2%)EtOH=71.7mg(4.1%)PEG 400=1737.6mg(98.8%) | S |
| 321 | 地塞米松=27.5mg(2.0%)DMA=5.6mg(0.4%)PEG 400=1347.3mg(97.6%) | S |
| 322 | 雷帕霉素=9.1mg(0.152%)EtOH=90.9mg(1.514%)F127=262.8mg(4.378%)水=1489.1mg(24.804%)芝麻油=4151.5mg(69.152%) | E |
| 323 | 雷帕霉素=24.4mg(0.625%)Phosal 50PG=203.1mg(5.201%)EtOH=166.8mg(4.272%)Labrafac CC=1502.8mg(38.486%)芝麻油=2007.7mg(51.416%) | E |
| 324 | 含有2mm珠的174号制剂 | SP |
| 325 | 含有2mm珠的175号制剂 | SP |
| 326 | 雷帕霉素=51mg(1.47%)EtOH=407.7mg(11.77%)Cremophor EL=1502.9mg(43.44%)Capmul PG8=1502.9mg(43.44%) | SEF |
| 327 | 雷帕霉素=60.1mg(1.956%)EtOH=125.0mg(4.067%)Caprol MPGO=1444.1mg(46.989%)Softigen 767=1444.1mg(46.989%) | SEF |
Claims (24)
1.液体制剂,该液体制剂包含选自雷帕霉素和其药学上可接受的盐的治疗物质,其中所述液体制剂具有不大于20%的在溶解的气体中的氧气百分数,并且其中所述液体制剂不包含抗氧化剂。
2.权利要求1的液体制剂,其中所述液体制剂具有不大于17.5%的在溶解的气体中的氧气百分数。
3.权利要求2的液体制剂,其中所述液体制剂具有不大于16.5%的在溶解的气体中的氧气百分数。
4.权利要求1的液体制剂,其中在25℃和60%相对湿度经过至少2周的时间,所述治疗物质的制剂强度是至少80%,其中所述制剂强度是相对于制剂刚刚被制备时在制剂中存在的治疗物质的重量而言,在特定时间时制剂中存在的治疗物质的重量百分数。
5.权利要求4的液体制剂,其中在25℃和60%相对湿度经过至少2周的时间,治疗物质的制剂强度是至少90%。
6.权利要求5的液体制剂,其中在25℃和60%相对湿度经过至少1个月的时间,治疗物质的制剂强度是至少90%。
7.权利要求5的液体制剂,其中在25℃和60%相对湿度经过至少2个月的时间,治疗物质的制剂强度是至少90%。
8.权利要求5的液体制剂,其中在25℃和60%相对湿度经过至少3个月的时间,治疗物质的制剂强度是至少90%。
9.权利要求4的液体制剂,其中在5℃经过至少3个月的时间,治疗物质的制剂强度是至少90%。
10.权利要求9的液体制剂,其中在5℃经过至少1年的时间,治疗物质的制剂强度是至少90%。
11.权利要求9的液体制剂,其中在5℃经过至少2年的时间,治疗物质的制剂强度是至少90%。
12.权利要求1、5和9中的任何一项的液体制剂,其中液体制剂在被次级包装包围的容器中,以减少液体制剂所接触的光的量。
13.权利要求1的液体制剂,其另外包含液体聚乙二醇。
14.权利要求13的液体制剂,其中雷帕霉素占2%w/w,液体聚乙二醇是PEG 400,且PEG 400占94%w/w,且液体制剂另外包含占4%w/w的乙醇。
15.液体制剂,该液体制剂包含选自雷帕霉素和其药学上可接受的盐的治疗物质,其中所述液体制剂具有不大于20%的在溶解的气体中的氧气百分数,并且其中所述液体制剂不包含抗氧化剂,其中所述抗氧化剂为抗坏血酸、柠檬酸、亚硫酸钠、EDTA二钠、二硫苏糖醇、延胡索酸、β-羟基苯甲醚、没食子酸丙酯、α和β-生育酚、甲苯磺酸、酒石酸、硫代甘油、硫脲、甲醛合次硫酸氢钠、硫代硫酸钠、谷氨酸、丁基化羟基甲苯、抗坏血酸棕榈酸酯、苄醇、苯扎氯铵和马来酸。
16.密封容器,该密封容器包含含有雷帕霉素或其药学上可接受的盐的液体制剂,其中所述液体制剂与含有不多于20%氧气的顶空气体接触,并且其中所述液体制剂不包含抗氧化剂。
17.权利要求16的密封容器,其中液体制剂与含有不多于10%氧气的顶空气体接触。
18.权利要求16的密封容器,其中液体制剂与含有不多于5%氧气的顶空气体接触。
19.权利要求16的密封容器,其中顶空体积与液体制剂体积的比率不大于1.5。
20.权利要求19的密封容器,其中顶空体积与液体制剂体积的比率不大于0.5。
21.权利要求16的密封容器,相对液体制剂中的每毫克活性物质,其在顶空中含有不大于1μl的氧气。
22.权利要求21的密封容器,相对液体制剂中的每毫克活性物质,其在顶空中含有不大于0.5μl的氧气。
23.权利要求16、17和18中任何一项的密封容器,其中密封容器是预填装的注射器。
24.密封容器,该密封容器包含含有雷帕霉素或其药学上可接受的盐的液体制剂,其中所述液体制剂与含有不多于20%氧气的顶空气体接触,并且其中所述液体制剂不包含抗氧化剂,其中所述抗氧化剂为抗坏血酸、柠檬酸、亚硫酸钠、EDTA二钠、二硫苏糖醇、延胡索酸、β-羟基苯甲醚、没食子酸丙酯、α和β-生育酚、甲苯磺酸、酒石酸、硫代甘油、硫脲、甲醛合次硫酸氢钠、硫代硫酸钠、谷氨酸、丁基化羟基甲苯、抗坏血酸棕榈酸酯、苄醇、苯扎氯铵和马来酸。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US77201806P | 2006-02-09 | 2006-02-09 | |
| US60/772,018 | 2006-02-09 | ||
| PCT/US2007/003573 WO2007092620A2 (en) | 2006-02-09 | 2007-02-09 | Stable formulations, and methods of their preparation and use |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN101605529A CN101605529A (zh) | 2009-12-16 |
| CN101605529B true CN101605529B (zh) | 2013-03-13 |
Family
ID=38261629
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2007800049514A Active CN101605529B (zh) | 2006-02-09 | 2007-02-09 | 稳定制剂及它们的制备和使用方法 |
Country Status (9)
| Country | Link |
|---|---|
| US (2) | US8492400B2 (zh) |
| EP (1) | EP2001438A2 (zh) |
| JP (1) | JP5528708B2 (zh) |
| KR (2) | KR20140093764A (zh) |
| CN (1) | CN101605529B (zh) |
| AU (1) | AU2007212271B2 (zh) |
| BR (1) | BRPI0707612B8 (zh) |
| CA (1) | CA2635797C (zh) |
| WO (1) | WO2007092620A2 (zh) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN107334734A (zh) * | 2017-07-10 | 2017-11-10 | 浙江大学 | 一种西罗莫司或其衍生物的眼用制剂 |
Families Citing this family (64)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8673341B2 (en) * | 2004-04-30 | 2014-03-18 | Allergan, Inc. | Intraocular pressure reduction with intracameral bimatoprost implants |
| US9498457B2 (en) | 2004-04-30 | 2016-11-22 | Allergan, Inc. | Hypotensive prostamide-containing biodegradable intraocular implants and related implants |
| US8722097B2 (en) | 2004-04-30 | 2014-05-13 | Allergan, Inc. | Oil-in-water method for making polymeric implants containing a hypotensive lipid |
| US8663639B2 (en) | 2005-02-09 | 2014-03-04 | Santen Pharmaceutical Co., Ltd. | Formulations for treating ocular diseases and conditions |
| DK1848431T3 (en) | 2005-02-09 | 2016-04-18 | Santen Pharmaceutical Co Ltd | LIQUID FORMULATIONS FOR TREATMENT OF DISEASES OR CONDITIONS |
| JP2008533204A (ja) * | 2005-03-21 | 2008-08-21 | マクサイト, インコーポレイテッド | 病気又は症状の治療のためのドラッグ送達システム |
| JP4358785B2 (ja) * | 2005-05-27 | 2009-11-04 | 麒麟麦酒株式会社 | 密封容器内の酸素量の測定方法及びこれに用いる密封容器のピアス装置 |
| JP5528708B2 (ja) | 2006-02-09 | 2014-06-25 | 参天製薬株式会社 | 安定な製剤ならびにそれらを調製および使用する方法 |
| CN101443004B (zh) | 2006-03-23 | 2013-03-06 | 参天制药株式会社 | 用于与血管通透性有关的疾病或病症的制剂 |
| US9386770B2 (en) * | 2006-06-13 | 2016-07-12 | Phibro Animal Health Corp. | Use of predissolved pristinamycin-type and polyether ionophore type antimicrobial agents in the production of ethanol |
| WO2009018333A2 (en) * | 2007-07-30 | 2009-02-05 | Board Of Supervisors Of Louisiana State University And Agricultural And Mechanical College | Dha and pedf, a therapeutic composition for nerve and retinal pigment epithelial cells |
| ES2584904T3 (es) * | 2007-09-10 | 2016-09-30 | Boston Biomedical, Inc. | Nuevas composiciones y métodos para el tratamiento del cáncer |
| KR20100072333A (ko) * | 2007-11-01 | 2010-06-30 | 보오슈 앤드 롬 인코포레이팃드 | 약물 전달을 위한 비히클로서의 비-수성 수혼화성 물질 |
| MX2010012080A (es) * | 2008-05-05 | 2011-04-11 | Univ Winthrop Hospital | Metodo para mejorar el perfil de riesgo cardiovascular de los inhibidores de cox. |
| WO2010006306A1 (en) * | 2008-07-10 | 2010-01-14 | Inspire Pharmaceuticals, Inc. | Method of treating blepharitis |
| CN102231969A (zh) * | 2008-10-03 | 2011-11-02 | 万能医药公司 | 大环内酯化合物及其使用方法 |
| WO2010085572A1 (en) * | 2009-01-23 | 2010-07-29 | Inspire Pharmaceuticals, Inc. | Method of treating dry eye disease with azithromycin |
| US20110305747A1 (en) * | 2009-07-30 | 2011-12-15 | Allergan, Inc. | Combination of dapsone with other anti-acne agents |
| TWI492769B (zh) | 2009-09-23 | 2015-07-21 | Alcon Res Ltd | 可注射的水性眼用組成物及其使用之方法 |
| EP2394636B1 (en) * | 2010-05-28 | 2014-03-19 | Novagali Pharma S.A. | Method for treating retinal conditions using an intraocular tamponade |
| EP2361636A1 (en) * | 2010-02-26 | 2011-08-31 | CSL Behring AG | Immunoglobulin preparation and storage system for an immunoglobulin preparation |
| TW201138782A (en) * | 2010-04-26 | 2011-11-16 | Besins Healthcare Lu Sarl | Low-oil pharmaceutical emulsion compositions comprising progestogen |
| AU2011260016B2 (en) * | 2010-06-02 | 2013-08-22 | Fresenius Kabi Oncology Ltd. | Stable pharmaceutical compositions of Rapamycin esters |
| CA2814805C (en) | 2010-10-21 | 2021-11-02 | Rtu Pharmaceuticals, Llc | Ready to use ketorolac formulations |
| US9504664B2 (en) | 2010-10-29 | 2016-11-29 | Infirst Healthcare Limited | Compositions and methods for treating severe pain |
| US8895537B2 (en) | 2010-10-29 | 2014-11-25 | Infirst Healthcare Ltd. | Compositions and methods for treating cardiovascular diseases |
| US10695432B2 (en) | 2010-10-29 | 2020-06-30 | Infirst Healthcare Limited | Solid solution compositions and use in severe pain |
| US11224659B2 (en) | 2010-10-29 | 2022-01-18 | Infirst Healthcare Limited | Solid solution compositions and use in severe pain |
| US9308213B2 (en) | 2010-10-29 | 2016-04-12 | Infirst Healthcare Limited | Solid solution compositions and use in chronic inflammation |
| US10695431B2 (en) | 2010-10-29 | 2020-06-30 | Infirst Healthcare Limited | Solid solution compositions and use in cardiovascular disease |
| US9271950B2 (en) | 2010-10-29 | 2016-03-01 | Infirst Healthcare Limited | Compositions for treating chronic inflammation and inflammatory diseases |
| US9744132B2 (en) | 2010-10-29 | 2017-08-29 | Infirst Healthcare Limited | Solid solution compositions and use in chronic inflammation |
| US11202831B2 (en) | 2010-10-29 | 2021-12-21 | Infirst Healthcare Limited | Solid solution compositions and use in cardiovascular disease |
| US9737500B2 (en) | 2010-10-29 | 2017-08-22 | Infirst Healthcare Limited | Compositions and methods for treating severe pain |
| US11730709B2 (en) | 2010-10-29 | 2023-08-22 | Infirst Healthcare Limited | Compositions and methods for treating severe pain |
| US8349005B2 (en) | 2011-01-03 | 2013-01-08 | Masatoshi Murata | Method for burying implant to choroid |
| US20120219682A1 (en) * | 2011-02-28 | 2012-08-30 | Frank Monteleone | Antimicrobial compositions within antioxidant solutions used to protect whole protein foods |
| DE102011108948A1 (de) * | 2011-07-29 | 2013-01-31 | Achim Göpferich | Wässrige, kolloidale Lösungen von lipophilen Substanzen,insbesondere Arzneistofflösungen |
| CN102319207A (zh) * | 2011-08-01 | 2012-01-18 | 福建省微生物研究所 | 42-(二甲基亚膦酰)雷帕霉素液体组合物 |
| US8912215B2 (en) | 2011-12-13 | 2014-12-16 | Everon Biosciences, Inc. | Rapamycin composition |
| AU2013355043A1 (en) * | 2012-12-06 | 2015-07-02 | Tobira Therapeutics, Inc. | Oligonucleotide formulation |
| JP6433085B2 (ja) | 2013-04-09 | 2018-12-05 | ボストン バイオメディカル, インコーポレイテッド | がんの処置に使用するための2−アセチルナフト[2,3−b]フラン−4,9−ジオン |
| PL3119794T3 (pl) | 2014-06-25 | 2018-04-30 | NuCana plc | Preparat zawierający prolek gemcytabiny |
| HRP20230584T1 (hr) | 2014-06-25 | 2023-09-15 | NuCana plc | Prolijekovi gemcitabina |
| GB201512728D0 (en) * | 2015-07-20 | 2015-08-26 | Isis Innovation | Nanoencapsulated oxygen |
| GB201522764D0 (en) | 2015-12-23 | 2016-02-03 | Nucana Biomed Ltd | Formulations of phosphate derivatives |
| US20170239250A1 (en) | 2016-02-19 | 2017-08-24 | Eagle Pharmaceuticals, Inc. | Pemetrexed formulations |
| JP6944958B2 (ja) | 2016-05-25 | 2021-10-06 | 参天製薬株式会社 | 持続性浮腫を伴う滲出性加齢黄斑変性の処置のためのシロリムスの使用 |
| CA2972296A1 (en) | 2016-06-30 | 2017-12-30 | Durect Corporation | Depot formulations |
| US10682340B2 (en) | 2016-06-30 | 2020-06-16 | Durect Corporation | Depot formulations |
| JP7106563B2 (ja) | 2016-11-29 | 2022-07-26 | スミトモ ファーマ オンコロジー, インコーポレイテッド | ナフトフラン誘導体、その調製、および使用方法 |
| CA3049543A1 (en) * | 2017-01-06 | 2018-07-12 | Santen Pharmaceutical Co., Ltd. | Intratumoral administration of sirolimus for treatment of prostate cancer |
| US11065217B2 (en) | 2017-01-27 | 2021-07-20 | Temple University—Of the Commonwealth System of Higher Education | Use of short chain fatty acids for the treatment and prevention of diseases and disorders |
| JP6195028B1 (ja) * | 2017-02-02 | 2017-09-13 | セントラル硝子株式会社 | α,α−ジフルオロアセトアルデヒドアルキルヘミアセタールの保存方法 |
| US11285081B2 (en) | 2017-02-17 | 2022-03-29 | Santen Pharmaceutical Co., Ltd. | Sealed preparation container and use for same |
| CA3062656A1 (en) | 2017-05-17 | 2018-11-22 | Boston Biomedical, Inc. | Methods for treating cancer |
| US10532221B2 (en) * | 2017-08-17 | 2020-01-14 | Justin C. Quon | Method of noninvasive treatment of diabetic retinopathy |
| EP3691654A4 (en) | 2017-09-25 | 2021-11-24 | Surface Pharmaceuticals, Inc. | OPHTHALMIC PHARMACEUTICAL COMPOSITIONS AND METHODS FOR TREATMENT OF EYE SURFACE DISEASES |
| US20210213045A1 (en) * | 2017-11-20 | 2021-07-15 | Veloce Biopharma Llc | Novel ophthalmic composition and methods of use |
| MX2020006425A (es) * | 2017-12-21 | 2023-01-12 | Siemens Healthcare Diagnostics Inc | Composiciones que comprenden oxígeno estabilizado y métodos para formar las mismas. |
| WO2019135779A1 (en) * | 2018-01-08 | 2019-07-11 | Veloce Biopharma, Llc | Novel ophthalmic composition and methods of use |
| CN111712231A (zh) * | 2018-02-23 | 2020-09-25 | 百多力股份公司 | 用于40-o-环状烃酯和相关结构的肠胃外制剂材料和方法 |
| EA202092974A1 (ru) * | 2018-06-01 | 2021-04-09 | Байер Кропсайенс Лп | Стабилизированная фунгицидная композиция, содержащая циклодекстрин |
| KR102351951B1 (ko) * | 2020-05-06 | 2022-01-17 | 한국원자력연구원 | 결핵균을 검출하는 방법 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1374872A (zh) * | 1998-12-07 | 2002-10-16 | 诺瓦提斯公司 | 大环内酯的稳定化 |
| CN1556694A (zh) * | 2000-06-06 | 2004-12-22 | ���չ�˾ | 对氧化作用敏感的活性组分水溶液制剂的制备方法 |
| CN1671385A (zh) * | 2002-07-30 | 2005-09-21 | 惠氏公司 | 含有瑞帕霉素羟基酯的胃肠外制剂 |
Family Cites Families (249)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3416530A (en) | 1966-03-02 | 1968-12-17 | Richard A. Ness | Eyeball medication dispensing tablet |
| US3630200A (en) | 1969-06-09 | 1971-12-28 | Alza Corp | Ocular insert |
| US3828777A (en) | 1971-11-08 | 1974-08-13 | Alza Corp | Microporous ocular device |
| US3914402A (en) | 1973-06-14 | 1975-10-21 | Alza Corp | Ophthalmic dosage form, for releasing medication over time |
| US3926188A (en) | 1974-11-14 | 1975-12-16 | Alza Corp | Laminated drug dispenser |
| US4093709A (en) | 1975-01-28 | 1978-06-06 | Alza Corporation | Drug delivery devices manufactured from poly(orthoesters) and poly(orthocarbonates) |
| US4014335A (en) | 1975-04-21 | 1977-03-29 | Alza Corporation | Ocular drug delivery device |
| FR2382240A1 (fr) * | 1977-03-03 | 1978-09-29 | Mouls Pierre | Dispositif permettant d'instiller des liquides medicamenteux dans l'oeil |
| US4300557A (en) | 1980-01-07 | 1981-11-17 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Method for treating intraocular malignancies |
| AU543727B2 (en) | 1980-06-02 | 1985-05-02 | Ayerst Mckenna & Harrison Inc. | Injectable composition of rapamycin |
| IT1141715B (it) | 1980-06-06 | 1986-10-08 | Sadepan Chimica Spa | Collante a base di resina urea-formaldeide additivato con ligninsolfonato di calcio e/o ammonio,resina urea formaldeide modificata con ligninsolfonato di calcio e/o ammonio e metodo di produzione degli stessi,per la preparazione di pannelli agglomerati di legno |
| US4316885A (en) | 1980-08-25 | 1982-02-23 | Ayerst, Mckenna And Harrison, Inc. | Acyl derivatives of rapamycin |
| US4650803A (en) | 1985-12-06 | 1987-03-17 | University Of Kansas | Prodrugs of rapamycin |
| US5322691A (en) | 1986-10-02 | 1994-06-21 | Sohrab Darougar | Ocular insert with anchoring protrusions |
| US5147647A (en) | 1986-10-02 | 1992-09-15 | Sohrab Darougar | Ocular insert for the fornix |
| KR920003601B1 (ko) | 1987-09-03 | 1992-05-04 | 유니버시티 어브 죠지아 리서취 화운데이션 인코포레이티드 | 점안 싸이클로스포린(cyclosporin)의 조성물 |
| US4997652A (en) | 1987-12-22 | 1991-03-05 | Visionex | Biodegradable ocular implants |
| US4853224A (en) | 1987-12-22 | 1989-08-01 | Visionex | Biodegradable ocular implants |
| EP0356399A3 (en) | 1988-08-26 | 1991-03-20 | Sandoz Ag | Substituted 4-azatricyclo (22.3.1.04.9) octacos-18-ene derivatives, their preparation and pharmaceutical compositions containing them |
| US4946450A (en) | 1989-04-18 | 1990-08-07 | Biosource Genetics Corporation | Glucan/collagen therapeutic eye shields |
| US5100899A (en) | 1989-06-06 | 1992-03-31 | Roy Calne | Methods of inhibiting transplant rejection in mammals using rapamycin and derivatives and prodrugs thereof |
| US5164188A (en) | 1989-11-22 | 1992-11-17 | Visionex, Inc. | Biodegradable ocular implants |
| US5883082A (en) | 1990-08-14 | 1999-03-16 | Isis Pharmaceuticals, Inc. | Compositions and methods for preventing and treating allograft rejection |
| US5192773A (en) | 1990-07-02 | 1993-03-09 | Vertex Pharmaceuticals, Inc. | Immunosuppressive compounds |
| JPH04230389A (ja) | 1990-07-16 | 1992-08-19 | American Home Prod Corp | ラパマイシン誘導体 |
| DE4022553A1 (de) | 1990-07-16 | 1992-01-23 | Hund Helmut Gmbh | Vorrichtung zur hochreproduzierbaren applikation definierter volumina von loesungen und suspensionen diagnostisch oder therapeutisch wirksamer substanzen auf der cornea-oberflaeche |
| US5023262A (en) | 1990-08-14 | 1991-06-11 | American Home Products Corporation | Hydrogenated rapamycin derivatives |
| PT98990A (pt) | 1990-09-19 | 1992-08-31 | American Home Prod | Processo para a preparacao de esteres de acidos carboxilicos de rapamicina |
| US5290892A (en) | 1990-11-07 | 1994-03-01 | Nestle S.A. | Flexible intraocular lenses made from high refractive index polymers |
| IE65341B1 (en) | 1990-11-08 | 1995-10-18 | Fujisawa Pharmaceutical Co | Suspensions containing tricyclic compounds |
| US5378475A (en) | 1991-02-21 | 1995-01-03 | University Of Kentucky Research Foundation | Sustained release drug delivery devices |
| US5078999A (en) | 1991-02-22 | 1992-01-07 | American Home Products Corporation | Method of treating systemic lupus erythematosus |
| US5120842A (en) | 1991-04-01 | 1992-06-09 | American Home Products Corporation | Silyl ethers of rapamycin |
| JP3158437B2 (ja) | 1991-04-26 | 2001-04-23 | 藤沢薬品工業株式会社 | 眼疾患に対するマクロライド化合物の使用 |
| US5565560A (en) | 1991-05-13 | 1996-10-15 | Merck & Co., Inc. | O-Aryl,O-alkyl,O-alkenyl and O-alkynylmacrolides having immunosuppressive activity |
| US5120727A (en) | 1991-05-29 | 1992-06-09 | American Home Products Corporation | Rapamycin dimers |
| US5120725A (en) | 1991-05-29 | 1992-06-09 | American Home Products Corporation | Bicyclic rapamycins |
| IL102414A (en) | 1991-07-25 | 1996-08-04 | Univ Louisville Res Found | Medicinal preparations for the treatment of ocular inflammation, containing rapamycin |
| US5189042A (en) | 1991-08-22 | 1993-02-23 | Merck & Co. Inc. | Fluoromacrolides having immunosuppressive activity |
| US5457111A (en) | 1991-09-05 | 1995-10-10 | Abbott Laboratories | Macrocyclic immunomodulators |
| US5192802A (en) | 1991-09-25 | 1993-03-09 | Mcneil-Ppc, Inc. | Bioadhesive pharmaceutical carrier |
| US5679666A (en) | 1991-11-22 | 1997-10-21 | Alcon Laboratories, Inc. | Prevention and treatment of ocular neovascularization by treatment with angiostatic steroids |
| US5770592A (en) | 1991-11-22 | 1998-06-23 | Alcon Laboratories, Inc. | Prevention and treatment of ocular neovascularization using angiostatic steroids |
| US5516781A (en) | 1992-01-09 | 1996-05-14 | American Home Products Corporation | Method of treating restenosis with rapamycin |
| US5177203A (en) | 1992-03-05 | 1993-01-05 | American Home Products Corporation | Rapamycin 42-sulfonates and 42-(N-carboalkoxy) sulfamates useful as immunosuppressive agents |
| SG49652A1 (en) | 1992-03-30 | 1998-06-15 | American Home Prod | Rapamycin formulation for iv injection |
| US5178635A (en) | 1992-05-04 | 1993-01-12 | Allergan, Inc. | Method for determining amount of medication in an implantable device |
| FR2690846B1 (fr) | 1992-05-05 | 1995-07-07 | Aiache Jean Marc | Forme galenique pour administration oculaire et procede de preparation. |
| WO1994005257A1 (en) | 1992-09-08 | 1994-03-17 | Allergan, Inc. | Sustained release of ophthalmic drugs from a soluble polymer drug delivery vehicle |
| GB9221220D0 (en) | 1992-10-09 | 1992-11-25 | Sandoz Ag | Organic componds |
| US5258389A (en) | 1992-11-09 | 1993-11-02 | Merck & Co., Inc. | O-aryl, O-alkyl, O-alkenyl and O-alkynylrapamycin derivatives |
| JP3520517B2 (ja) | 1992-11-18 | 2004-04-19 | 藤沢薬品工業株式会社 | 医薬用持続性製剤 |
| EP0689545A4 (en) | 1993-03-17 | 1996-04-24 | Abbott Lab | IMMUNOREGULATORS WITH MACROCYCLIC AMIDE AND UREA |
| GB2278780B (en) | 1993-05-27 | 1998-10-14 | Sandoz Ltd | Macrolide formulations |
| US5798355A (en) | 1995-06-07 | 1998-08-25 | Gpi Nil Holdings, Inc. | Inhibitors of rotamase enzyme activity |
| EP2226085B1 (en) | 1993-07-19 | 2013-11-27 | Angiotech Pharmaceuticals, Inc. | Anti-angiogenic compositions and methods of use |
| WO1995003009A1 (en) | 1993-07-22 | 1995-02-02 | Oculex Pharmaceuticals, Inc. | Method of treatment of macular degeneration |
| US5616588A (en) | 1993-09-30 | 1997-04-01 | American Home Products Corporation | Rapamycin formulation for IV injection |
| AU688782B2 (en) * | 1993-09-30 | 1998-03-19 | Wyeth | Rapamycin formulations for oral administration |
| US5536729A (en) * | 1993-09-30 | 1996-07-16 | American Home Products Corporation | Rapamycin formulations for oral administration |
| IL111004A (en) | 1993-09-30 | 1998-06-15 | American Home Prod | Oral formulations of rapamycin |
| US5516770A (en) | 1993-09-30 | 1996-05-14 | American Home Products Corporation | Rapamycin formulation for IV injection |
| US5443505A (en) | 1993-11-15 | 1995-08-22 | Oculex Pharmaceuticals, Inc. | Biocompatible ocular implants |
| EP0729471A1 (en) | 1993-11-19 | 1996-09-04 | Abbott Laboratories | Semisynthetic analogs of rapamycin (macrolides) being immunomodulators |
| US5527907A (en) | 1993-11-19 | 1996-06-18 | Abbott Laboratories | Macrolide immunomodulators |
| DE69423781T2 (de) | 1993-12-17 | 2000-08-10 | Novartis Ag | Rapamycin-derivate als immunosuppressoren |
| US5788687A (en) | 1994-02-01 | 1998-08-04 | Caphco, Inc | Compositions and devices for controlled release of active ingredients |
| US5773021A (en) | 1994-03-14 | 1998-06-30 | Vetoquinol S.A. | Bioadhesive ophthalmic insert |
| US5516522A (en) | 1994-03-14 | 1996-05-14 | Board Of Supervisors Of Louisiana State University | Biodegradable porous device for long-term drug delivery with constant rate release and method of making the same |
| EP0754046A1 (en) | 1994-04-04 | 1997-01-22 | FREEMAN, William R. | Use of phosphonylmethoxyalkyl nucleosides for the treatment of raised intraocular pressure |
| US5466233A (en) | 1994-04-25 | 1995-11-14 | Escalon Ophthalmics, Inc. | Tack for intraocular drug delivery and method for inserting and removing same |
| US5621108A (en) | 1994-12-05 | 1997-04-15 | Trustees Of The University Of Pennsylvania | Processes and intermediates for preparing macrocycles |
| US5725493A (en) | 1994-12-12 | 1998-03-10 | Avery; Robert Logan | Intravitreal medicine delivery |
| JPH08333257A (ja) * | 1995-04-04 | 1996-12-17 | Otsuka Pharmaceut Co Ltd | 塩酸プロカテロール水溶液製剤収容製品及び塩酸プロカテロール水溶液製剤 |
| AU5857396A (en) | 1995-05-14 | 1996-11-29 | Optonol Ltd. | Intraocular implant, delivery device, and method of implanta tion |
| US5696135A (en) | 1995-06-07 | 1997-12-09 | Gpi Nil Holdings, Inc. | Inhibitors of rotamase enzyme activity effective at stimulating neuronal growth |
| WO1996041865A1 (en) | 1995-06-07 | 1996-12-27 | Ariad Gene Therapeutics, Inc. | Rapamcycin-based regulation of biological events |
| US5614547A (en) | 1995-06-07 | 1997-03-25 | Guilford Pharmaceuticals Inc. | Small molecule inhibitors of rotamase enzyme |
| US6037370A (en) | 1995-06-08 | 2000-03-14 | Vertex Pharmaceuticals Incorporated | Methods and compositions for stimulating neurite growth |
| BE1009856A5 (fr) | 1995-07-14 | 1997-10-07 | Sandoz Sa | Composition pharmaceutique sous la forme d'une dispersion solide comprenant un macrolide et un vehicule. |
| JP3266005B2 (ja) | 1995-09-19 | 2002-03-18 | 藤沢薬品工業株式会社 | エアゾール製剤およびその製造方法 |
| US5773019A (en) | 1995-09-27 | 1998-06-30 | The University Of Kentucky Research Foundation | Implantable controlled release device to deliver drugs directly to an internal portion of the body |
| WO1997016068A1 (en) | 1995-10-31 | 1997-05-09 | Merck & Co., Inc. | Triterpene derivatives with immunosuppressant activity |
| GB9601120D0 (en) | 1996-01-19 | 1996-03-20 | Sandoz Ltd | Organic compounds |
| EP0880362B1 (en) | 1996-02-13 | 2005-05-25 | G.D. SEARLE & CO. | Compositions comprising a cyclooxygenase-2 inhibitor and a leukotriene b 4 receptor antagonist |
| US5743274A (en) | 1996-03-18 | 1998-04-28 | Peyman; Gholam A. | Macular bandage for use in the treatment of subretinal neovascular members |
| US5904144A (en) | 1996-03-22 | 1999-05-18 | Cytotherapeutics, Inc. | Method for treating ophthalmic diseases |
| JP3309175B2 (ja) | 1996-03-25 | 2002-07-29 | 参天製薬株式会社 | タンパク性薬物含有強膜プラグ |
| GB9710962D0 (en) | 1997-05-28 | 1997-07-23 | Univ Cambridge Tech | Polyketides and their synthesis |
| RU2123314C1 (ru) | 1996-06-27 | 1998-12-20 | Павлова Татьяна Вячеславовна | Способ постановки ирригационной системы в теноново пространство |
| SI1208847T1 (sl) | 1996-07-30 | 2007-06-30 | Novartis Ag | Farmacevtski sestavki za zdravljenje stanj zavračanja transplantatov in avtoimunskih ali vnetnih stanj |
| US6142969A (en) | 1996-10-25 | 2000-11-07 | Anamed, Inc. | Sutureless implantable device and method for treatment of glaucoma |
| US6007510A (en) | 1996-10-25 | 1999-12-28 | Anamed, Inc. | Implantable devices and methods for controlling the flow of fluids within the body |
| AUPO427196A0 (en) | 1996-12-19 | 1997-01-23 | University Of Sydney, The | A method for preventing or controlling cataract |
| TW450810B (en) | 1997-02-20 | 2001-08-21 | Fujisawa Pharmaceutical Co | Macrolides antibiotic pharmaceutical composition for preventing and treating skin diseases |
| US6273913B1 (en) | 1997-04-18 | 2001-08-14 | Cordis Corporation | Modified stent useful for delivery of drugs along stent strut |
| EP1003569B1 (en) | 1997-08-11 | 2004-10-20 | Allergan, Inc. | Sterile bioerodible implant device containing retinoid with improved biocompatability and method of manufacture |
| US5902598A (en) | 1997-08-28 | 1999-05-11 | Control Delivery Systems, Inc. | Sustained release drug delivery devices |
| US6342507B1 (en) | 1997-09-05 | 2002-01-29 | Isotechnika, Inc. | Deuterated rapamycin compounds, method and uses thereof |
| US20060198867A1 (en) | 1997-09-25 | 2006-09-07 | Abbott Laboratories, Inc. | Compositions and methods of administering rapamycin analogs using medical devices for long-term efficacy |
| US6890546B2 (en) | 1998-09-24 | 2005-05-10 | Abbott Laboratories | Medical devices containing rapamycin analogs |
| US6015815A (en) | 1997-09-26 | 2000-01-18 | Abbott Laboratories | Tetrazole-containing rapamycin analogs with shortened half-lives |
| US20030190286A1 (en) | 1997-10-01 | 2003-10-09 | Dugger Harry A. | Buccal, polar and non-polar spray or capsule containing drugs for treating allergies or asthma |
| GB9721497D0 (en) * | 1997-10-09 | 1997-12-10 | Ciba Geigy Ag | Organic compounds |
| IL135774A0 (en) | 1997-10-22 | 2001-05-20 | Ponikau Jens | Use of antinfungal agents for the topical treatment of fungus-induced mucositis |
| ZA989885B (en) | 1997-10-31 | 1999-05-05 | Abbott Lab | Use of macrolides for the treatment of cancer and macular degeneration |
| CZ287497B6 (cs) | 1997-12-30 | 2000-12-13 | Galena, A. S. | Topické oční přípravky s imunosupresivními látkami |
| AU2337599A (en) | 1998-01-23 | 1999-08-09 | Microcide Pharmaceuticals, Inc. | Efflux pump inhibitors |
| DE19810655A1 (de) | 1998-03-12 | 1999-09-16 | Univ Eberhard Karls | Arzneimittel mit einem Gehalt an Ciclosporin |
| JP2002506028A (ja) | 1998-03-13 | 2002-02-26 | ジョンズ ホプキンズ ユニヴァーシティ スクール オヴ メディシン | 糖尿病性網膜症または眼炎症の処置におけるゲニステインのようなタンパク質チロシンインヒビターの使用 |
| EP1083896A4 (en) | 1998-05-11 | 2002-09-11 | Endowment For Res In Human Bio | USE OF NEOMYCIN FOR TREATING ANGIOGENESIS-RELATED DISEASES |
| US6399629B1 (en) | 1998-06-01 | 2002-06-04 | Microcide Pharmaceuticals, Inc. | Efflux pump inhibitors |
| WO2000006121A1 (de) * | 1998-07-24 | 2000-02-10 | Jago Research Ag | Medizinische aerosolformulierungen |
| US6378526B1 (en) | 1998-08-03 | 2002-04-30 | Insite Vision, Incorporated | Methods of ophthalmic administration |
| US6376517B1 (en) | 1998-08-14 | 2002-04-23 | Gpi Nil Holdings, Inc. | Pipecolic acid derivatives for vision and memory disorders |
| US7338976B1 (en) | 1998-08-14 | 2008-03-04 | Gpi Nil Holdings, Inc. | Heterocyclic esters or amides for vision and memory disorders |
| US6384056B1 (en) | 1998-08-14 | 2002-05-07 | Gpi Nil Holdings, Inc. | Heterocyclic thioesters or ketones for vision and memory disorders |
| US6632836B1 (en) | 1998-10-30 | 2003-10-14 | Merck & Co., Inc. | Carbocyclic potassium channel inhibitors |
| US6303637B1 (en) | 1998-10-30 | 2001-10-16 | Merck & Co., Inc. | Heterocyclic potassium channel inhibitors |
| US6472370B1 (en) | 1998-11-17 | 2002-10-29 | Ortho-Mcneil Pharmaceutical, Inc. | Anticonvulsant derivatives useful in treating post traumatic stress disorder |
| US6399655B1 (en) | 1998-12-22 | 2002-06-04 | Johns Hopkins University, School Of Medicine | Method for the prophylactic treatment of cataracts |
| EA005815B1 (ru) | 1998-12-23 | 2005-06-30 | Джи.Ди.Сирл Ллс | Комбинация ингибиторов транспорта желчных кислот в подвздошной кишке и ингибиторов белка, переносящего эфиры холестерина, для сердечно-сосудистых показаний |
| EP1140134A1 (en) | 1998-12-24 | 2001-10-10 | R-Tech Ueno, Ltd. | Agent for treating visual cell function disorder |
| US6864232B1 (en) | 1998-12-24 | 2005-03-08 | Sucampo Ag | Agent for treating visual cell function disorder |
| EP1154691A4 (en) | 1999-01-05 | 2004-07-07 | Massachusetts Eye & Ear Infirm | TARGETED ADMINISTRATION OF REGULATED RELEASE MEDICINE TO RETINA AND CHOROID THROUGH SCLEROTIC |
| US6706283B1 (en) | 1999-02-10 | 2004-03-16 | Pfizer Inc | Controlled release by extrusion of solid amorphous dispersions of drugs |
| US7374779B2 (en) | 1999-02-26 | 2008-05-20 | Lipocine, Inc. | Pharmaceutical formulations and systems for improved absorption and multistage release of active agents |
| US6267985B1 (en) | 1999-06-30 | 2001-07-31 | Lipocine Inc. | Clear oil-containing pharmaceutical compositions |
| US6217895B1 (en) | 1999-03-22 | 2001-04-17 | Control Delivery Systems | Method for treating and/or preventing retinal diseases with sustained release corticosteroids |
| US6239113B1 (en) | 1999-03-31 | 2001-05-29 | Insite Vision, Incorporated | Topical treatment or prevention of ocular infections |
| US6254860B1 (en) | 1999-04-13 | 2001-07-03 | Allergan Sales, Inc. | Ocular treatment using cyclosporin-A derivatives |
| US7063857B1 (en) | 1999-04-30 | 2006-06-20 | Sucampo Ag | Use of macrolide compounds for the treatment of dry eye |
| EP1173177B2 (en) | 1999-04-30 | 2014-03-05 | Sucampo AG | Use of macrolide compounds for the treatment of dry eye |
| US6576224B1 (en) | 1999-07-06 | 2003-06-10 | Sinuspharma, Inc. | Aerosolized anti-infectives, anti-inflammatories, and decongestants for the treatment of sinusitis |
| JP2001064198A (ja) | 1999-08-24 | 2001-03-13 | Teika Seiyaku Kk | 角膜疾患治療剤 |
| AU7452900A (en) * | 1999-10-18 | 2001-04-30 | Fujisawa Pharmaceutical Co., Ltd. | Method for producing liposome preparation |
| CN1292721C (zh) | 1999-10-21 | 2007-01-03 | 爱尔康公司 | 药物释放装置 |
| PT1221918E (pt) | 1999-10-21 | 2005-06-30 | Alcon Inc | Administracao de drogas sub-tenon |
| US6416777B1 (en) | 1999-10-21 | 2002-07-09 | Alcon Universal Ltd. | Ophthalmic drug delivery device |
| ATE383873T1 (de) | 1999-10-22 | 2008-02-15 | Biogen Idec Inc | Verwendung eines cd40:cd154 bindungs- unterbrechers zur behandlung immunologischer komplikationen des auges |
| US6331313B1 (en) | 1999-10-22 | 2001-12-18 | Oculex Pharmaceticals, Inc. | Controlled-release biocompatible ocular drug delivery implant devices and methods |
| WO2001030337A2 (en) | 1999-10-22 | 2001-05-03 | Orbon Corporation | Ophthalmic formulation of dopamine antagonists |
| ES2283344T3 (es) | 1999-10-29 | 2007-11-01 | Kosan Biosciences, Inc. | Analogos de la rapamicina. |
| RU2149615C1 (ru) | 1999-11-10 | 2000-05-27 | Нестеров Аркадий Павлович | Способ введения лекарственных препаратов при заболеваниях заднего отрезка глаза |
| US6531464B1 (en) | 1999-12-07 | 2003-03-11 | Inotek Pharmaceutical Corporation | Methods for the treatment of neurodegenerative disorders using substituted phenanthridinone derivatives |
| AU784340B2 (en) | 1999-12-23 | 2006-03-16 | Pfizer Products Inc. | Pharmaceutical compositions providing enhanced drug concentrations |
| US6489335B2 (en) | 2000-02-18 | 2002-12-03 | Gholam A. Peyman | Treatment of ocular disease |
| US20030018044A1 (en) | 2000-02-18 | 2003-01-23 | Peyman Gholam A. | Treatment of ocular disease |
| DE60100866T2 (de) | 2000-04-07 | 2004-07-29 | Laboratoire Medidom S.A. | Cyklosporin, Hyaluronsäure und Polysorbate enthaltenes Augenarzneimittel |
| US6375972B1 (en) | 2000-04-26 | 2002-04-23 | Control Delivery Systems, Inc. | Sustained release drug delivery devices, methods of use, and methods of manufacturing thereof |
| CN1127955C (zh) | 2000-07-07 | 2003-11-19 | 中山医科大学中山眼科中心 | 一种眼前段及眼表免疫相关性疾病治疗药物 |
| CN1204919C (zh) | 2000-08-30 | 2005-06-08 | 中国科学院化学研究所 | 长效环孢素眼内释药体系 |
| ES2312456T3 (es) | 2000-08-30 | 2009-03-01 | Johns Hopkins University | Dispositivos para suministro intraocular de farmacos. |
| US6696483B2 (en) | 2000-10-03 | 2004-02-24 | Oncopharmaceutical, Inc. | Inhibitors of angiogenesis and tumor growth for local and systemic administration |
| US6534693B2 (en) | 2000-11-06 | 2003-03-18 | Afmedica, Inc. | Surgically implanted devices having reduced scar tissue formation |
| US20050084514A1 (en) | 2000-11-06 | 2005-04-21 | Afmedica, Inc. | Combination drug therapy for reducing scar tissue formation |
| US20040018228A1 (en) | 2000-11-06 | 2004-01-29 | Afmedica, Inc. | Compositions and methods for reducing scar tissue formation |
| DE60114229T2 (de) | 2000-11-29 | 2006-07-06 | Allergan, Inc., Irvine | Verhinderung von transplantatabstossung im auge |
| CA2433032C (en) | 2001-01-03 | 2008-11-25 | Bausch & Lomb Incorporated | Sustained release drug delivery devices with coated drug cores |
| AP2003002828A0 (en) | 2001-01-16 | 2003-09-30 | Vascular Therapies Llc | Implantable device containing resorbable matrix material and anti-proliferative drugs for preventing or treating failure of hemodialysis vascular access and other vascular grafts. |
| US7181287B2 (en) | 2001-02-13 | 2007-02-20 | Second Sight Medical Products, Inc. | Implantable drug delivery device |
| EP3406249A1 (en) | 2001-02-19 | 2018-11-28 | Novartis AG | Treatment of breast tumors with a rapamycin derivative in combination with an aromatase inhibitor |
| US6777000B2 (en) | 2001-02-28 | 2004-08-17 | Carrington Laboratories, Inc. | In-situ gel formation of pectin |
| US6713081B2 (en) | 2001-03-15 | 2004-03-30 | The United States Of America As Represented By The Department Of Health And Human Services | Ocular therapeutic agent delivery devices and methods for making and using such devices |
| AR033151A1 (es) | 2001-04-12 | 2003-12-03 | Sucampo Pharmaceuticals Inc | Agente para el tratamiento oftalmico topico de las enfermedades inflamatorias oculares |
| WO2002089767A1 (en) | 2001-05-03 | 2002-11-14 | Massachusetts Eye And Ear Infirmary | Implantable drug delivery device and use thereof |
| JP2002332225A (ja) | 2001-05-09 | 2002-11-22 | Lion Corp | 眼科用組成物 |
| EP2316394B1 (en) | 2001-06-12 | 2016-11-23 | The Johns Hopkins University | Reservoir device for intraocular drug delivery |
| US7034037B2 (en) | 2001-06-29 | 2006-04-25 | Ethicon, Inc. | Compositions and medical devices utilizing bioabsorbable polymeric waxes and rapamycin |
| CA2452372A1 (en) | 2001-07-06 | 2003-01-16 | Sucampo Ag | Composition for topical administration comprising an interleukin-2 inhibitor and an antimicrobial agent |
| AR035293A1 (es) | 2001-08-23 | 2004-05-05 | Novartis Ag | Composicion oftalmica. |
| US6812220B2 (en) | 2001-08-29 | 2004-11-02 | University Of British Columbia | Pharmaceutical compositions and methods relating to fucans |
| GB0122318D0 (en) | 2001-09-14 | 2001-11-07 | Novartis Ag | Organic compounds |
| JP2003113078A (ja) | 2001-09-28 | 2003-04-18 | Lion Corp | 眼科用製剤 |
| US6656460B2 (en) | 2001-11-01 | 2003-12-02 | Yissum Research Development | Method and composition for dry eye treatment |
| US6939376B2 (en) | 2001-11-05 | 2005-09-06 | Sun Biomedical, Ltd. | Drug-delivery endovascular stent and method for treating restenosis |
| EP1441743A4 (en) | 2001-11-09 | 2009-02-25 | Eyetech Pharmaceuticals | METHODS FOR TREATING NEOFORMATIONS OF OCULAR BLOOD VESSELS |
| US6663880B1 (en) | 2001-11-30 | 2003-12-16 | Advanced Cardiovascular Systems, Inc. | Permeabilizing reagents to increase drug delivery and a method of local delivery |
| EP1455810B1 (de) | 2001-12-14 | 2007-06-13 | Jagotec Ag | Arzneiformulierung enthaltend ciclosporin und deren verwendung |
| GB0200429D0 (en) | 2002-01-09 | 2002-02-27 | Novartis Ag | Organic compounds |
| CA2478424A1 (en) | 2002-03-01 | 2003-09-12 | Novagali Pharma Sa | Self emulsifying drug delivery systems for poorly soluble drugs |
| JP2003261449A (ja) * | 2002-03-05 | 2003-09-16 | Nisshin Oillio Ltd | ファモチジン含有水性注射剤およびその製造法 |
| US6941948B2 (en) | 2002-03-07 | 2005-09-13 | Vectura Drug Delivery | Medicament storage and delivery devices |
| CN1456350A (zh) | 2002-05-10 | 2003-11-19 | 刘继东 | 环孢素眼用凝胶 |
| US20040057958A1 (en) | 2002-05-17 | 2004-03-25 | Waggoner David W. | Immunogenicity-enhancing carriers and compositions thereof and methods of using the same |
| US7026374B2 (en) | 2002-06-25 | 2006-04-11 | Aruna Nathan | Injectable microdispersions for medical applications |
| EP2277898A3 (en) | 2002-07-16 | 2011-06-01 | Biotica Technology Limited | Rapamycin analogues |
| AU2003256068A1 (en) | 2002-08-09 | 2004-02-25 | Sucampo Pharmaceuticals, Inc. | Pharmaceutical compositions comprising fk506 derivatives and the ir use for the treatment of allergic diseases |
| WO2004027027A2 (en) | 2002-09-18 | 2004-04-01 | Trustees Of The University Of Pennsylvania | Method of inhibiting choroidal neovascularization |
| AU2003279055A1 (en) | 2002-09-29 | 2004-04-19 | Surmodics, Inc. | Methods for treatment and/or prevention of retinal disease |
| US7704518B2 (en) | 2003-08-04 | 2010-04-27 | Foamix, Ltd. | Foamable vehicle and pharmaceutical compositions thereof |
| US7354574B2 (en) | 2002-11-07 | 2008-04-08 | Advanced Ocular Systems Limited | Treatment of ocular disease |
| AU2003293529A1 (en) | 2002-12-16 | 2004-07-29 | Nitromed, Inc. | Nitrosated and nitrosylated rapamycin compounds, compositions and methods of use |
| AR042890A1 (es) | 2003-01-16 | 2005-07-06 | Sucampo Pharmaceuticals Inc | Metodo de tratamiento del ojo seco con una composicion oftalmica que contiene un compuesto macrolido |
| CA2516022C (en) | 2003-02-17 | 2012-05-29 | Cold Spring Harbor Laboratory | Model for studying the role of genes in tumor resistance to chemotherapy |
| JP2004269419A (ja) * | 2003-03-07 | 2004-09-30 | Mochida Pharmaceut Co Ltd | ミコナゾール含有水性注射剤 |
| US20050074497A1 (en) | 2003-04-09 | 2005-04-07 | Schultz Clyde L. | Hydrogels used to deliver medicaments to the eye for the treatment of posterior segment diseases |
| US20050255144A1 (en) | 2003-04-09 | 2005-11-17 | Directcontact Llc | Methods and articles for the delivery of medicaments to the eye for the treatment of posterior segment diseases |
| WO2004096261A1 (es) | 2003-05-02 | 2004-11-11 | Arturo Jimenez Bayardo | Metodo para preparar una solucion acuosa de ciclosporina-a y solucion acuosa resultante |
| US7160867B2 (en) | 2003-05-16 | 2007-01-09 | Isotechnika, Inc. | Rapamycin carbohydrate derivatives |
| US7674170B2 (en) | 2003-06-25 | 2010-03-09 | Odom James M | Method of lottery wagering on a real world phased competition |
| EP1635875B8 (en) | 2003-06-26 | 2008-12-24 | pSivida Inc | In-situ gelling drug delivery system |
| US7083802B2 (en) | 2003-07-31 | 2006-08-01 | Advanced Ocular Systems Limited | Treatment of ocular disease |
| US20050037048A1 (en) * | 2003-08-11 | 2005-02-17 | Young-Ho Song | Medical devices containing antioxidant and therapeutic agent |
| EP1510206A1 (en) | 2003-08-29 | 2005-03-02 | Novagali Pharma SA | Self-nanoemulsifying oily formulation for the administration of poorly water-soluble drugs |
| US7585517B2 (en) | 2003-09-18 | 2009-09-08 | Macusight, Inc. | Transscleral delivery |
| US20050181018A1 (en) | 2003-09-19 | 2005-08-18 | Peyman Gholam A. | Ocular drug delivery |
| US7087237B2 (en) | 2003-09-19 | 2006-08-08 | Advanced Ocular Systems Limited | Ocular solutions |
| US7083803B2 (en) | 2003-09-19 | 2006-08-01 | Advanced Ocular Systems Limited | Ocular solutions |
| US7402399B2 (en) | 2003-10-14 | 2008-07-22 | Monogram Biosciences, Inc. | Receptor tyrosine kinase signaling pathway analysis for diagnosis and therapy |
| WO2005051451A2 (en) | 2003-11-20 | 2005-06-09 | Angiotech International Ag | Electrical devices and anti-scarring agents |
| WO2005051316A2 (en) | 2003-11-20 | 2005-06-09 | Angiotech International Ag | Polymer compositions and methods for their use |
| WO2006053007A2 (en) | 2004-11-09 | 2006-05-18 | Angiotech Biocoatings Corp. | Antimicrobial needle coating for extended infusion |
| US7186518B2 (en) | 2003-11-21 | 2007-03-06 | Dade Behring Inc. | Method and composition useful for determining FK 506 |
| AU2004296851A1 (en) | 2003-12-08 | 2005-06-23 | Gel-Del Technologies, Inc. | Mucoadhesive drug delivery devices and methods of making and using thereof |
| US20050256081A1 (en) | 2004-02-26 | 2005-11-17 | Peyman Gholam A | Tetracycline derivatives for the treatment of ocular pathologies |
| WO2005094279A2 (en) | 2004-03-25 | 2005-10-13 | The Rothberg Institute For Childhood Diseases | Immortalized human tuberous sclerosis null angiomyolipoma cell and method of use thereof |
| US7846940B2 (en) | 2004-03-31 | 2010-12-07 | Cordis Corporation | Solution formulations of sirolimus and its analogs for CAD treatment |
| US20050245497A1 (en) | 2004-04-08 | 2005-11-03 | Penfold Philip L | Treatment of ophthalmic conditions |
| US20050244472A1 (en) | 2004-04-30 | 2005-11-03 | Allergan, Inc. | Intraocular drug delivery systems containing excipients with reduced toxicity and related methods |
| US20060182783A1 (en) | 2004-04-30 | 2006-08-17 | Allergan, Inc. | Sustained release intraocular drug delivery systems |
| US20050250804A1 (en) | 2004-05-06 | 2005-11-10 | Glenmark Pharmaceuticals Limited | Pharmaceutical gel formulations |
| US20060024350A1 (en) | 2004-06-24 | 2006-02-02 | Varner Signe E | Biodegradable ocular devices, methods and systems |
| US20060018948A1 (en) | 2004-06-24 | 2006-01-26 | Guire Patrick E | Biodegradable implantable medical devices, methods and systems |
| WO2006002365A2 (en) | 2004-06-24 | 2006-01-05 | Angiotech International Ag | Microparticles with high loadings of a bioactive agent |
| JP2008512350A (ja) | 2004-07-01 | 2008-04-24 | イェール ユニバーシティ | 標的化され、そして高密度で薬物が負荷されるポリマー性物質 |
| WO2006014484A2 (en) | 2004-07-02 | 2006-02-09 | Surmodics, Inc. | Methods and devices for the treatment of ocular conditions |
| WO2006020755A2 (en) | 2004-08-10 | 2006-02-23 | Beth Israel Deaconess Medical Center, Inc. | Methods for identifying inhibitors of the mtor pathway as diabetes therapeutics |
| WO2006023130A2 (en) | 2004-08-12 | 2006-03-02 | Surmodics, Inc. | Biodegradable controlled release bioactive agent delivery device |
| AR050374A1 (es) | 2004-08-20 | 2006-10-18 | Wyeth Corp | Forma polimorfica de rafampicina |
| EP1781672B1 (en) | 2004-08-27 | 2010-10-06 | Cordis Corporation | Solvent free amorphous rapamycin |
| EP3173072A1 (en) | 2004-10-01 | 2017-05-31 | Ramscor, Inc. | Conveniently implantable sustained release drug compositions |
| MX2007003789A (es) | 2004-10-04 | 2007-07-20 | Qlt Usa Inc | Suministro ocular de formulaciones polimericas para suministro. |
| DK1848431T3 (en) * | 2005-02-09 | 2016-04-18 | Santen Pharmaceutical Co Ltd | LIQUID FORMULATIONS FOR TREATMENT OF DISEASES OR CONDITIONS |
| GB0504995D0 (en) | 2005-03-11 | 2005-04-20 | Biotica Tech Ltd | Use of a compound |
| JP2008533204A (ja) | 2005-03-21 | 2008-08-21 | マクサイト, インコーポレイテッド | 病気又は症状の治療のためのドラッグ送達システム |
| US20060216288A1 (en) | 2005-03-22 | 2006-09-28 | Amgen Inc | Combinations for the treatment of cancer |
| JP2008535847A (ja) | 2005-04-08 | 2008-09-04 | サーモディクス,インコーポレイティド | 網膜下に送達するための持続放出インプラント |
| NZ563003A (en) | 2005-04-27 | 2011-03-31 | Univ Florida | Use of a farnesyl transferase inhibitor to enhance autophagic protein degradation in protein conformation disorders |
| US20060247265A1 (en) | 2005-04-28 | 2006-11-02 | Clackson Timothy P | Therapies for treating disorders of the eye |
| JP2009500297A (ja) | 2005-06-08 | 2009-01-08 | セントカー・インコーポレーテツド | 眼の変性についての細胞療法 |
| EP1904056B1 (en) | 2005-07-18 | 2009-04-29 | Minu, L.L.C. | Use of a macrolide to restore corneal sensation |
| US20070014760A1 (en) | 2005-07-18 | 2007-01-18 | Peyman Gholam A | Enhanced recovery following ocular surgery |
| US20070134244A1 (en) | 2005-10-14 | 2007-06-14 | Alcon, Inc. | Combination treatment for pathologic ocular angiogenesis |
| DE102006051512A1 (de) | 2005-12-06 | 2007-06-14 | Pari GmbH Spezialisten für effektive Inhalation | Pharmazeutische Medikamentenzusammensetzungen mit Cyclosporin |
| BRPI0706949A2 (pt) | 2006-01-23 | 2011-04-12 | Yissum Res Dev Co | microesferas, método de preparação de microesferas que compreendem uma pluralidade de nanocápsulas acomodadas em um polìmero formador de gel, composição farmacêutica, método para aumentar a biodisponibilidade de um agente lipofìlico no corpo de um indivìduo humano e método de tratamento de um indìviduo para uma condição patólogica que requer um nìvel eficaz ao sangue de um agente ativo |
| JP5528708B2 (ja) | 2006-02-09 | 2014-06-25 | 参天製薬株式会社 | 安定な製剤ならびにそれらを調製および使用する方法 |
| JP2009528381A (ja) | 2006-02-28 | 2009-08-06 | パロマ ファーマシューティカルズ,インク. | 細胞増殖および血管新生を特徴とする疾患を治療する組成物および方法 |
| CN101443004B (zh) | 2006-03-23 | 2013-03-06 | 参天制药株式会社 | 用于与血管通透性有关的疾病或病症的制剂 |
-
2007
- 2007-02-09 JP JP2008554395A patent/JP5528708B2/ja active Active
- 2007-02-09 US US11/704,442 patent/US8492400B2/en active Active
- 2007-02-09 AU AU2007212271A patent/AU2007212271B2/en active Active
- 2007-02-09 BR BRPI0707612A patent/BRPI0707612B8/pt active IP Right Grant
- 2007-02-09 WO PCT/US2007/003573 patent/WO2007092620A2/en active Application Filing
- 2007-02-09 KR KR1020147020142A patent/KR20140093764A/ko not_active Application Discontinuation
- 2007-02-09 CA CA2635797A patent/CA2635797C/en active Active
- 2007-02-09 CN CN2007800049514A patent/CN101605529B/zh active Active
- 2007-02-09 EP EP07763361A patent/EP2001438A2/en not_active Withdrawn
-
2008
- 2008-09-08 KR KR1020087021928A patent/KR101478164B1/ko active IP Right Grant
-
2013
- 2013-06-24 US US13/925,719 patent/US8658667B2/en active Active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1374872A (zh) * | 1998-12-07 | 2002-10-16 | 诺瓦提斯公司 | 大环内酯的稳定化 |
| CN1556694A (zh) * | 2000-06-06 | 2004-12-22 | ���չ�˾ | 对氧化作用敏感的活性组分水溶液制剂的制备方法 |
| CN1671385A (zh) * | 2002-07-30 | 2005-09-21 | 惠氏公司 | 含有瑞帕霉素羟基酯的胃肠外制剂 |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN107334734A (zh) * | 2017-07-10 | 2017-11-10 | 浙江大学 | 一种西罗莫司或其衍生物的眼用制剂 |
| CN107334734B (zh) * | 2017-07-10 | 2020-03-17 | 浙江大学 | 一种西罗莫司或其衍生物的眼用制剂 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2009528276A (ja) | 2009-08-06 |
| US8492400B2 (en) | 2013-07-23 |
| US20070203173A1 (en) | 2007-08-30 |
| JP5528708B2 (ja) | 2014-06-25 |
| US20140011834A1 (en) | 2014-01-09 |
| BRPI0707612B1 (pt) | 2020-09-24 |
| US8658667B2 (en) | 2014-02-25 |
| WO2007092620A3 (en) | 2009-03-26 |
| WO2007092620A2 (en) | 2007-08-16 |
| BRPI0707612A2 (pt) | 2011-05-10 |
| EP2001438A2 (en) | 2008-12-17 |
| KR20140093764A (ko) | 2014-07-28 |
| AU2007212271A1 (en) | 2007-08-16 |
| AU2007212271B2 (en) | 2012-11-01 |
| KR101478164B1 (ko) | 2014-12-31 |
| CN101605529A (zh) | 2009-12-16 |
| BRPI0707612B8 (pt) | 2021-05-25 |
| CA2635797C (en) | 2015-03-31 |
| CA2635797A1 (en) | 2007-08-16 |
| KR20080094814A (ko) | 2008-10-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN101605529B (zh) | 稳定制剂及它们的制备和使用方法 | |
| CN101137370B (zh) | 用于治疗疾病或病症的液体制剂 | |
| CN104147005B (zh) | 用于治疗疾病或病症的液体制剂 | |
| US8663639B2 (en) | Formulations for treating ocular diseases and conditions | |
| EP2187743B1 (en) | Rapamycin formulations for treatment of age related macular degeneration | |
| US20060257450A1 (en) | Drug delivery systems for treatment of diseases or conditions | |
| AU2012200274B2 (en) | Liquid formulations for treatment of diseases or conditions | |
| AU2013200089B2 (en) | Stable formulations, and methods of their preparation and use |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| ASS | Succession or assignment of patent right |
Effective date: 20110825 |
|
| C41 | Transfer of patent application or patent right or utility model | ||
| TA01 | Transfer of patent application right |
Effective date of registration: 20110825 Address after: Osaka Japan Applicant after: Santen Pharmaceutical Co., Ltd. Address before: American California Applicant before: Macusight Inc. |
|
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant |